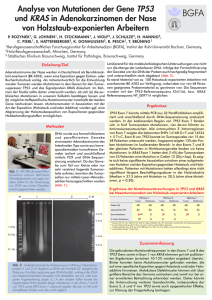
Die prognostische Bedeutung von Mutationen im WT1
Werbung

Zentrum für Innere Medizin der Universität Ulm Klinik für Innere Medizin III Hämatologie, Onkologie, Rheumatologie und Infektionskrankheiten Ärztlicher Direktor: Prof. Dr. med. Hartmut Döhner Die prognostische Bedeutung von Mutationen im WT1Gen bei der akuten myeloischen Leukämie mit normalem Karyotyp Dissertation zur Erlangung des Doktorgrades der Medizin der Medizinischen Fakultät der Universität Ulm Vorgelegt von Simone Moschny, aus Sulzbach-Rosenberg 2012 Amtierender Dekan: Prof. Dr. Thomas Wirth 1. Berichterstatter: Prof. Dr. Konstanze Döhner 2. Berichterstatter: Prof. Dr. Daniel Walcher Tag der Promotion: 11.07.2013 Inhalt Inhalt ....................................................................................................................... I Abkürzungsverzeichnis ........................................................................................... I 1 2 Einleitung ......................................................................................................... 1 1.1 Die akute myeloische Leukämie ................................................................ 1 1.2 Die Bedeutung von molekularen Markern in der AML ............................... 4 1.3 Das WT1-Gen ........................................................................................... 8 1.3.1 Aufbau des WT1-Gens ....................................................................... 8 1.3.2 Die Isoformen von WT1 ...................................................................... 8 1.3.3 Expression und Funktion des WT1-Proteins ....................................... 9 1.3.4 Die Rolle von WT1 in der Onkogenese............................................. 10 1.3.5 Die Bedeutung von WT1 bei der AML .............................................. 11 Material und Methoden .................................................................................. 15 2.1 Geräte- und Reagenzienliste ................................................................... 15 2.2 Patientenkollektiv .................................................................................... 16 2.3 Materialgewinnung und –aufbereitung .................................................... 16 2.4 DNA-Extraktion ....................................................................................... 17 2.5 Polymerasekettenreaktion ....................................................................... 18 2.5.1 2.6 Gelelektrophorese ................................................................................... 20 2.6.1 2.7 3 Durchführung der Fast-PCR ............................................................. 18 Aufreinigung des PCR-Produkts ....................................................... 22 Cycle Sequencing Reaction (CSR) ......................................................... 22 2.7.1 Durchführung der CSR ..................................................................... 22 2.7.2 Aufreinigung des CSR-Produkts ....................................................... 24 2.8 Sequenzierung und Identifizierung von Mutationen ................................ 24 2.9 Statistische Auswertung .......................................................................... 25 Ergebnisse ..................................................................................................... 27 I 3.1 Inzidenz von WT1-Mutationen ................................................................. 27 3.2 Assoziation mit anderen molekularen Markern ....................................... 31 3.3 Assoziation von WT1-Mutationen mit klinischen Charakteristika ............ 32 3.4 Prognostische Bedeutung von WT1-Mutationen für das Ansprechen auf Induktionstherapie ............................................................................................. 34 3.5 4 Prognostische Bedeutung von WT1-Mutationen für das Überleben ........ 34 Diskussion ..................................................................................................... 37 4.1 Häufigkeit von WT1-Mutationen .............................................................. 37 4.2 Lokalisation der Mutationen und Mutationstyp ........................................ 37 4.3 Assoziation von WT1-Mutationen mit klinischen Charakteristika und molekularen Markern ........................................................................................ 38 4.4 Prognostische Bedeutung von WT1-Mutationen ..................................... 39 4.5 Schlussfolgerung ..................................................................................... 41 5 Zusammenfassung ........................................................................................ 43 6 Literaturverzeichnis ........................................................................................ 45 II Abkürzungsverzeichnis a: Jahre ALL: Akute lymphatische Leukämie AML: Akute myeloische Leukämie AMLSG: AML Study Group BASP1-Gen: Brain acid soluble protein 1-Gen bp: Basenpaare bs: Buccal swab CALGB: Cancer and Leukemia Group B CBFB-Gen: Core-binding factor subunit beta-Gen CD: Cluster of Differentiation CEBPA-Gen: CCAAT/enhancer binding protein alpha CR: Complete Remission CSR: Cycle Sequencing Reaction ddNTP: Didesoxyribonukleosidtriphosphate DDS: Denys-Drash-Syndrom del: Deletion DFS: Disease-free survival DNA: Desoxyribonukleinsäure dNTP: Desoxynukleosidtriphosphate EVI1-Gen: Ecotropic viral integration site 1-Gen FAB-Klassifikation: French-American-British-Klassifikation FLT3-Gen: FMS-like-Tyrosinkinase 3 FMS: Fibromyalgie-Syndrom HR: Hazard Ratio ins: Insertion ITD: Internal tandem duplication KM: Knochenmark LDH: Laktatdehydrogenase Mg: Magnesium MKL1-Gen: Myocardin-like protein 1-Gen MLL-Gen: Mixed Lineage Leukemia-Gen MRC: Medical Research Council I mut: mutiert n: Anzahl neg: negativ NPM1-Gen: Nucleophosmin 1-Gen NRAS-Gen: Neuroblastoma Rat Sarcoma-Gen NUP214-Gen: Nuclear core complex protein 214-Gen OR: Odds Ratio OS: Overall survival p: p-Wert PB: Peripheres Blut PCR: Polymerasekettenreaktion PML-Gen: Promyelocytic leukemia-Gen pos: Positiv PTD: Partial tandem duplication RARA-Gen: Retinoic acid receptor-alpha-Gen RAS-Gen: Rat Sarcoma-Gen RBM15-Gen: RNA-binding protein 15-Gen RFS: Relapse-free survival rm: Remission material RNA: Ribonukleinsäure RPMI 1640 Kulturmedium: Roswell Park Memorial Institute RPN1-Gen: Dolichyl-diphosphooligosaccharide-protein glycosyltransferase subunit 1 RUNX-Gen: Runt-related transcription factor-Gen s-AML: Sekundäre akute myeloische Leukämie t: Translokation t-AML: Therapieassoziierte akute myeloische Leukämie TKD: Tyrosin kinase domain U: Umdrehungen WAGR-Syndrom: Kongenitales Syndrom mit Wilms’ Tumor, Aniridie, urogenitalen Missbildungen und geistiger Retardierung WBC: White blood cells WHO: World Health Organization II wt: Wildtyp WT1-Gen: Wilms’ Tumor 1-Gen WTIP-Gen: Wilms tumor 1 interacting protein-Gen III 1 Einleitung 1.1 Die akute myeloische Leukämie Die akute myeloische Leukämie (AML) ist eine maligne, monoklonale Erkrankung des Knochenmarks. Sie ist durch eine Erhöhung der Leukozyten im Blut gekennzeichnet, wobei das Auftreten von Myeloblasten im Differentialblutbild charakteristisch ist. Morphologisch wird das Vorliegen von mindestens 20% Myeloblasten im Knochenmark für die Diagnose akute myeloische Leukämie definiert. Bis zu Beginn der 90er Jahre wurde die AML mittels der FABKlassifikation in mehrere Subtypen unterteilt: M0: Undifferenzierte Leukämie M1: Myeloische Leukämie ohne Ausreifung M2: Myeloische Leukämie mit Ausreifung M3: Promyelozyten-Leukämie M4: Myelomonozytäre Leukämie M5: Monoblasten-Leukämie 5A: ohne Ausreifung 5B: mit Ausreifung M6: Erythrozyten-Leukämie M7: Megakaryozyten-Leukämie Basierend auf den Forschungsergebnissen der letzten Jahre wurde diese Klassifikation weiterentwickelt und auch das Vorhandensein genetischer Aberrationen berücksichtigt. Die letzte Auflage der neuen WHO-Klassifikation erfolgte im August 2008. Auf Grund ihrer prognostischen Bedeutung enthält diese erstmalig auch die molekularen Marker Nucleophosmin 1 (NPM1) und CCAAT/enhancer binding protein alpha (CEBPA) (Vardiman et al. 2009): 1 als provisorische Entität Tabelle 1: WHO-Klassifikation der akuten myeloischen Leukämie (AML) (Vardiman et al. 2009) 1. AML mit wiederkehrenden zytogenetischen Abnormalitäten 1.1 AML mit balancierten Translokationen/Inversionen - AML mit t(8;21)(q22;q22); RUNX1-RUNX1T1 - AML mit inv(16)(p13.1;q22) oder t(16;16)(p13.1;q22); CBFB-MYH11 - akute Promyelozyten-Leukämie mit t(15;17)(q22;q12)(PML/RARA) - AML mit t(9;11)(p22;q23); MLLT3-MLL - AML mit t(6;9)(p23;q34); DEK-NUP214 - AML mit inv(3)(q21;q26.2) oder t(3;3)(q21;q26.2); RPN1-EVI1 - AML (megakaryoblastisch) mit t(1;22)(p13;q13); RBM15-MKL1 1.2 AML mit Genmutationen 2. AML mit myelodysplasieverwandten Veränderungen 3. AML, therapiebedingte 4. AML, nicht anderweitig klassifiziert - AML mit minimaler Differenzierung - AML ohne Ausreifung - AML mit Ausreifung - Akute myelomonozytäre Leukämie - Akute monoblastische und monozytäre Leukämie - Akute Erythroleukämie - Akute Megakaryoblastenleukämie - Akute Basophilen-Leukämie - Akute Panmyelosis mit Myelofibrose 5. Myeloisches Sarkom 6. Myeloische Proliferationen bei Down-Syndrom 6.1 Transient abnormale Myelopoese 6.2 Myeloische Leukämie assoziiert mit Down-Syndrom 7. Blastische plasmazytoide dendritische Zell-Neoplasien 2 Im Weiteren wird empfohlen, den FMS like Tyrosinkinase 3 (FLT3)-Status zu bestimmen. Die AML ist charakterisiert durch eine Anhäufung erworbener somatischer genetischer Veränderungen, die sich auf Zellproliferation, Zelldifferenzierung und Apoptose auswirken. Diese genetischen Veränderungen können in zwei Formen vorliegen, entweder in Form einer chromosomalen Aberration oder durch sogenannte submikroskopische Veränderungen, wie Genmutationen oder eine veränderte Genexpression. Mittels zytogenetischer Untersuchungen lassen sich bei der AML in ca. 50% der Fälle balancierte und unbalancierte Chromosomenaberrrationen detektieren. Zahlreiche prospektive und retrospektive Studien in den 90er Jahre haben gezeigt, dass der Karyotyp den wichtigsten Prognosefaktor bei Diagnose darstellt und eine Einteilung der AML-Patienten in die drei Risikogruppen erlaubt: Niedrig-, Intermediär und Hochrisiko (Mrózek u. Bloomfield 2006). Anhand dieser Einteilung kann nicht nur die Prognoseeinschätzung des Patienten vorgenommen werden, sondern sie ist auch Basis für Therapieentscheidungen. So zählt unter anderem die Translokation t(8;21) zu der Niedrigrisikogruppe, die mit einer weniger intensiven Therapie kurativ behandelt werden kann, während ein komplexer Karyotyp per se mit einer eher schlechten Prognose vergesellschaftet ist und nur durch eine allogene Blutstammzelltransplantation kurativ therapiert werden kann (Mrózek u. Bloomfield 2006). Bisherige Daten legen nahe, dass die verschiedenen genetischen Veränderungen in der Leukämogenese kooperieren; dies wird auch im so genannten 2-KlassenModell beschrieben: Klasse 1-Mutationen führen zur Aktivierung der Signaltransduktion. Hieraus resultieren eine gesteigerte Proliferation und eine Apoptosehemmung der Leukämie-Progenitorzellen. Zu diesen Klasse 1-Mutationen zählen unter anderem Mutationen des FLT3-Gens. Die Klasse 2-Mutationen betreffen Transkriptionsfaktoren, was eine gestörte Ausdifferenzierung der Zelle zur Folge hat (Kelly und Gilliland 2002) 3 1.2 Die Bedeutung von molekularen Markern in der AML Bei etwa 40-49 % der Erwachsenen mit AML liegen keine chromosomalen Aberrationen vor (Mrózek et al. 2007). Dieser normale Karyotyp wird der Gruppe mit Intermediärrisiko zugeordnet, obwohl diese Patientengruppe hinsichtlich ihrer Prognose sehr heterogen ist. Auf Grund dieser Tatsache ist es notwendig, diese Gruppe anhand weiterer prognostischer Faktoren zu unterteilen. In den letzten Jahren konnten mit Hilfe neuer molekulargenetischer Techniken neue molekulare Marker identifiziert werden, die nicht nur pathogenetisch relevant sind, sondern auch eine prognostische Bedeutung aufweisen (Schlenk et al. 2008). Zu diesen molekularen Markern gehören die Gene NPM1, FLT3, CEBPA und das mixed lineage bzw. myeloid lymphoid leukemia (MLL) Gen. FLT3 lässt sich den Klasse 1-Mutationen zuordnen, während CEBPA und MLL, möglicherweise auch NPM1, zu den Klasse 2-Mutationen zählen (Schlenk et al. 2008). Mittels dieser molekularen Marker kann nicht nur die Prognose des einzelnen Patienten bestimmt werden, sondern sie bilden auch die Grundlage für eine Individualisierung der Therapie gemäß dem genetischen Risikoprofil und haben somit entscheidenden Einfluss auf das weitere therapeutische Vorgehen. Die Häufigkeit der genetischen Aberrationen ist in Abbildung 1 dargestellt. Dabei fällt auf, dass oben genannte Mutationen vor allem bei Patienten mit normalem Karyotyp auftreten. Dagegen finden sich bei der AML mit komplexem Karyotyp deutlich weniger Mutationen in oben genannten Genen (Döhner u. Döhner 2008). Mutationen im NPM1-Gen treten bei ungefähr 35,2% aller AML-Patienten bzw. 48% der AML-Patienten mit normalem Karyotyp auf (Falini et al. 2005; Döhner et al. 2005). Beim FLT3-Gen unterscheidet man zwei Arten von Mutationen, zum einen interne Tandemduplikationen (FLT3-ITD) und zum anderen Mutationen in der Tyrosinkinase-Domäne (FLT3-TKD) (Stirewalt u. Radich 2003). Der Genotyp FLT3-ITDpos findet sich bei etwa 25% aller AML-Patienten bzw bei 31% der Patienten mit normalem Karyotyp. Dieser Genotyp ist mit einer sehr schlechten Prognose assoziiert. Sowohl das rezidivfreie Überleben (RFS) als auch das 4 Gesamtüberleben (OS) sind in dieser Patientengruppe deutlich geringer (Stirewalt u. Radich 2003; Döhner u. Döhner 2008; Schlenk et al. 2008). 45% normaler Karyotyp NPM1 , FLT3, CEBPA , MLL , WT1, RUNX1 , RAS 11% komplexer Karyotyp TP53 KIT RAS FLT3 5% t(8;21) 23% verschiedene 6% inv(16) 2% t(9;11) NPM1 , CEBPA , 2% t(11q23) MLL , RUNX1 1% t(6;9) FLT3 1% inv(3)/t(3;3) NRAS Abbildung 1: Darstellung der zytogenetischen Subgruppen bei der AML und der mutierten Gene (Döhner u. Döhner 2008) Etwa 40% (Döhner u. Döhner 2008) der NPM1-Mutationen gehen mit einer internen Tandemduplikation im FLT3-Gen (FLT3-ITD) einher. Der Genotyp NPM1mut/FLT3-ITDneg ist mit einer guten Prognose assoziiert. Fast alle Patienten erreichen eine komplette Remission und die Rezidivrate ist niedrig. (Döhner u. Döhner 2008; Schlenk et al. 2008). Die Inzidenz von FLT3-TKD-Mutationen variiert zwischen 5% und 11% der Patienten mit normalem Karyotyp (Stirewalt u. Radich 2003; Mead et al. 2007; Döhner u. Döhner 2008; Gaidzik et al. 2008). Allerdings ist die prognostische Bedeutung dieser Mutation noch weitgehend unklar, da in den bisherigen Studien sowohl negative als auch positive Effekte dieser Mutation beschrieben wurden. So beschreiben Stirewalt u. Radich ein eher schlechteres Outcome, während die Studie von Mead et al. auf eine eher günstigere Prognose bei FLT3-TKDMutationen hinweist. 5 Mutationen im CEBPA-Gen wurden erstmals 2001 beschrieben. Hier konnte bei ca. 7,8% aller AML-Patienten eine CEBPA-Mutation gezeigt werden (Pabst et al. 2001), bei Patienten mit normalem Karyotyp variiert die Inzidenz zwischen 12,8% und 15%. (Fröhling et al. 2004; Tenen 2001; Taskesen et al. 2011; Schlenk et al. 2008). In den ersten Studien zur prognostischen Bedeutung zeigte sich bereits ein positiver Effekt von CEBPA-Mutationen auf die Prognose der Patienten (Fröhling et al.2004). Aktuelle Studien zeigen allerdings, dass nur Patienten mit biallelischer CEBPA-Mutation eine günstigere Prognose hinsichtlich kompletter Remission (CR), rezidivfreiem Überleben (RFS) und Gesamtüberleben (OS) aufweisen, während sich bei Patienten mit monoallelischer CEBPA-Mutation kein Unterschied zum Wildtyp zeigt (Wouters et al. 2009; Taskesen et al. 2011). Sowohl die AML mit mutiertem NPM1 als auch die AML mit mutiertem CEBPA wurde in die WHOKlassifikation von 2008 als sogenannte provisorische Entität aufgenommen (Vardiman et al. 2009). Bei ca. 11% der Patienten mit normalem Karyotyp zeigen sich partielle TandemDuplikationen im MLL-Gen (MLL-PTD). Bei diesen Mutationen wird von einer eher schlechten Prognose ausgegangen. So zeigte sich eine signifikant verkürzte Dauer der CR (Caligiuri et al. 1998; Döhner et al. 2002). Allerdings war kein Einfluss von MLL-PTD Mutationen auf das OS nachweisbar (Döhner et al. 2002; Mrózek u. Bloomfield 2006). Betrachtet man nun die Inzidenz der einzelnen molekularen Marker in Hinblick auf das zuvor beschriebene 2-Klassen-Modell, dann fällt auf, dass nur bei wenigen Patienten mehr als eine Mutation derselben Klasse auftritt. Dabei zeigt sich, dass NPM1-Mutationen häufig mit FLT3-Mutationen, dagegen nach bisherigen Daten nicht mit CEBPA-Mutationen assoziiert sind; NPM1 spielt sowohl in der Zelldifferenzierung als auch in der Proliferation eine entscheidende Rolle. Das oben beschriebene gemeinsame Auftreten von Genmutationen unterstützt die Hypothese, NPM1-Mutationen zu den Klasse-2-Mutationen zu zählen (Falini et al. 2005; Falini et al. 2007; Döhner u. Döhner 2008; Schlenk et al. 2008) Wie bereits erwähnt, hängt die Prognose der AML-Patienten entscheidend von dem jeweiligen molekulargenetischen Profil ab. So konnten u.a. Schlenk und 6 Döhner zeigen, dass NPM1- und CEBPA-Mutationen zu den günstigen Genotypen zählen, solange keine zusätzliche FLT3-ITD Mutation vorliegt. Alle anderen Markerkonstellationen hingegen, wie z.B. die NPM1mut/FLT3-ITDpos, sind mit einer schlechten Prognose assoziiert; der eigentlich günstige Einfluss der NPMMutation scheint hier keinen Effekt mehr aufzuweisen. In einer aktuellen Studie konnte eindrucksvoll gezeigt werden, dass Patienten mit dem Genotyp FLT3-ITDpos von einer allogenen Stammzelltransplantation profitieren, während dieser Effekt bei Patienten mit dem günstigen Genotyp NPM1mut/FLT3-ITDneg nicht festzustellen ist, so dass diese Patienten primär keinem allogenen Transplantationskonzept zugeführt werden, zumal die allogene Stammzelltransplantation mit einer Therapie-assoziierten Mortalität von ca. 20% einhergeht (Schlenk et al. 2008). Nach aktueller Datenlage können Patienten mit dem Genotyp NPM1mut/FLT3-ITDneg der Gruppe mit Niedrigrisiko zugeordnet werden (Schlenk et al. 2008). Der „Triple-negative“ Genotyp NPM1wt/CEBPAwt/FLT3-ITDneg weist wiederum eine schlechte Prognose auf. Neuste Studien zeigen, dass CEBPA-Mutationen nur dann zur Niedrigrisikogruppe gezählt werden können, wenn beide Allele eine Mutation tragen. Eine CEBPAsingle-Mutation zeigt dagegen nur einen geringgradigen Benefit verglichen mit dem Wildtyp-Allel und ist abhängig von dem Auftreten einer konkurrenten Mutation (Taskesen et al. 2011). Ziel der aktuellen Forschung ist es, durch die Analyse weiterer molekularer Marker oder die Definition bestimmter Genotypen eine möglichst genaue Prognoseabschätzung für den Patienten zu ermöglichen und diesem eine individuelle Therapie zukommen zu lassen. Ein weiterer, potentiell interessanter Marker, dessen prognostische Bedeutung bei der AML bislang völlig unklar war, ist das Wilms Tumor 1-Gen (WT1). 7 1.3 Das WT1-Gen 1.3.1 Aufbau des WT1-Gens Das WT1-Gen, welches in der chromosomalen Bande 11p13 lokalisiert ist, wurde 1990 erstmals kloniert. Die Region, in der sich das Gen befindet, konnte auf 345 Kilobasenpaare eingegrenzt werden, wobei das Transkript etwa 50 Kilobasenpaare enthält (Call et al. 1990). Das Gen setzt sich aus zehn Exons zusammen. Dabei befinden sich N-terminal Prolin- und Glutamin-reiche Sequenzen, die an der Interaktion mit RNA oder Proteinen beteiligt sind (Exon 1-6). Am C-terminalen Ende enthält das WT1Protein vier terminale Zinkfinger, die wesentlich für seine Funktion als Transkriptionsfaktor sind und in den Exons 7-10 kodiert werden (Call et al. 1990; Hohenstein u. Hastie 2006; Menke et al. 1998). Abbildung 2: Schematische Darstellung des Wilms Tumor 1-Gens (Gaidzik et al. 2009) 1.3.2 Die Isoformen von WT1 Die Funktionsweise des WT1-Proteins und vor allem die Auswirkungen von Mutationen sind immer noch unklar, da es mehrere verschiedene Isoformen des WT1-Proteins gibt, die zum Teil gegensätzliche Funktionen haben. Diese Isoformen entstehen durch alternatives Splicing, alternative Startcodons und RNAEditing. Die wichtigsten Isoformen scheinen die KTS-Isoformen von Exon 5 zu sein. Hier werden drei Aminosäuren zwischen dem dritten und dem vierten Zinkfinger entweder eingebaut oder weggelassen. Im Mausmodell konnte gezeigt 8 werden, dass die Veränderung dieser Isoformen, d.h. dass entweder nur +KTSoder -KTS-Isoformen exprimiert werden, Nierendefekte zur Folge haben, die kurz nach der Geburt zum Tod führen (Hohenstein u. Hastie 2006). 1.3.3 Expression und Funktion des WT1-Proteins Die Expression von WT1 ist während der Embryogenese am höchsten, wo es in multipotenten Progenitorzellen verschiedener Gewebe, v.a. des urogenitalen System, nachgewiesen werden kann (Pritchard-Jones et al. 1994). Im Erwachsenenalter findet sich WT1 fast ausschließlich in der Niere und den Gonaden exprimiert, wohingegen die Expression in den Knochenmarkzellen deutlich geringer und im Wesentlichen auf die CD34 + Vorläuferzellen beschränkt ist (King-Underwood et al. 1996). WT1 „knock-out Mausmodelle“ belegen klar, dass WT1 für die Entwicklung des urogenitalen Systems essentiell ist, jedoch keine signifikanten Effekte auf das hämatopoetische System hat. Trotz dieser Beobachtung wird WT1 in vielen Leukämien überexprimiert und stellt somit ein attraktives Target für eine Immuntherapie dar und wird auch für den Nachweis minimaler Resterkrankung verwendet (Inoue et al. 1997). Für das WT1-Protein konnten verschiedene Funktionen ermittelt werden. Wie sich schon aus seiner Struktur mit vier Zinkfingern schließen lässt, agiert es als Transkriptionsfaktor. WT1 kann sowohl die Transkription aktivieren als auch supprimieren. Für die Supprimierung der Transkription sind zwei Co-Suppressoren beschrieben worden: BASP1 und WTIP. Allerdings besitzen nur die –KTSIsoformen eine ausreichend hohe Affinität zur DNA, um als Transkriptionsfaktoren zu agieren. Die +KTS-Isoformen scheinen dagegen am RNA-Metabolismus beteiligt zu sein, eventuell im Bereich des Splicing (Hohenstein u. Hastie 2006). Außerdem konnte WT1 auch im Zytoplasma und an den Ribosomen nachgewiesen werden, was darauf hindeutet, dass WT1 auch für die Translation von Bedeutung ist. Diese Funktion beschränkt sich ebenfalls auf die +KTSIsoformen (Hohenstein u. Hastie 2006). In Modell mit knock out-Mäusen konnte nachgewiesen werden, dass das WT1Protein an der Entwicklung verschiedener mesodermaler Gewebe, wie zum 9 Beispiel des Urogenitaltrakts, der Herzkranzgefäße und der Milz, beteiligt ist. So ist das WT1-Protein wesentlich für die Ausbildung von Nephronen in der Niere, indem es zur Differenzierung der Zellen beiträgt und diese vor Apoptose schützt. Außerdem scheint es auch bei der Proliferation von neuronalen und vaskulären Progenitorzellen eine Rolle zu spielen (Hohenstein u. Hastie 2006). 1.3.4 Die Rolle von WT1 in der Onkogenese Die ersten Mutationen im WT1-Gen wurden 1978 bei drei Patienten mit dem WAGR-Syndrom Fehlbildungen Symptome (Kombination und mentaler aufwiesen: aus Wilms’ Retardierung) Aniridie, Fehlbildung Tumor, Aniridie, identifiziert, des urogenitalen welche Genitale und folgende mentale Retardierung. Bei diesen Mutationen handelte es sich um Deletionen auf dem kurzen Arm von Chromosom 11, wo WT1 lokalisiert ist. Einer der oben beschriebenen Patienten entwickelte einen Wilms’ Tumor, so dass man von einem angeborenen Defekt des WT1-Gens ausging und so zum ersten Mal die Bedeutung von WT1 in der Onkogenese beschrieben wurde (Riccardi et al. 1978). Außer bei dem WAGR-Syndrom sind Keimbahnmutationen in den Zinkfingerregionen des WT1-Gens auch bei der Entstehung des Denys-DrashSyndroms (DDS) und des Frasier-Syndroms beteiligt, die alle mit Missbildungen im Urogenitaltrakt und einem erhöhten Risiko für einen Wilms’ Tumor einhergehen (King-Underwood et al. 1996). Mutationen im WT1-Gen, sowohl homozygot als auch heterozygot, treten bei etwa 10 % der Wilms’ Tumoren auf (King-Underwood et al. 1996). Dabei verhält sich WT1 hier meist wie ein Tumorsuppressorgen, dessen Inaktivierung nach dem Second-Hit-Modell zur Entstehung von Wilms’ Tumoren beitragen kann (Call et al. 1990; King-Underwood et al. 1996). Second-Hit bedeutet, dass in der Keimbahn bereits eine heterozygote Mutation vorliegt. Wenn zu dieser zusätzlich eine zufällige Mutation des gesunden Allels auftritt, kommt es zur Entstehung des Wilms‘ Tumors. Damit liegen zwei mutierte Allele in den Tumorzellen vor. Im Gegensatz dazu wurden nur bei wenigen hereditären und sporadischen Wilms’ Tumoren heterozygote Mutationen gefunden. WT1 könnte folglich auch als 10 Onkogen fungieren. Abgesehen davon besteht die Möglichkeit, dass hier die Tumorentstehung nicht auf die WT1-Mutation per se zurückzuführen ist, sondern durch Interaktion mit anderen, eventuell mutierten, Genen entsteht (Haber et al. 1990). Schließlich fand man auch bei verschiedenen Tumorentitäten von Erwachsenen eine erhöhte Expression von WT1, unter anderem in kolorektalen Karzinomen und Hirntumoren (Hohenstein u. Hastie 2006). Allerdings wurden hier keine Mutationen im WT1-Gen gefunden. Die Tumorentstehung ist in diesen Fällen scheinbar allein auf die gesteigerte Expression von WT1 zurückzuführen, das in oben genannten Geweben beim Erwachsenen normalerweise nicht vorkommt (Hohenstein u. Hastie 2006). 1.3.5 Die Bedeutung von WT1 bei der AML Bei der Untersuchung der Expression von WT1 in der normalen Hämatopoese konnte festgestellt werden, dass WT1 nur in den CD34+-Zellen, also den frühen hämatopoetischen Progenitorzellen, exprimiert wird. So scheinen auch WT1Mutationen besonders in den schlecht differenzierten Formen der myeloischen und lymphatischen Leukämien eine Rolle zu spielen (King-Underwood et al. 1996). Schließlich konnte in der Mehrzahl der Fälle von AML eine Expression von WT1 nachgewiesen werden, während WT1 bei der Differenzierung in der normalen Hämatopoese herunter reguliert wird (Pritchard-Jones et al. 1994; KingUnderwood et al. 1996). Schon 1990 wurde die Expression von WT1 bei einem Patienten mit Erythroleukämie und einem Patienten mit einer akuten lymphatischen Leukämie (ALL) beschrieben (Call et al. 1990), wobei diese Expression wahrscheinlich auf den Differenzierungsgrad der hämatopoetischen Zellen, und nicht auf eine WT1Mutation zurückzuführen ist (Pritchard-Jones et al. 1994). Die erste WT1-Mutation in Zusammenhang mit Leukämie wurde bei einer WAGRPatientin mit sekundärer AML detektiert. Die AML trat dabei 17 Jahre nach Remission eines Wilms‘ Tumors auf. Bei diesem Fall zeigte sich eine Punktmutation in Codon 385 des WT1-Gens (3. Zinkfinger). Diese hatte einen 11 Austausch von Guanin gegen Adenin zur Folge, wodurch im WT1-Protein Cystein durch Tyrosin ersetzt wurde. Da bei der Patientin eine angeborene Deletion eines WT1-Gens vorlag, handelte es sich hier also um eine homozygote Mutation (Pritchard-Jones et al. 1994). Im Anschluss daran wurde 1996 und 1998 je eine weitere Studie zur Mutationsanalyse bei verschiedenen Leukämien durchgeführt. 1996 wurden von der britischen Arbeitsgruppe um King-Underwood erstmals WT1-Mutationen bei ca. 15% der AML-Patienten beschrieben (King-Underwood et al. 1996). Diese Mutationen waren überwiegend in den Exons 1, 7 und 9 lokalisiert. Insertionen in Exon 1 und 7 führen auf Proteinebene zu einem trunkierten WT1-Protein mit entweder komplettem Fehlen oder kompletter Zerstörung der funktionell wichtigen Zinkfinger-Region. In Exon 9 wurde eine Nonsense-Mutation beschrieben, durch welche nur die beiden letzten Zinkfinger verloren gehen (King-Underwood et al. 1996). Des Weiteren wurde eine Assoziation von WT1-Mutationen mit aggressiven Formen der AML festgestellt. Die Patienten zeigten ein schlechtes Ansprechen auf Chemotherapie und nur einer von vier Patienten erreichte eine CR. In einer Anschlussstudie von 1998 wurden erneut Leukämie-Patienten auf WT1Mutationen untersucht. Bei den AML-Patienten wurden wiederum Insertionen in Exon 1 und 7 sowie eine Punktmutation in Exon 6 detektiert. Des Weiteren wurde eine Missense-Mutation in Exon 9 festgestellt, die bereits als homozygote Mutation im Wilms’ Tumor von Patienten mit Denys-Drash-Syndrom beschrieben worden war. Im Gegensatz zum Wilms’ Tumor traten bei der AML meist heterozygote Mutationen auf. In wenigen Fällen konnten auch homozygote Mutationen nachgewiesen werden (King-Underwood u. Pritchard-Jones 1998). Auch in dieser Studie waren WT1-Mutationen mit einer schlechten Prognose assoziiert. Die Tatsache, dass sich Mutationstypen, die in Wilms’ Tumoren nachgewiesen werden können (v.a. große Deletionen, Punktmutationen) von denen bei der AML (v.a. Insertionen) unterscheiden, legt nahe, dass die pathogenetischen Mechanismen von WT1 auf hämatopoetische Zellen und urogenitales Gewebe unterschiedlich sind. Diese Hypothese konnte in Experimenten mit Knock-outMäusen unterstützt werden. Denn bei diesen WT1-/--Mäusen konnte keine Störung der Hämatopoese festgestellt werden, was darauf schließen lässt, dass ein 12 komplettes Fehlen des WT1-Proteins keinen wesentlichen Einfluss auf die Hämatopoese hat, aber der onkogene Effekt möglicherweise durch ein mutiertes WT1-Gen entsteht (Kreidberg et al. 1993; Pritchard-Jones et al. 1994). Dagegen zeigte sich, bei WT1-/--Mäusen eine erhöhte Apoptoserate in Nieren und Keimzellen sowie eine gestörte Proliferation bzw. Differenzierung im neuronalen und epikardialen Gewebe (Kreidberg et al. 1993; Hohenstein u. Hastie 2006). Erst 2007 untersuchte die Gruppe um Summers die Inzidenz und die klinische Bedeutung von WT1-Mutationen in einer Serie von 70 AML-Patienten mit normalem Karyotyp systematisch. Dabei wurden bei 10% der AML-Patienten WT1-Mutationen identifiziert; hierbei handelte es sich um kurze Insertionen oder Deletionen in Exon 7 und 9, welche zu einer Verschiebung des Leserahmens (sog. Frameshift-Mutationen) führten und mit einem Bruch in der DNABindungsdomäne einhergingen. Auffallend war, dass bei sechs von sieben Patienten mit WT1-Mutation ebenfalls eine FLT3-ITD-Mutation festzustellen war, die per se mit einer schlechten Prognose assoziiert ist. Dabei konnte kein Patient mit dem Genotyp WT1mut/FLT3-ITDpos eine CR erreichen, was zunächst vermuten ließ, dass WT1-Mutationen zu einer noch ungünstigeren Prognose führen und möglicherweise auch eine gewisse Resistenz der AML gegenüber Chemotherapie verursachen könnten (Summers et al. 2007). Basierend auf dieser Studie analysierten im Folgenden zwei weitere Arbeitsgruppen die Bedeutung von WT1Mutationen bei AML-Patienten mit normalem Karyotyp. So führten Paschka und Kollegen eine WT1-Mutationsanalyse an 196 Patienten mit normalem Karyotyp durch, wobei nur Exon 7 und 9 des Gens untersucht wurden. Es konnten bei 21 von 196 Patienten WT1-Mutationen gefunden werden. Bis auf eine Nonsense-Mutation handelte es sich in Exon 7 um FrameshiftMutationen, die hauptsächlich durch Wiederholungen kurzer Sequenzabschnitte verursacht wurden. In Exon 9 kam es dagegen durch Punktmutationen zur Substitution einzelner Aminosäuren im Bereich des dritten Zinkfingers. Des Weiteren zeigte sich eine Assoziation von WT1-Mutationen mit höheren Leukozytenzahlen und mit dem Vorliegen einer FLT3-ITD-Mutation (Paschka et al. 2008). Für die Gruppe von Patienten mit dem Genotyp WT1mut zeigte sich ein schlechteres krankheitsfreies Überleben (DFS, p<0.001) und OS (p<0.001) im 13 Vergleich zu WT1wt- Patienten, während in Bezug auf das Erreichen einer CR kein signifikanter Unterschied ermittelt werden konnte (Paschka et al. 2008). Nahezu zeitgleich veröffentlichte die Arbeitsgruppe um Fitzgibbon ebenfalls eine Studie über eine mögliche prognostische Bedeutung von WT1-Mutationen bei der AML; hier fokusierte die Mutationsanalyse ebenfalls auf die Exons 7 und 9. Es konnten 32 Mutationen in 285 AML-Patienten mit normalem Karyotyp (11%) detektiert werden, wobei wieder hauptsächlich Insertionen oder Deletionen detektiert wurden. Die oben beschriebene Assoziation von WT1-Mutationen mit FLT3-ITD konnte in dieser Studie allerdings nicht gezeigt werden. Patienten mit WT1-Mutationen hatten eine geringere CR-Rate (p=0.02). Für das DFS und OS konnte jedoch kein signifikanter Unterschied im Vergleich zu WT1wt-Patienten nachgewiesen werden (Virappane et al. 2008). Somit ist die prognostische Bedeutung von WT1-Mutationen bei AML-Patienten mit normalem Karyotyp noch nicht abschließend geklärt. Ziel dieser Arbeit war es, eine größere Anzahl jüngerer homogen behandelter AML-Patienten mit normalem Karyotyp auf Mutationen im WT1-Gen zu untersuchen und deren Inzidenz und prognostische Bedeutung zu evaluieren, insbesondere im Kontext mit anderen AML-assoziierten molekularen Veränderungen. 14 2 Material und Methoden 2.1 Geräte- und Reagenzienliste Aqua ad iniectabilia, B. Braun, Melsungen, Deutschland Big Dye® Terminator v3.1 Cycle Sequencing Kit, Applied Biosystems, Foster City, Kalifornien, USA Blue Juice, Invitrogen, Carlsbad, Kalifornien, USA 100-bp-Ladder, Invitrogen, Carlsbad, Kalifornien, USA Desoxynucleoside Triphospahte Set, PCR Garde Roche, Roche Applied Science, Mannheim, Deutschland TM DyeEx 2.0 Spin Kit, Qiagen, Venlo, Niederlande DyeEx 96 Kit, Qiagen, Venlo, Niederlande 200 µl 1%-Ethidium-Bromid-Lösung, Firma Carl Roth, Karlsruhe, Deutschland Fast MicroAmp® Optical 96-Well Reaction Plate, Applied Biosystems, Foster City, Kalifornien, USA Ficoll Seperating Solution, Seromed, Biochrom, Berlin, Deutschland GeneAmp PCR System 2700, Applied Biosystems, Foster City, Kalifornien, USA GeneAmp PCR System 2720, Applied Biosystems, Foster City, Kalifornien, USA Gene ID 7490, http://ncbi.nlm.nih.gov/ 3130/3130xl Genetic Analyser, Applied Biosystems, Foster City, Kalifornien, USA HotStar Taq DNA Polymerase, Qiagen, Venlo, Niederlande 50mM Magnesium-Chlorid, Invitrogen, Carlsbad, Kalifornien, USA 50mM Magnesium-Chlorid, Qiagen, Venlo, Niederlande Multifuge 4KR Heraeus, Firma Carl Roth, Karlsruhe, Deutschland Orange G, Sigma Aldrich, St. Louis, Missouri, USA 10x PCR Buffer, Invitrogen, Carlsbad, Kalifornien, USA 10x PCR Buffer, Qiagen, Venlo, Niederlande Platinum Taq DNA Polymerase, Invitrogen, Carlsbad, Kalifornien, USA Qiaquick PCR-Purification-Kit, Qiagen, Venlo, Niederlande Q-Solution, Qiagen, Venlo, Niederlande RLT Puffer Plus, AllPrep DNA/RNA-Kit- Qiagen, Venlo, Niederlande WT1 Referenzsequenz: NCBI; cDNA NM_0024426; www.ncbi.org 15 Zentrifuge 5415 D, Eppendorf, Hamburg, Deutschland 2.2 Patientenkollektiv Das untersuchte Patientenkollektiv setzte sich aus 617 jüngeren AML-Patienten (18-60 Jahre) mit zytogenetisch normalem Karyotyp zusammen. Diese Patienten waren im Rahmen von drei Multicenter-Studien behandelt worden [HD93-Studie (n=77), HD98A-Studie (n=268), AMLSG 07-04-Studie (n=272)]. 499 Patienten hatten eine de novo AML, 60 Patienten eine sekundäre AML (s-AML) nach einem myelodysplastischen Syndrom und 12 Patienten eine therapieassoziierte AML (tAML). Bei 46 Patienten war die Genese der AML nicht weiter eruierbar. Das einzige Einschlusskriterium bestand in der Verfügbarkeit von Knochenmark und/oder peripherem Blut zur Durchführung der DNA-Analyse. Zusätzlich waren bei 16 Patienten Remissionsmaterial Wangenabstriche vorhanden, und um bei weiteren gegebenenfalls 10 Patienten Keimbahnmutationen identifizieren zu können. Eine Einverständniserklärung gemäß der Deklaration von Helsinki, die sich auf die Behandlung und die Durchführung von genetischen Analysen bezieht, lag bei allen Patienten vor. Bei allen Patienten wurde eine intensive Doppelinduktionstherapie durchgeführt, gefolgt von einer Konsolidierungstherapie. In allen drei oben genannten Studien erfolgte eine Randomisierung für eine allogene Knochenmarktransplantation durch einen passenden Spender. Zusätzlich wurde das WT1-Mutationsscreening auch an einer Kontrollgruppe aus 38 gesunden Probanden durchgeführt. 2.3 Materialgewinnung und –aufbereitung Das Material für die WT1-Analyse wurde entweder aus peripherem Blut und/oder aus Knochenmark gewonnen. Das Beckenkammpunktion aspiriert. 16 Knochenmark wurde mittels Die Gewinnung mononukleärer Zellen erfolgte nach dem Prinzip der Dichtegradientenzentrifugation. Material mit hohen Leukozytenzahlen wurde zunächst im Verhältnis von 1:2 bis 1:3 mit RPMI 1640 Kulturmedium verdünnt. Im nächsten Schritt wurden peripheres Blut und/oder Knochenmark im Verhältnis 1:2 auf ein Ficoll-Medium (Ficoll Separating Solution, Seromed, Biochrom, Berlin, Deutschland) geschichtet und anschließend bei 2800 U/min für 20 Minuten bei Raumtemperatur zentrifugiert. Die mononukleären Zellen, die sich danach zwischen Plasma und Ficollschicht befanden, wurden mit einer sterilen Pipette abgenommen. Nach zweimaligem Waschen mit 50 ml RPMI 1640 Medium (Zentrifugation bei 1200 U/min für 10 Minuten bei Raumtemperatur) wurde die Zellzahl in einer Neubauer-Zählkammer bestimmt. Die erhaltenen mononukleären Zellen wurden bis zum weiteren Gebrauch als Zellpellet mit je 5x10 5 bis 1x107 Zellen bei –80°C aufbewahrt. 2.4 DNA-Extraktion Die DNA-Extraktion wird auf Eis durchgeführt. Die Zentrifugation erfolgt jeweils bei 4 °C und bei 13 000 U/min. Hierzu wird das Zellpellet in 600 µl RLT Puffer Plus (AllPrep DNA/RNA-Kit, Qiagen, Venlo, Niederlande) gelöst. Das Lysat wird daraufhin auf die Säulen aus dem DyeExTM 2.0 Spin Kit gegeben und drei Minuten zentrifugiert, um das Lysat zu homogenisieren. Anschließend wird das Lysat auf die blauen Säulen aus dem AllPrep DNA/RNA-Kit von Qiagen pipettiert und nochmals eine Minute zentrifugiert, wobei in der Säule die DNA gebunden wird. Anschließend werden die Säulen mit 500 µl AW 1-Puffer gewaschen und 15 Sekunden zentrifugiert. Der Überstand wird verworfen. Daraufhin wird die Säule mit 500 µl AW 2-Puffer gewaschen und nochmals zwei Minuten zentrifugiert und der Überstand wiederum verworfen. Danach wird die Säule in einem neuen Eppendorf-Gefäß eine Minute trocken zentrifugiert und diese Säule wiederum auf ein neues Eppendorf-Gefäß gesetzt. Nun werden 100 µl Puffer TE (Tris und EDTA) in die Mitte der Säule pipettiert und für 1-3 Minuten inkubiert. Anschließend wird die Säule eine Minute zentrifugiert, um die DNA aus der Säule zu lösen. Zur Erfolgskontrolle werden 2 µl DNA-Lösung mit 8 µl Aqua ad iniectabilia (B. Braun, 17 Melsungen, Deutschland) und 2 µl Blue Juice (Invitrogen, Carlsbad, Kalifornien, USA) auf ein 1%-Agarose-Gel aufgetragen. Die Elektrophorese wird für 40 Minuten bei 100 V und 400 mA durchgeführt. Außerdem wird die Konzentration der erhaltenen DNA im Photometer bestimmt. Hierzu werden 3 µl DNA mit 67 µl Aqua ad iniectabilia Braun verdünnt. 2.5 Polymerasekettenreaktion 2.5.1 Durchführung der Fast-PCR Für den Nachweis von WT1-Mutationen wurde der gesamte kodierende Bereich in 12 PCR-Reaktionen amplifiziert. Die Primer wurden dabei so gelegt, dass sie immer im Bereich der Introns zu liegen kamen. Dadurch konnte die gesamte kodierende Region einschließlich der Splice-Sites amplifiziert werden. Zur Amplifizierung der einzelnen Polymerasekettenreaktion (PCR) Exons mit der des WT1-Gens gewonnenen wurde DNA-Lösung eine der entsprechenden Patientenprobe durchgeführt. Bei der PCR kommt es durch Denaturierung der DNA bei 95 °C zu einer Aufspaltung des Doppelstrangs. Das Binden der Primer am 3’- bzw. 5’-Ende des entsprechenden Exons wird durch Abkühlen der Probe auf 57 °C erreicht. Danach wird durch die DNA-Polymerase der ausgewählte Genabschnitt amplifiziert. In dieser Phase wird die Temperatur auf 72 °C erhöht um unspezifische Hybridisierungen zu vermeiden. Dieser Vorgang wird in 40 Zyklen wiederholt, bis ausreichend Genkopien im Reagenz vorliegen. Der Reaktionsansatz wurde in eine Fast MicroAmp® Optical 96-Well Reaction Plate (Applied Biosystems, Foster City, Kalifornien, USA) pipettiert. Exon 1 wurde wegen seiner großen Länge und seiner GC-reichen Sequenzen in drei Teilen amplifiziert. Diese werden im Folgenden als Exon 1a, 1b und 1c bezeichnet. Zur Durchführung der PCR wurde das Desoxynucleoside Triphosphate Set von PCR Grade Roche verwendet. Die Primersequenzen setzten sich wie folgt zusammen: 18 Tabelle 2: Sequenzen der Primer für die jeweiligen Exons (WT1: Wilms Tumor 1) WT1- Forward-Primer Reverse-Primer Exon 1a M13-ATCCTGGACTTCCTCTTGCTG CTCAGGCACTGCTCCTCG Exon 1b CTGTGCCCTGCCTGTGAG M13-CCGGCCTACTTACCCTGATTG Exon 1c CTCCTTCATCAAACAGGAGCC M13-GGGAAGCAGCTGGGTAAGAG Exon 2 AAAGTCCTGGAGGCTTGTGG M13-CCTCCTTTGCCTAATTTGCTG Exon 3 AGGCTCAGGATCTCGTGTCTC M13-GTCTCGTGCCTCCAAGACC Exon 4 M13-AACTGTGCAGAGATCAGTGGG AGAGAGCTTTGCCCTTTCTTC Exon 5 GCCAAGTCCAGATCTGATTCC M13-GCTACCCTGATTACCCACGTC Exon 6 M13-ATCATTCCCTCCTGATTGCAG CCCTGATGTTAAAGGAGCCTG Exon 7 CTCCAGTGCTCACTCTCCCTC M13-CCTTAGCAGTGTGAGAGCCTG Exon 8 M13-CTAACAAGCTCCAGCGAAGTG CACATGGCTGACTCTCTCATTC Exon 9 M13-GTGAGGCAGATGCAGACATTG AGCCACGCACTATTCCTTCTC Exon 10 M13-CTTGTGATGACTTCACTCGGG GTTTCCAGAAGCACCGGTATC Primer Für Exon 1 wurden auf Grund seiner GC-reichen Sequenzen die HotStar Taq DNA Polymerase, 10x PCR Buffer, 50mM Magnesium-Chlorid und Q-Solution von Qiagen (Venlo, Niederlande) verwendet. Auf 1 µl DNA-Template wurde der Reaktionsansatz für Exon 1 wie folgt pipettiert: Tabelle 3: Reaktionsansatz für die Polymerasekettenreaktion bei Exon 1a-c (Mg: Magnesium; dNTP: Desosynukleosidtriphosphat) Exon 1a Exon 1b Exon 1c Aqua ad iniectabilia Braun 14,75 µl 14,25 µl 14,75 µl 10x PCR Buffer, Minus Mg 2,5 µl 2,5 µl 2,5 µl Q-Solution 5 µl 5 µl 5 µl 50 mM Magnesium-Chlorid - 0,5 µl - dNTP 0,25 µl 0,25 µl 0,25 µl Forward Primer 1 µl 1 µl 1 µl Reverse Primer 1 µl 1 µl 1 µl Hot Star Taq DNA-Polymerase 0,25 µl 0,25 µl 0,25 µl Für Exon 2 bis 10 wurde die PCR mit der Platinum Taq DNA Polymerase durchgeführt. Polymerase, 10x PCR Buffer und 50mM Magnesium-Chlorid wurden 19 von Invitrogen (Carlsbad, Kalifornien, USA) bezogen. Für 1 µl DNA-Template wurde folgender Reaktionsansatz verwendet: Tabelle 4: Reaktionsansatz für die Polymerasekettenreaktion (PCR) bei Exon 2-10(Mg: Magnesium; dNTP: Desosynukleosidtriphosphat) Aqua ad iniectabilia Braun 19 µl 10X PCR Buffer, Minus Mg 2,5 µl 50 mM Magnesium-Chlorid 0,75 µl dNTP 0,25 µl Forward Primer 1 µl Reverse Primer 1 µl Platinum® Taq DNA-Polymerase 0,25 µl Zusätzlich wurde für jedes Exon der PCR-Ansatz ohne DNA-Template pipettiert und somit als Negativkontrolle mitgeführt. Die PCR-Reaktion erfolgte in einem Thermocycler (GeneAmp PCR System 2720 von Applied Biosystems, Foster City, Kalifornien, USA) in 40 Zyklen. Zunächst lief die Maschine 10 s bei 95 °C. Danach folgten 40 Zyklen nach folgendem Schema: 95 °C für 10 s (Denaturierung) 57 °C für 30 s (Binden der Primer) 72 °C für 30 s (Amplifizierung durch die DNA-Polymerase) Anschließend wurden 72 °C für weitere 7 s beibehalten und letztlich die Proben bis zur Entnahme auf 12 °C abgekühlt. Bis zur Aufreinigung des PCR-Produkts wurden die Proben bei 4 °C gelagert. 2.6 Gelelektrophorese Um den Erfolg der PCR-Reaktion zu überprüfen, wurden 5 µl aus jeder Probe zusammen mit 4 µl Ladepuffer (0.06 g Orange G von Sigma Aldrich, St. Louis Missouri, USA, 30 ml Glycerol, 70 ml destilliertes Wasser) auf ein 2%-Agarose-Gel aufgetragen. Die Negativkontrollen zu den jeweiligen Exons wurden ebenfalls 20 mitgeführt. Als Größenstandard wurde ein 100-bp-Ladder (Invitrogen, Carlsbad, Kalifornien, USA) an erster Stelle aufgetragen. Die Gelelektrophorese erfolgte bei 130 V für 60 min. Im Anschluss wurde das Gel zum Färben für 30 min in EthidiumBromid-Lösung (200 µl 1%-Ethidium-Bromid-Lösung von Firma Roth, Karlsruhe, Deutschland, in 4 l destilliertem Wasser) gelegt. Danach wurden die Banden unter UV-Licht sichtbar gemacht und dokumentiert. Dabei zeigte sich als Beispiel folgendes Gel-Bild: Abbildung 3: PCR Produkte von Exon 2 aufgetrennt mittels Gelelektrophorese. Nummer 2 bis 8 entsprechen Exon 2 bei 7 verschiedenen Patienten; Nummer 1: 100-bp-Ladder als Größenstandard; Nummer 9: Negativkontrolle Bei erfolgreich amplifiziertem PCR-Produkt konnte dieses, je nach Größe des entsprechenden PCR-Produktes, an der entsprechenden Position auf dem Gel detektiert werden und die übrigen 20 µl der Probe wurden weiterverarbeitet. Falls sich auch in einer Negativkontrolle eine Bande zeigte, wurde die PCR für dieses Exon wiederholt, da dies auf eine Verunreinigung des Reaktionsansatzes schließen ließ. 21 2.6.1 Aufreinigung des PCR-Produkts Die Aufreinigung des PCR-Produkts erfolgte mittels des QIAquick PCRPurification-Kits der Firma Qiagen. Die Zentrifugation erfolgte hierbei immer bei 13000 U/min für 1 min (Zentrifuge 5415 D von Eppendorf, Hamburg, Deutschland). Zunächst wurde zum PCR-Produkt der Bindepuffer (Buffer PBI) pipettiert. Die Menge hiervon betrug das Fünffache des Volumens des PCR-Produkts, in diesem Fall also 100 µl. Diese Mischung wurde anschließend in die Säulen (QIAquick Spin Columns) pipettiert und zentrifugiert. Dies ermöglichte das Binden des DNAProdukts in der stationären Phase der Säulen. Danach wurden 750 µl eines Waschpuffers (Buffer PE) zugegeben. Nach erneuter Zentrifugation wurde der Überstand verworfen und die Säulen nochmals zentrifugiert. Hierdurch wurden die überschüssigen Reagenzien der PCR-Reaktion, wie Primer und DNA-Polymerase, aus den Säulen ausgewaschen, während die DNA weiter in der stationären Phase gebunden blieb. Anschließend wurde die Säule auf ein neues Eppendorf-Gefäß gesetzt und darauf 40 µl destilliertes Wasser (Firma Braun, Melsungen, Deutschland) pipettiert. Nach einer weiteren Zentrifugation erhielt man das vollständig aufgereinigte PCR-Produkt, das auf diese Weise aus der stationären Phase gelöst wurde, im Durchfluss. 2.7 Cycle Sequencing Reaction (CSR) 2.7.1 Durchführung der CSR Bei der CSR erfolgt nach Binden des Primers an das PCR-Produkt die Synthese des komplementären DNA-Stranges durch die DNA-Polymerase. Hierfür sind im Reagenz die vier Desoxynukleosidtriphosphate (dNTP) und zusätzlich die 2’,3’Didesoxyribonucleosidtriphosphate (ddNTP) der vier Basen enthalten. Die vier verschiedenen ddNTP sind hierzu jeweils mit einem anderen Fluoreszenzfarbstoff markiert. Wenn die ddNTP bei der Synthese des DNA-Stranges eingebaut werden, kommt es zum Kettenabbruch. Hierdurch erhält man unterschiedlich 22 lange Fragmente des DNA-Stranges, die alle mit einer bestimmten Base enden, die später bei der Desoxyribonucleosidtriphosphate Sequenzierung und die ermittelt wird. Die Didesoxyribonukleosidtriphosphate, sowie auch die Polymerase, sind allesamt im Big Dye (Big Dye® Terminator v3.1 Cycle Sequencing Kit von Applied Biosystems) enthalten. Zusätzlich wird ein 5x Sequencing Buffer (Applied Biosystems) zugegeben, um während der Reaktion den pH-Wert stabil zu halten. Der verwendete M13F-Primer dient als Forward Primer sowie als Reverse Primer und besteht aus folgender Basensequenz: 5´- GTA AAA CGA CGG CCA GT - 3´ Zur Durchführung der CSR wurden 0,5 µl der aufgereinigten PCR-Produkte in die Vertiefungen einer MicroAmp® Optical 96-Well Reaction Plate von Applied Biosystems pipettiert. Daraufhin wurde zu jeder Probe ein Reaktionsansatz hinzugefügt, der sich wie folgt zusammensetzte: Tabelle 5: Reaktionsansatz für die Cycling Sequencing Reaction (CSR) Aqua Braun 10,5 µl Sequencing Buffer 1 µl M13F-Primer 1 µl Big Dye 2 µl Anschließend wurde die CSR-Reaktion in 40 Zyklen in einem Thermocycler (GeneAmp PCR System 2700 von Applied Biosystems, Foster City, Kalifornien, USA) unter folgenden Bedingungen durchgeführt: 96 °C für 2 min 95 °C für 15 s 55 °C für 1 min 60 °C für 3 min 4 °C für 10 min 23 Nach Beenden des letzten Zyklus wurden die Produkte bis zur Entnahme aus der PCR-Maschine auf 4 °C gekühlt. Bis zur Aufreinigung des CSR-Produkts wurden die Proben ebenfalls bei 4 °C und lichtgeschützt gelagert. 2.7.2 Aufreinigung des CSR-Produkts Im Anschluss an die CSR-Reaktion wurde das CSR-Produkt aufgereinigt. Dies wurde, abhängig von der Menge der Proben, auf einer DyeEx 96 Plate oder in DyeExTM 2.0 Spin Columns (Qiagen, Venlo, Niederlande) durchgeführt. Bei der Aufreinigung mit dem DyeExTM 2.0 Spin Kit wurden die Säulen (DyeExTM 2.0 Spin Columns) zunächst gevortext, von unten geöffnet und nach Lockerung des Deckels für 3 min bei 3000 U/min in einer Mikrozentrifuge (Zentrifuge 5415 D Eppendorf) zentrifugiert. Der Überstand wurde verworfen. Anschließend wurde das PCR-Produkt auf die Säulen pipettiert und diese nochmals wie oben angegeben zentrifugiert. Hierbei wurden sämtliche Reagenzien in der stationären Phase gebunden. Im Überstand befand sich das aufgereinigte CSR-Produkt. Bei der Aufreinigung mit dem DyeEx 96 Kit wurde zunächst die Dye Ex 96 Plate bei 2350 U/min für 7 min zentrifugiert (Multifuge 4KR Heraeus, Firma Carl Roth, Karlsruhe, Deutschland). Der Überstand wurde verworfen. Anschließend wurde das CSR-Produkt auf die Platte pipettiert und nochmals wie oben beschrieben zentrifugiert. Anschließen erhielt man in einer Costar-Platte, die zuvor unter die Dye Ex 96 Plate gesetzt wurde, das aufgereinigte CSR-Produkt. Die erhaltenen CSR-Produkte wurden für die nachfolgende Sequenzierung in eine MicroAmp® Optical 96-Well Reaction Plate überführt. 2.8 Sequenzierung und Identifizierung von Mutationen Im Sequenziergerät (3130/3130xl Genetic Analyzer, Applied Biosystems) wurden im CSR-Produkt die fluoreszenzmarkierten ddNTP an den Enden der DNA24 Stränge identifiziert. Durch Ermittlung der Stranglänge konnte die Position der Base innerhalb der Gensequenz bestimmt werden. Nach der Sequenzierung wurde die Gensequenz wie folgt dargestellt: ins1333CGGT Abbildung 4: Darstellung einer Insertion (CGGT) (ins: Insertion) Die Basen werden in dieser Abbildung als Peaks dargestellt, wobei jeder Base eine bestimmte Farbe zugeordnet ist. Zur Identifizierung von Mutationen wird die zu untersuchende Sequenz manuell mit der Originalsequenz verglichen (WT1 Referenzsequenz: NCBI; cDNA NM_0024426). Auf diese Weise können Veränderungen der Sequenz wie Punktmutationen, Insertionen und Deletionen detektiert werden. 2.9 Statistische Auswertung Schwerpunkt der Dissertationsarbeit war der Nachweis der WT1 Genmutation an einer definierten Patientenpopulation mit AML, die im Rahmen der AML HD98B und AMLSG 06-04 Studie behandelt wurde. Es handelte sich um eine rein experimentelle Arbeit. Die Ergebnisse dieser Arbeit waren jedoch Grundlage für die Durchführung der in der Arbeit erwähnten klinischen Korrelationen, die im Rahmen eines größeren Forschungsprojektes analysiert wurden. Durch diese Korrelationen ergaben sich neue, klinisch signifikante Aspekte, die im Ergebnisteil vorgestellt und diskutiert werden. Die statistischen Analysen zur Korrelation der experimentellen Daten mit den klinischen Daten wurden von einem Biostatistiker und dem Leiter der 25 Studienzentrale der Abteilung für Innere Medizin III durchgeführt. Da der Schwerpunkt der Dissertationsarbeit nicht in der Durchführung dieser Korrelationen und der damit verbundenen statistischen Analysen, sondern im Nachweis der krankheitsspezifischen Genmutation lag, erfolgt keine Beschreibung der statistischen Analysen. 26 3 Ergebnisse 3.1 Inzidenz von WT1-Mutationen WT1-Mutationen konnten bei 78 von 617 Patienten (12,6%) identifiziert werden. Die Mutationen traten am häufigsten in Exon 7 (n=60, 76,9%) und 9 (n=13, 16,7%) auf, aber auch in Exon 1 (n=1), 2 (n=3), 3 (n=5) und 8 (n=5) konnten Mutationen gefunden werden. Abbildung 5: Schematische Darstellung des WT1-Gens mit Lokalisation der gefundenen WT1Mutationen bei Patienten mit AML (WT1: Wilms Tumor 1; n: Anzahl) Unter den Mutationen in Exon 7 befanden sich 39 Insertionen und 10 Deletionen, die alle eine Verschiebung des Leserahmens zur Folge hatten. Hierbei betrug die Anzahl der zusätzlichen oder fehlenden Nukleotide zwischen 1 und 28 Basenpaare. Des Weiteren konnten in Exon 7 auch Punktmutationen (n=11) identifiziert werden. Darunter entstand bei 2 Mutationen an Stelle von Serin ein Stopcodon (S312X), was einen vorzeitigen Abbruch der Translation zur Folge hatte. Außerdem befanden sich unter den Punktmutationen noch 3 NonsenseMutationen und 6 Missense-Mutationen. Bei einer Missense-Mutation kodierte das mutierte Codon eine andere Aminosäure, was zu einer veränderten Funktion des Genprodukts führte. Bei einer Nonsense-Mutation dagegen entstand durch die Mutation ein Stop-Codon, wodurch ein vorzeitiger Kettenabbruch erfolgte, woraus ein kompletter Funktionsverlust des Genprodukts resultierte. 27 In Exon 9 waren 11 von 13 Mutationen Punktmutationen, welche in drei Fällen in einem Stopcodon (R390X) resultierten, während die restlichen MissenseMutationen waren. Außerdem wurden in Exon 9 zwei Insertionen detektiert, die eine Verschiebung des Leserahmens zur Folge hatten. Im Weiteren konnte in Exon 1 eine Missense-Punktmutation und in Exon 2 drei Punktmutationen, darunter zwei Stopcodons und eine Missense-Mutation, festgestellt werden. In Exon 3 fanden sich eine Deletion, drei Insertionen und eine Punktmutation, die in einem Stopcodon (Y220X) resultierte. In Exon 8 wurden vier Punktmutationen identifiziert, von welchen eine ein Stopcodon zur Folge hatte. Die Übrigen stellten Missense-Mutationen dar. Außerdem konnte auch in Exon 8 eine Insertion detektiert werden. Bei 72 Patienten lagen heterozygote und bei sechs Patienten homozygote Mutationen vor. Bei insgesamt drei Patienten konnten jeweils zwei Mutationen im WT1-Gen identifiziert werden. In zwei Fällen waren diese Mutationen in Exon 3 und Exon 7 lokalisiert. Der dritte Patient hatte Mutationen in Exon 7 und Exon 9. Eine Übersicht über die identifizierten Mutationen zeigt Tabelle 6: Tabelle 6: Auflistung aller identifizierten WT1-Mutationen (WT1: Wilms Tumor 1; rm: Remissionsmaterial; bs: buccal swab; bp: Basenpaare; ins: Insertion; del: Deletion); in den Versuchen wurde vorwiegend Knochenmark verwendet, nur wenn dieses nicht vorlag wurden die Versuche mit peripheren Blut durchgeführt, wobei hier auf eine ausreichende Blastenzahl geachtet wurde. Exon WT1-Mutation Analyse auf Keimbahnmutationen 1 P13T 2 P181S (homozygot) 2 S187X (homozygot) 2 S187X (homozygot) 3 973ins19bp 3 Y220X (homozygot) 3 1058del1bp 3; 7 988ins1bp;R300Q 3; 7 982ins2bp;1304ins5bp 7 1331ins8bp 7 R300Q Wildtyp (rm) Wildtyp (bs) Wildtyp (bs) 28 7 1305ins1bp (homozygot) Wildtyp (bs) 7 R300R 7 1329ins8bp Wildtyp (rm) 7 1334ins1bp Wildtyp (rm) 7 1332ins2bp Wildtyp (bs) 7 1334ins1bp 7 1323ins11bp 7 1337ins8bp 7 R300R 7 1333ins4bp 7 1335del1bp 7 1334ins4bp 7 1327del5bp 7 1333ins5bp 7 S312X;1321ins4bp 7 1325ins5bp 7 S312P 7 1333ins4bp 7 1340ins4bp;1340ins12bp 7 1315ins1bp 7 S312X;1332ins17bp;1332ins3bp 7 1319del1bp 7 1304del1bp 7 1335ins7bp 7 1340del1bp 7 1303del28bp 7 1310del7bp 7 1333ins4bp 7 1328ins7bp 7 1300ins8bp 7 1334ins1bp 7 R311R 7 R300Q 7 1363del1bp 7 1310ins1bp 7 1300ins7bp 7 1334ins1bp 7 1326ins10bp 7 1305ins1bp Wildtyp (bs) Wildtyp (bs) Wildtyp (rm) Wildtyp (rm) Wildtyp (bs) Wildtyp (rm) 29 7 1338del2bp 7 S312R;R300P;1338ins5bp Wildtyp (rm) 7 1303ins1bp Wildtyp (rm) 7 1333ins4bp 7 1333ins1bp 7 1344ins2bp 7 1338ins4bp 7 1320del14bp (homozygot) 7; 9 Wildtyp (bs) 1343ins12bp;R394P Wildtyp (bs) 7 1333ins1bp 7 1334ins4bp 8 R365H 8 1499ins1bp 8 R365H 8 H506Q Wildtyp (rm) 8 R353X Wildtyp (bs) 9 S393P 9 S393P 9 R390X Wildtyp (bs) 9 1572ins1bp Wildtyp (bs) 9 1586ins1bp Wildtyp (bs) 9 D396N 9 H397R 9 R390X 9 R390X Wildtyp (bs) 9 D396H Wildtyp (bs) 9 R394W 9 D396H Wildtyp (rm) Wildtyp (bs) Bei den 38 gesunden Probanden, die als der Kontrollgruppe dienten, konnten keine WT1-Mutationen identifiziert werden. Außerdem waren von 26 WT1mutierten Patienten, die sich in kompletter Remission befanden, Wangenabstriche, peripheres Blut oder Knochenmark vorhanden. Keiner von diesen wies eine Keimbahnmutation des WT1-Gens auf. 30 3.2 Assoziation mit anderen molekularen Markern In der untersuchten Patientengruppe war für 612 Patienten die Information zum FLT3-ITD-Mutationsstatus und für 552 Patienten die Information zum CEBPAMutationsstatus vorhanden. Unter den Patienten mit WT1-Mutation waren 41 von 78 (53%) zusätzlich FLT3-ITDpos, während in der Gruppe ohne WT1-Mutation 171 von 534 (32%) Patienten mit FLT3-ITDpos waren. In 17 von 72 (24%) Patienten mit WT1-Mutation fand sich eine Mutation im CEBPA-Gen, während 51 von 480 (11%) Patienten mit WT1wt eine CEBPA-Mutation aufwiesen. WT1-Mutationen waren folglich signifikant mit FLT3-ITD-Mutationen (p<0.001) und CEBPAMutationen (p=0,004) assoziiert. Bei 24 von 75 (32%) der Patienten mit WT1-Mutation fand sich eine zusätzliche Mutation im NPM1-Gen. Bei Patienten ohne WT1-Mutation fand sich dagegen in 286 von 523 (55%) Fällen eine NPM1-Mutation (p=0.0003). Folglich lag hier eine inverse Korrelation von WT1-Mutationen mit NPM1-Mutationen vor. Bei der Untersuchung der Assoziation mit MLL-PTD (p=0.64) und FLT3-TKDMutationen (p=0.66) zeigte sich keine signifikante Assoziation mit WT1Mutationen. Abbildung 6 auf der folgenden Seite zeigt graphisch, mit welcher Häufigkeit die verschiedenen Mutationen gemeinsam mit WT1-Mutationen auftraten: 31 WT1 NPM1 Hypothetische Klasse IIMutationen, die die Differenzierung verhindern CEBPA Klasse I-Mutationen, die die Proliferation fördern MLL-PTD FLT3-ITD 32% 24% 5% 53% FLT3-TKD 8% NRAS 11% Abbildung 6: Darstellung der Häufigkeit von Mutationen, die gemeinsam mit WT1-Mutationen aufgetreten sind. Dunkelgrau dargestellt sind hypothetische Klasse II-Mutationen, die die Abbildung 6: Darstellung derhellgrau Häufigkeit von Mutationen, die gemeinsam Mutationen Differenzierung verhindern; entspricht Klasse I-Mutationen, diemit dieWT1 Proliferation fördern. aufgetreten (WT1: Wilms sind. Tumor Dunkelgrau 1-Gen; dargestellt NPM1: Nucleophosmin sind hypothetische 1-Gen; CEBPA: CCAAT/enhancer binding protein alpha-Gen; MLL: Myeloid lymphoid leukemia-Gen; FLT3: FMS-like Tyrosinkinas 3-Gen; NRAS: Neuroblastoma rat sarcoma-Gen; PTD: partielle Tandemduplikation; ITD: interne Tandemduplikation; TKD: Tyrosinkinasedomäne) (Gaidzik et al. 2009) 3.3 Assoziation von WT1-Mutationen mit klinischen Charakteristika In Bezug auf die klinischen Charakteristika zeigte sich eine signifikante Assoziation von WT1-Mutationen mit jüngerem Alter (p=0.007), erhöhten Werten der Laktatserumdehydrogenase (LDH) (p=0.007) und einem höheren Blastenanteil im peripheren Blut (p=0.01). Hierbei waren erhöhte Werte von LDH und Blutblasten auch signifikant mit dem Genotyp WT1mut/FLT3-ITDpos assoziiert. So betrugen bei Patienten mit WT1mut/FLT3-ITDpos die LDH durchschnittlich 755,5 U/l und der Blastenanteil durchschnittlich 71%. Danach folgten Patienten die entweder eine FLT3-ITD-Mutation (LDH=559,5 U/I; Blastenanteil=55%) oder eine WT1-Mutation (LDH=422 U/I; Blastenanteil=35%) aufwiesen. Die niedrigsten Werte konnten bei Patienten gemessen werden, die weder FLT3-ITDpos noch WT1mut waren. Hier ergaben sich als Mittelwerte der LDH 362 U/l und des Blastenanteils 27%. Die klinischen Parameter in Abhängigkeit vom WT1- und FLT3-ITD-Mutationsstatus sind in Tabelle 7 dargestellt: 32 Tabelle 7: Absolute Häufigkeiten bzw. Median und Spannweite der untersuchten klinischen Parameter einschließlich p-Werte in Bezug auf den WT1- und FLT3-ITD- Mutationsstatus (WT Wilms Tumor 1-Gen; FLT3: FMS-like Tyrosinkinase-Gen; ITD: interne Tandemduplikation; wt: Wildtyp; mut: mutiert; s-AML: sekundäre AML; t-AML: therapieassoziierte AML a: Jahre; WBC: white blood cells; PB: peripheres Blut; KM: Knochenmark; LDH: Laktatdehydrogenase) wt WT1 FLT3-ITD WT1 neg mut FLT3-ITD WT1 neg wt FLT3-ITD WT1 pos mut FLT3-ITD pos Geschlecht P 0,05 Weiblich 178 (49,0%) 23 (62,2%) 104 (60,8%) 22 (53,7%) Männlich 185 (51,0%) 14 (37,8%) 67 (39,2%) 19 (46,3%) AML-Typ 0,35 De novo 288 (79,3%) 29 (78,4%) 146 (85,4%) 33 (80,5%) s-AML 43 (11,8%) 3 (8,1%) 10 (5,8%) 2 (4,9%) t-AML 9 (2,5%) 0 (0%) 3 (1,8%) 0 (0%) Unbekannt 23 (6,3%) 5 (13,5%) 12 (7,0%) 6 (14,6%) 49,4 41,9 47,2 46,4 16-60,9 23-59,8 18,3-60,9 19,4-58,8 13,5 13,9 39,2 30,1 0,2-369 1,3-108 0,2-345 1,1-220 27 35 55 71 0-99 0-98 0-100 1-96 70 72 87 88 0-100 7-96 2-100 20-100 362 422 559,5 755,5 89-2371 131-4566 122-4091 184-2992 Alter in a Median Spannweite 0,007 WBC-Anzahl 9 in 10 /l Median Spannweite 0,22 PB-Blasten in % Median Spannweite 0,01 KM-Blasten in % Median Spannweite 0,14 LDH in U/l Median Spannweite 33 0,007 3.4 Prognostische Bedeutung von WT1-Mutationen für das Ansprechen auf Induktionstherapie In der univariaten Analyse konnte in Bezug auf das Erreichen einer kompletten Remission (CR), eine therapierefraktäre Erkrankung und frühzeitigen Tod kein Unterschied zwischen Patienten mit und ohne WT1-Mutation festgestellt werden. Da bei Patienten mit dem Genotyp WT1mut/FLT3-ITDpos die höchsten LDH-Werte und der höchste Blastengehalt vorlagen, scheint hier die Zellproliferation am stärksten ausgeprägt zu sein. Daher wurde für diese Subgruppe eine weitere Analyse durchgeführt. Bei Patienten mit dem Genotyp WT1mut/FLT3-ITDpos (n=40) war die CR-Rate signifikant niedriger (63%) als bei Patienten mit WT1mut/FLT3ITDneg (n=37) (92%; p=0.003). Des Weiteren hatte der Genotyp WT1mut/FLT3ITDpos auch ein signifikant höheres Rezidivrisiko zur Folge (33% gegenüber 5%; p=0.003). Auf Grund dieser Daten wurde im Anschluss eine multivariate Analyse mit den Variablen FLT3-ITD-Mutation und WT1-Mutation durchgeführt. Hierbei zeigte sich eine signifikante Assoziation für hohe Leukozytenzahlen (Odds Ratio [OR]=0,63; p=0,009) und dem Genotyp WT1mut/FLT3-ITDpos (OR=0,19; p=0,03) mit dem Versagen auf Induktionstherapie. Weitere signifikante Variablen waren CEBPAMutationen (OR=2,67; p=0.02) und NPM1-Mutationen (OR=2,13; p=0.001), die signifikant mit gutem Ansprechen auf die Induktionstherapie assoziiert waren. 3.5 Prognostische Bedeutung von WT1-Mutationen für das Überleben Für die vorliegende Analyse umfasste das durchschnittliche Follow-up einen Zeitraum von 44 Monaten. Hierbei zeigten sich in Bezug auf das RFS (p=0.40) und OS (p=0.62) in der univariaten Analyse, wie in Abbildung 7 dargestellt, keine Unterschiede zwischen WT1mut und WT1wt. Gleiche Ergebnisse erhielt man, wenn nur Exon 7 und 9 oder nur Fälle von de novo AML in die Analyse eingeschlossen wurden. Betrachtete man nur diejenigen Patienten, die entweder mehrere Zyklen Hochdosis-Chemotherapie oder eine autologe Stammzelltransplantation erhalten hatten, konnten ebenfalls keine Unterschiede hinsichtlich des RFS (p=0.23) und OS (p=0.46) festgestellt werden. 34 Abbildung 7: (A) Darstellung von rezidivfreiem Überleben (Relapse-free Survival) und (B) Gesamtüberleben (Overall Survival) bei Patienten mit WT1 mut (rot) und WT1 wt (schwarz) (WT1: Wilms Tumor 1-Gen; wt: Wildtyp; mut: mutiert; n: Anzahl; Gaidzik et al. 2009) Wenn in die Analyse allerdings das gleichzeitige Vorliegen einer FLT3-ITD Mutation miteinbezogen wurde, hatten Patienten mit dem Genotyp WT1mut/FLT3ITDpos im Vergleich zu Patienten mit dem Genotyp WT1mut/FLT3-ITDneg ein signifikant schlechteres RFS (p=0.006) und OS (p<0.0001): B A WT1 mutierte Patienten 100 P=0.006 75 FLT3-ITDneg n=24 50 25 P<0.0001 75 Overall Survival(%) Relapse-free Survival(%) 100 WT1 mutierte Patienten FLT3-ITDneg n=29 50 25 FLT3-ITDpos n=27 FLT3-ITDpos n=15 0 0 0 1 2 3 4 5 6 7 Time (Months) 8 9 0 10 1 2 3 4 5 6 7 Time (Months) 8 9 10 Abbildung 8: (A) Darstellung von rezidivfreiem Überleben (Relapse-free Survival) und (B) Gesamtüberleben (Overall Survival) bei WT1-mutierten Vorhandenseins einer FLT3-ITD Mutation [FLT3-ITD pos Patienten in (rot) und FLT3-ITD Abhängigkeit des neg (schwarz)] (WT1: Wilms Tumor 1-Gen; FLT3: FMS-like tyrosinkinase 3- Gen; ITD: interne Tandemduplikation; neg: negativ; pos: positiv; n: Anzahl: Gaidzik et al. 2009) 35 In der multivariaten Analyse waren die Genotypen NPM1mut/FLT3-ITDneg (HR=0,51 und 0,39), CEBPAmut (Hazard Ratio [HR]=0,51 und 0,39), MLL-PTDpos (HR=1,57 für RFS), das Alter (HR=1,2 und 1,3 bei einem Altersunterschied von zehn Jahren) und eine erhöhte Leukozytenzahl (HR=1,55 und 1,58) signifikante Variablen für die Endprodukte RFS und OS. Wenn man WT1 Mutationen für sich betrachtet konnte hier kein signifikanter Effekt nachgewiesen werden. Der Genotyp WT1mut/FLT3-ITDpos zeigte dagegen im Vergleich zu WT1mut/FLT3-ITDneg einen höheren Blastenanteil im peripheren Blut (71% vs. 35%), einen höheren LDH-Wert (755,5 U/l vs. 422 U/l) sowie oben beschriebene Unterschiede in RFS und OS. 36 4 Diskussion 4.1 Häufigkeit von WT1-Mutationen In unserer Patientenkohorte traten bei 78 von 617 (12,6%) Patienten WT1Mutationen auf, während Paschka et al. und Virappane eine etwas niedrigere Inzidenz an WT1-Mutationen von 10,7% (Paschka et al. 2008) bzw. 10% (Virappane et al. 2008) beschrieben. Eine mögliche Ursache für diese Unterschiede besteht darin, dass in unserer Studie alle Exons des WT1-Gens untersucht und 14 Mutationen in den Exons 1, 2, 3 und 8 identifiziert wurden. In den anderen Studien hingegen wurden die Mutationsanalysen nur in den Exons 7 und 9 durchgeführt (Paschka et al. 2008; Virappane et al. 2008). 4.2 Lokalisation der Mutationen und Mutationstyp 76,9% der WT1-Mutationen waren in unserer Studie Frameshift-Mutationen in Exon 7. Diese Mutationen führen zu einem verkürzten Protein und zum Verlust aller vier Zinkfinger, da Exon 7 den ersten Zinkfinger des WT1-Proteins kodiert. Dadurch sind sämtliche Funktionen der Zinkfinger betroffen, wie z.B. das Signal zum Transport in den Zellkern und die Bindungsdomänen zur Interaktion mit anderen Proteinen. Am zweithäufigsten mit 16,7% befanden sich WT1-Mutationen in Exon 9, wovon die Mehrzahl Punktmutationen waren, besonders häufig in Codon D396 und H397. Man nimmt an, dass diese Mutationen die DNA-Bindung und die Stabilität der Helix des dritten Zinkfingers beeinträchtigen. Außerdem befanden sich unter den Punktmutationen auch Missense-Mutationen an R390X in Exon 9, die bereits als Keimbahnmutation bei Wilms’ Tumor-Patienten beschrieben wurden (Little et al. 2004). Nur bei zwei Patienten konnten wir Frameshift-Mutationen in Exon 9 nachweisen. Auf Grund der Lokalisation der Mutation ist davon auszugehen, dass bei dieser Mutation nur der dritte und vierte Zinkfinger betroffen sind. 37 Darüber hinaus fanden wir Mutationen in den Exons 1 (n=1), 2 (n=3), 3 (n=5) und 8 (n=5). Dabei handelte es sich in Exon 2, 3 und 8 um Frameshift- und Punktmutationen. Die Frameshift-Mutationen in Exon 2 und 3 führen zu einem verkürzten Protein, wobei diesem die Transrepressions- und die Transaktivierungsdomäne sowie alle vier Zinkfinger fehlen. Bei den FrameshiftMutationen in Exon 8 entsteht ebenfalls ein verkürztes Protein ohne den zweiten Zinkfinger. Als Folge von Mutationen in Exon 1, die bereits beschrieben wurden (King-Underwood et al. 1996), fehlt der Teil des Proteins, der durch Exon 1 kodiert wird. Es ist bislang nicht bekannt, welche unterschiedlichen Einflüsse diese Mutationen auf die biologische Funktion des WT1-Proteins haben, und wie sie sich auf die Prognose auswirken. Interessant ist, dass sich bei der AML die Mutationen vor allem in Exon 7 und 9 häufen, während sich beim WAGR, DDS und FrasierSyndrom Mutationen im Bereich des zweiten und dritten Zinkfingers, also auf Exon 8 oder 9, finden (Yang et al. 2007). Außerdem bestehen die Mutationen beim Wilms’ Tumor hauptsächlich aus großen Deletionen und Punktmutationen. Bei der AML wurden dagegen hauptsächlich Insertionen identifiziert. Diese unterschiedlichen Mutationstypen und unterschiedlichen Lokalisationen der Mutationen bei verschiedenen Krankheiten weisen darauf hin, dass der jeweiligen Krankheitsentität unterschiedliche Pathomechanismen zu Grunde liegen. Bei AML-Patienten haben die identifizierten Mutationen ein trunkiertes WT1-Protein zur Folge, bei dem in den meisten Fällen die Zinkfingerregion, welche von entscheidender funktioneller Bedeutung ist, komplett zerstört ist oder sogar vollständig fehlt. 4.3 Assoziation von WT1-Mutationen mit klinischen Charakteristika und molekularen Markern Auch bei den klinischen Charakteristika zeigten sich Unterschiede unserer Studie im Vergleich zur CALGB- (Paschka et al. 2008) und zur MRC-Studie (Virappane et al. 2008). So waren in unserer Studie die Patienten mit WT1-Mutation mit einem medianen Alter von 41,9 Jahren im Durchschnitt jünger als Patienten ohne WT138 Mutation (medianes Alter 49,4 Jahre). Außerdem zeigten sich höhere LDH-Werte und höhere periphere Blastenzahlen, was auf eine höhere proliferative Aktivität der WT1-mutierten Leukämien hindeutet. Dagegen konnte in der CALGB-Studie lediglich eine Assoziation mit hohen Leukozytenzahlen gezeigt werden (Paschka et al. 2008), während in der MRC–Studie kein Zusammenhang von WT1Mutationen mit der proliferativen Aktivität vorlag (Virappane et al. 2008). Bei der Untersuchung einer möglichen Assoziation von WT1-Mutationen mit anderen AML-assoziierten molekularen Markern fanden Summers et al. eine absolute Inzidenz von 6 FLT3-ITD-Mutationen bei 7 WT1-mutierten Patienten. Paschka et al. untersuchten 196 AML-Patienten auf WT1-Mutationen. Diese waren bei 21 Patienten (11%) nachweisbar. Eine Koinzidenz mit FLT3-ITD lag in 12 Fällen (57%) vor (Paschka et al. 2008). Auch Virappane et al. fanden eine Koinzidenz von WT1-Mutation und FLT3-ITD. Hier lag bei WT1-mutierten Patienten in 23 von 47 Fällen (49%) eine FLT3-ITD-Mutation vor (Virappane et al. 2008). Diese positive Korrelation von WT1- und FLT3-ITD-Mutation konnte in unserer Arbeit bestätigt werden. Die von uns gefundene Inzidenz von FLT3-ITDMutationen bei Patienten mit WT1-Mutation lag bei 48%. Die prognostische Bedeutung dieser Koinzidenz wird im nächsten Abschnitt erläutert. Des Weiteren konnten wir einen Zusammenhang von WT1-Mutationen mit CEBPA-Mutationen feststellen. So lag bei 27% der WT1-mutierten Patienten eine CEBPA-Mutation vor, während die Gesamtinzidenz von CEBPA-Mutationen nur bei 13% lag. Bezüglich NPM1 zeigte sich, wie oben bereits erwähnt eine inverse Korrelation, so dass WT1-mutierte Patienten seltener eine NPM1-Mutation (32%) trugen als Patienten ohne WT1-Mutation (55%). 4.4 Prognostische Bedeutung von WT1-Mutationen Beide Studien von Virappane und Paschka beschreiben eine Assoziation von WT1-Mutationen mit einer schlechten Prognose. Dabei erreichten in der MRCStudie signifikant weniger Patienten eine CR, bedingt durch einen höheren Anteil an refraktären Leukämien. Darüber hinaus waren auch die beiden Endpunkte RFS und das OS für Patienten mit dem Genotyp WT1mut signifikant schlechter. Hier 39 zeigte sich für den Genotyp WT1mut eine 5-Jahres-Überlebensrate von 26% gegenüber 47% für WT1wt. In der multivariaten Analyse war WT1mut ein unabhängiger ungünstiger prognostischer Faktor für RFS sowie OS (Virappane et al. 2008). In der CALGB-Studie konnte zwar kein Effekt von WT1 auf die CR-Rate nachgewiesen werden. Allerdings war auch hier das Vorliegen einer WT1Mutation mit einem signifikant schlechteren RFS und OS assoziiert. Denn während sich die 3-Jahres-Überlebensrate für den Genotyp WT1wt auf 56% belief, betrug diese bei vorliegender WT1-Mutation nur 10%. Ebenso war in der multivariaten Analyse die WT1-Mutation ein unabhängiger Faktor für eine ungünstige Prognose sowohl für das RFS als auch für das OS (Paschka et al. 2008). In unserer Studie konnten wir allerdings keinen signifikanten Einfluss von WT1Mutationen auf die CR-Rate, das RFS und das OS nachweisen. Diese Unterschiede sind sehr wahrscheinlich auf Unterschiede in der Therapie der Patienten zurückzuführen. So wurden die Patienten unserer Studie in der Konsolidierungsphase mit höheren Dosen Cytarabin behandelt. Die kumulative Dosis betrug hierbei 18-54 g/m2, wobei die meisten Patienten über 36 g/m2 erhielten. Dagegen beinhaltete die Therapie der Patienten aus der MRC- und CALGB-Studie relativ niedrig dosiertes Cytarabin. So wurden laut Protokoll in den Therapiestudien MRC 10 und MRC 12 etwa 6 g/m² bzw. 1-8 g/m² appliziert (Virappane et al. 2008). Auch in der CALGB-Studie wurde in den Therapieprotokollen 9621 und 19808 eine kumulative Dosis von 13-25 g/m² angegeben (Paschka et al.2008). Daher wäre es möglich, dass der beschriebene negative Effekt der WT1-Mutation durch die intensivere Cytarabin-Therapie überwunden werden kann und deshalb in unserer Studie nicht zum Tragen kommt. Bei Summers et al. war aufgefallen, dass der Genotyp WT1mut/FLT3-ITDpos durch Versagen der Induktionstherapie gekennzeichnet war. Keiner der 5 Patienten mit kurativem Therapieansatz erreichte eine komplette Remission (Summers et al. 2007). Des Weiteren zeigten Paschka et al. ebenfalls einen negativ prognostischen Effekt. Hier zeigte sich ein RFS sowie OS von 8% (1 von 12 Patienten) (Paschka et al. 2008). Auch wir sahen eine signifikante Assoziation von WT1-Mutationen mit FLT3-ITD-Mutationen sowie einen additiven Effekt des 40 Genotyps WT1mut/FLT3-ITDpos hinsichtlich der proliferativen Marker. Aus diesem Grund führten wir eine Subgruppenanalyse durch, bei der zusätzlich zu WT1 der FLT3-ITD-Status berücksichtigt wurde. Dabei wies der Genotyp WT1mut/FLT3ITDpos die höchsten LDH-Werte und die höchsten Blastenzahlen im peripheren Blut auf, so dass man in diesen Fällen von einer sehr hohen proliferativen Aktivität der AML und einem möglichen additiven Effekt dieser beiden Mutationen ausgehen kann. 4.5 Schlussfolgerung Zusammenfassend konnten in dieser Arbeit WT1-Mutationen mit einer Inzidenz von 12,6% bei AML-Patienten mit normalem Karyotyp nachgewiesen werden. Die Mehrzahl der Mutationen war in funktionell relevanten Domänen lokalisiert, weshalb eine funktionelle Relevanz der beschriebenen Mutationen sehr wahrscheinlich ist. Die genauen Pathomechanismen, wie WT1-Mutationen zur Entstehung der AML beitragen, sind bislang noch unklar. Die prognostische Bedeutung von WT1-Mutationen wurde in mindestens 3 größeren Studien untersucht, wobei WT1-Mutationen sowohl in der CALGB- als auch in der MRCStudie mit einem schlechten klinischen Verlauf und einer schlechten Prognose assoziiert waren. In unserer Studie untersuchten wir eine große homogene Patientenkohorte auf WT1-Mutationen und konnten eine vergleichbare Inzidenz zeigen. Allerdings konnten wir keinen negativen Einfluss auf die Prognose durch WT1-Mutationen bei jüngeren AML-Patienten mit normalem Karyotyp feststellen. Eine mögliche Ursache liegt möglicherweise in der unterschiedlichen Therapieintensität, die in diesen Studien verabreicht wurde. Während in den Studien der MRC und CALGB eine relativ niedrige Cytosin-Arabinosid-Dosis verabreicht wurde, erhielten die Patienten in unserer Studie sehr hohe Dosen Cytosin-Arabinosid. In Zusammenschau mit unseren Ergebnissen könnte der negativ-prognostische Effekt von WT1-Mutationen durch die hohe CytosinArabinosid-Dosierung aufgehoben werden. Um dies zu prüfen, sind weitere vergleichende Studien notwendig. 41 Weiterhin konnten wir beobachten, dass die Proliferationsmarker LDH und Blastenzahl im peripheren Blut bei Patienten mit WT1-Mutation erhöht waren. Diese Werte lagen allerdings noch höher vor, wenn WT1-Mutationen gemeinsam mit FLT3-ITD-Mutationen auftraten. Somit könnte es sich hier um einen synergetischen Effekt von WT1- und FLT3-ITD-Mutation handeln. Dieser Effekt konnte auch klinisch in der Subgruppenanalyse nachgewiesen werden, da Patienten mit diesem kombinierten Genotyp ein signifikant schlechteres RFS und OS aufwiesen. 42 5 Zusammenfassung AML-Patienten mit normalem Karyotyp, welche ca. 40-50% aller AML-Patienten ausmachen, stellen biologisch und klinisch eine äußerst heterogene Gruppe dar. Insbesondere die Identifizierung neuer molekularer Marker, wie beispielsweise NPM1 (Nucleophosmin 1), CEBPA (CCAAT/enhancer binding protein alpha) und FLT3 (FMS-like-Tyrosinkinase 3), führte nicht nur zu einer weiteren Charakterisierung dieser zytogenetischen AML Subgruppe, sondern es konnte auch gezeigt werden, dass diese Marker eine prognostische Bedeutung haben. So gehen NPM1- und CEBPA-Mutationen mit einer günstigen Prognose einher, während eine FLT3-ITD-Mutation (ITD: interne Tandemduplikation) eine eher ungünstige Prognose aufweist. Ein weiterer, neuer molekularer Marker ist das Wilms’ Tumor 1 (WT1)-Gen, das auf Chromosom 11 lokalisiert und aus 10 Exons besteht. Das WT1-Protein fungiert als Transkriptionsfaktor, der besonders bei der Entwicklung des Urogenitaltrakts von Bedeutung ist. Allerdings spielt das WT1Gen auch in der Onkogenese eine wichtige Rolle. So wurde es zunächst beim Wilms’ Tumor der kindlichen Niere entdeckt; ca. 10 % der kindlichen Nierentumoren weisen eine Mutation im WT1-Gen auf. In den letzten Jahren konnten in kleineren Studien auch WT1- Mutationen bei AML-Patienten identifiziert werden, deren prognostische Bedeutung noch nicht abschließend geklärt ist. Daher war Ziel dieser Studie, die Inzidenz und prognostische Bedeutung von WT1-Mutationen in einer großen Kohorte (n=617) homogen behandelter, jüngerer AML-Patienten zu untersuchen. Die Patienten waren im Rahmen von drei prospektiven Therapiestudien der AML Study Group (AMLSG), HD93-Studie, HD98A-Studie, AMLSG 07-04-Studie, behandelt worden. Die Mutationsanalyse erfolgte mittels Polymerasekettenreaktion für alle kodierenden Exons (1-10) und anschließender direkter Sequenzierung. Dabei konnten wir bei 78 von 617 Patienten WT1-Mutationen identifizieren, welche besonders häufig in Exon 7 und 9 lokalisierten, aber auch in den anderen Exons vorkamen. WT1-Mutationen waren signifikant häufig mit FLT3-ITD- und CEBPAMutationen assoziiert, während sich eine signifikant negative Korrelation mit NPM1-Mutationen zeigte. Hinsichtlich der klinischen Charakteristika wiesen Patienten mit WT1-Mutation signifikant 43 erhöhte LDH-Werte (Laktatdehydrogenase) und einen erhöhten Gehalt an Blasten im peripheren Blut auf und waren signifikant jünger als Patienten ohne WT1-Mutation. In Bezug auf das Ansprechen auf die Induktionstherapie konnte kein Unterschied zwischen Patienten mit und ohne WT1-Mutation festgestellt werden. Auch in der Überlebenszeitanalyse zeigten sich in der univariaten Analyse keine Unterschiede zwischen Patienten mit und ohne WT1-Mutation. Allerdings zeigte sich bei Patienten mit dem Genotyp WT1mut/FLT3-ITDpos eine signifikant niedrigere Rate an kompletten Remissionen sowie ein schlechteres rezidivfreies und Gesamtüberleben. Die von uns erhobenen Daten sind diskrepant zu den WT1-Mutationsstudien des Medical Research Council (MRC) und der Cancer and Leukemia Study Group B (CALBG), welche WT1 als ungünstigen prognostischen Faktor identifizierten. Durch eine detaillierte vergleichende Analyse konnte eine mögliche Ursache für diese klinischen Unterschiede herausgearbeitet werden: Im Gegensatz zu den Studien der MRC und der CALGB erhielten die Patientenstudien der AMLSG eine signifikant höhere Dosis Cytosin-Arabinosid basierter Chemotherapie, welche den negativen Effekt einer WT1- Mutation möglicherweise aufheben kann. Abschließend lässt sich sagen, dass die prognostische Bedeutung einer WT1Mutation noch nicht geklärt ist. Die in den unterschiedlichen Studien generierten Daten legen nahe, dass möglicherweise die verabreichte Cytosin-ArabinosidDosis hier eine Rolle spielen könnte. Dies muss allerdings in weiteren vergleichenden Analysen mit anderen Studien geprüft werden. Unsere, aber auch Daten anderer Studiengruppen legen nahe, dass der Genotyp WT1mut/FLT3-ITDpos mit einem prognostisch ungünstigen klinischen Verlauf assoziiert zu sein scheint. Die Durchführung von Meta-Analysen könnte hier hilfreich sein, um diese Ergebnisse zu validieren und die prognostische Bedeutung von WT1-Mutationen per se oder auch in Kombination zu evaluieren. 44 6 Literaturverzeichnis 1. Caligiuri MA, Strout MP, Lawrence D, Arthur DC, Baer MR, Yu F, Knuutila S, Mrózek K, Oberkircher AR, Marcucci G, de la Chapelle A, Elonen E, Block AW, Rao PN, Herzig GP, Powell BL, Ruutu T, Schiffer CA, Bloomfield CD: Rearrangement of ALL1 (MLL) in Acute Myeloid Leukemia with Normal Cytogenetics. Cancer Res 58: 55-59 (1998) 2. Call KM, Glaser T, Ito CY, Buckler AJ, Pelletier J, Haber DA, Rose EA, Kral A, Yeger H, Lewis WH, Jones C, Housman DE: Isolation and Characterization of a Zinc Finger Polypeptide Gene at the Human Chromosome 11 Wilms’ Tumor Locus. Cell 60: 509-520 (1990) 3. Döhner K, Döhner H: Molecular characterization of acute myeloid leukaemia. Haematologica 93: 976-982 (2008) 4. Döhner K, Schlenk RF, Habdank M, Scholl C, Rücker FG, Corbacioglu A, Bullinger L, Fröhling S, Döhner H: Mutant nucleophosmin (NPM1) predicts favorable prognosis in younger adults with acute myeloid leukemia and normal cytogenetics: interaction with other gene mutations. Blood 106: 3740-3746 (2005) 5. Döhner K, Tobis K, Ulrich R, Fröhling S, Benner A, Schlenk RF, Döhner H: Prognostic Significance of Partial Tandem Duplications of MLL Gene in Adult Patients 16 to 60 Years Old With Acute Myeloid Leukemia and Normal Cytogenetics. J Clin Oncol 20: 3254-3261 (2002) 6. Falini B, Mecucci C, Tiacci E, Alcalay M, Rosati R, Pasqualucci L, La Starza R, Diverio D, Colombo E, Santucci A, Bigerna B, Pacini R, Pucciarini A, Liso A, Vignetti M, Fazi P, Meani N, Pettirossi V, Saglio G, Mandelli F, Lo-Coco F, Pelicci P-G, Martelli MF: Cytoplasmatic Nucleophosmin in Acute Myelogenous Leukemia with Normal Karyotype. N Engl J Med 352;3: 254266 (2005) 45 7. Falini B, Nicoletti I, Martelli MF, Mecucci C: Acute myeloid leukemia carrying cytoplasmatic/mutated nucleophosmin (NPMc+ AML): biologic and clinical features. Blood 109: 874-885 (2007) 8. Fröhling S, Schlenk RF, Stolze I, Bihlmayr J, Benner A, Kreitmeier S, Tobis K, Döhner H, Döhner K: CEBPA Mutations in Younger Adults With Acute Myeloid Leukemia and Normal Cytogenetics: Prognostic Relevance and Analysis of Cooperating Mutations. J Clin Oncol 22: 624-633 (2004) 9. Gaidzik VI, Schlenk RF, Moschny S, Becker A, Bullinger L, Corbacioglu A, Krauter J, Schlegelberger B, Ganser A, Döhner H, Döhner K: Prognostic impact of WT1 mutations in cytogenetically normal acute myeloid leukemia: a study of the German-Austrian AML Study Group. Blood 113: 4505-4511 (2009) 10. Haber DA, Buckler AJ, Glaser T, Call KM, Pelletier J, Sohn RL, Douglass EC, Housman DE: An Internal Deletion within an 11p13 Zinc Finger Gene Contributes to the Development of Wilms’ Tumor. Cell 61: 1257-1269 (1990) 11. Hohenstein P, Hastie ND: The many facets of the Wilms’ tumour gene, WT1. Hum Mol Genet 15: 196-201 (2006) 12. Inoue K, Ogawa H, Sonoda Y, Kimura T, Sakabe H, Oka Y, Miyake S, Tamaki H, Oji Y, Yamagami T, Tatekawa T, Soma T, Kishimoto T, Sugiyama H: Aberrant Overexpression of the Wilms Tumor Gene (WT1) in Human Leukemia. Blood 89: 1405-1412 (1997) 13. Kelly LM, Gilliland DG: Genetics of Myeloid Leukemia. Annu Rev Genomics Hum Genet 3: 179-198 (2002) 14. King-Underwood L, Renshaw J, Pritchard-Jones K: Mutations in the Wilms’ tumor gene WT1 in leukemias. Blood 87: 2171-2179 (1996) 46 15. King-Underwood L, Pritchard-Jones K: Wilms’ Tumor (WT1) Gene Mutations Occur Mainly in Acute Myeloid Leukemia and May Confer Drug Resistance. Blood 91: 2961-2968 (1998) 16. Kreidberg JA, Sariola H, Loring JM, Maeda M, Pelletier J, Housman D, Jaenisch R: WT1 is required for early kidney development. Cell 74: 679-691 (1993) 17. Little SE, Hanks SP, King-Underwood L, Jones C, Rapley EA, Rahman N, Pritchard-Jones K: Frequency and Heritability of WT1 Mutations in Nonsyndromic Wilms’ Tumor Patients: A UK Children’s Cancer Study Group Study. J Clin Oncol 22: 4140-4146 (2004) 18. Mead AJ, Linch DC, Hills RK, Wheatley K, Burnett AK, Gale RE: FLT3 tyrosine kinase domain mutations are biologically distinct from and have significantly more favorable prognosis than FLT3 internal tandem duplications in patients with acute myeloid leucemia. Blood 110: 1262-1270 (2007) 19. Menke AL, van der Eb AJ, Jochemsen AG: The Wilms’ tumor 1 gene: oncogene or tumor suppressor gene. Int Rev Cytol 181: 151-212 (1998) 20. Mrózek K, Bloomfield CD: Chromosome Aberrations, Gene Mutations and Expression Changes, and Prognosis in Adult Acute Myeloid Leukemia. Hematology 2006 : 169-177 (2006) 21. Mrózek K, Marcucci G, Paschka P, Whitman SP, Bloomfield CD: Clinical relevance of mutations and gene-expression changes in adult acute myeloid leukemia with normal cytogenetics: are we ready for a prognostically priorized molecular classification? Blood 109: 431-448 (2007) 47 22. Pabst T, Mueller BU, Zhang P, Radomska HS, Narravula S, Schnittger S, Behre G, Hiddemann W, Tenen DG: Dominant-negative mutations of CEBPA, encoding CCAAT/enhancer binding protein- (C/EBP), in acute myeloid leukemia. Nat Genet 27: 263-270 (2001) 23. Paschka P, Marcucci G, Ruppert AS, Whitman SP, Mrózek K, Maharry K, Langer C, Baldus CD, Zhao W, Powell BL, Baer MR, Carroll AJ, Caligiuri MA, Kolitz JE, Larson RA, Bloomfield CD: Wilms Tumor 1 Gene Mutations Independently Predict Poor Outcome in Adults With Cytogenetically Normal Acute Myeloid Leukemia: A Cancer and Leukemia Group B Study. J Clin Oncol 26: 1-9 (2008) 24. Pritchard-Jones K, Renshaw J, King-Underwood L: The Wilms tumour (WT1) gene is mutated in a secondary leukaemia in a WAGR patient. Hum Mol Genet 3: 1633-1637 (1994) 25. Riccardi VM, Sujansky E, Smith AC, Francke U: Chromosomal imbalance in the Aniridia-Wilms’ tumor association: 11p interstitial deletion. Pediatrics 61: 604-610 (1978) 26. Schlenk RF, Döhner K, Krauter J, Fröhling S, Corbacioglu A, Bullinger L, Habdank M, Späth D, Morgan M, Benner A, Schlegelberger B, Heil G, Ganser A, Döhner H: Mutations and Treatment Outcome in Cytogenetically Normal Acute Myeloid Leukemia. N Engl J Med 358: 1909-1918 (2008) 27. Stirewalt DL, Radich JP: The role of FLT3 in haematopoetic malignancies. Nat Rev Cancer 3: 650-665 (2003) 28. Summers K, Stevens J, Kakkas I, Smith M, Smith LL, MacDougall F, Cavenagh J, Bonnet D, Young BD, Lister TA, Fitzgibbon J: Wilms’ tumour 1 mutations are associated with FLT3-ITD and failure of standard induction chemotherapy in patients with normal karyotype AML. Leukemia 21: 550551 (2007) 48 29. Taskesen E, Bullinger L, Corbacioglu A, Sanders MA, Erpelinck CAJ, Wouters BJ, van der Poel-van de Luytgaarde SC, Damm F, Krauter J, Ganser A, Schlenk RF, Löwenberg B, Delwel R, Döhner H, Valk PJM, Döhner K: Prognostic impact, concurrent genetic mutations, and gene expression features of AML with CEBPA mutations in a cohort of 1182 cytogenetically normal AML patients: further evidence for CEBPA double mutant AML as a distinctive disease entity. Blood 117: 2469-2475 (2011) 30. Tenen DG: Abnormalities of the CEBP alpha transcription factor: a major target in acute myeloid leukemia. Leukemia 15: 688-689 (2001) 31. Vardiman JW, Thiele J, Arber DA, Brunning RD, Borowitz MJ, Porwit A, Harris NL, Le Beau MM, Hellström-Lindberg E, Tefferi A, Bloomfield CD: The 2008 revision of the World Health Organization (WHO) classification of myeloid neoplasms and acute leukemia: rationale and important changes. Blood 114: 937-951 (2009) 32. Virappane P, Gale RE, Hills RK, Kakkas I, Summers K, Stevens J, Green CL, Allen CG, Quentmeier H, Drexler H, Burnett AK, Linch DC, Bonnet D, Lister TA, Fitzgibbon J: Mutations of the Wilms’ Tumor 1 gene is a poor prognostic factor associated with chemoresistance in normal karyotype acute myeloid leukaemia. J Clin Oncol 26: 5429-5435 (2008) 33. Wouters BJ, Löwenberg B, Erpelinck-Verschueren CAJ, van Putten WLJ, Valk PJM, Delwel R: Double CEBPA mutations, but not single CEBPA mutations, define a subgroup of acute myeloid leukemia with a distinctive gene expression profile that is uniquely associated with a favorable outcome. Blood 113: 3088-3091 (2009) 34. Yang L, Han Y, Saurez Saiz F, Minden MD: A tumor suppressor and oncogene: the WT1 story. Leukemia 21: 868-876 (2007) 49 Danksagung An dieser Stelle möchte ich allen danken, ohne deren Unterstützung diese Arbeit nicht möglich gewesen wäre. Mein erster Dank gilt meiner Doktormutter Frau Professor Dr. Konstanze Döhner, die mir die Chance gegeben hat, auf diesem spannenden Gebiet forschen zu dürfen. Ganz besonders danken möchte ich meiner Betreuerin Frau Dr. Verena Gaidzik, die mich von Anfang an mit enormem Einsatz und Motivation für diese Arbeit begeistert hat. Sie hat mich während meiner gesamten Dissertation zu jeder Zeit unterstützt und in schwierigen Situationen weitergebracht. Außerdem danke ich dem gesamten Laborteam der AML-Forschungsgruppe der Universität Ulm, insbesondere Annegret Becker und Marianne Habdank, die mir während der alltäglichen Arbeit im Labor mit Rat und Tat zur Seite standen. Darüber hinaus danke ich Herrn Dr. Richard Schlenk für die statistische Auswertung unserer Forschungsergebnisse. Mein wohl größter Dank gilt meiner Familie, insbesondere meinen Eltern, die mich während meines gesamten Studiums stets mit aller Kraft unterstützt haben. Lebenslauf Aus Gründen des Datenschutzes entfernt