Mobile Genetische Elemente / Transposition
Werbung

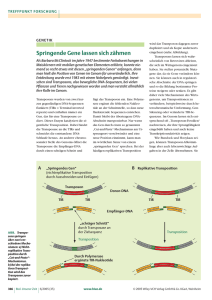
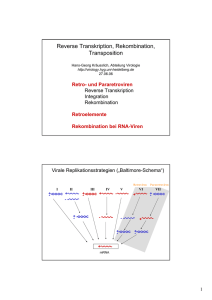
Mobile Genetische Elemente / Transposition Transposition Retrotransposition / Retroviren repetitive Elemente mobile Elemente und Genomevolution / -regulation Gentherapie Berit Jungnickel Institut für Klinische Molekularbiologie und Tumorgenetik GSF-Forschungszentrum für Umwelt und Gesundheit München [email protected] cut-paste Transposons: Insertion sequences Transposons nicht-virale Superfamilie virale Superfamilie Retroviren: endogene Retroviren Retroviren Eukaryonten einige Phagen Retrotransposons: copy-paste Prokaryonten Typen mobiler genetischer Elemente Transposition 2 Transpositionsmechanismen Conservative Transposition: Replikative Transposition: Ausschneiden, woanders einfügen an andere Stelle „kopieren“ Konservative Transposition Ausschneiden des Transposons erfolgt korrekt durch Transposase „Donor“-Chromosom muss durch Wirtsenzyme repariert werden Insertion in Zielsequenz: versetzte Schnittstellen werden eingeführt Dadurch Duplikation der Zielsequenz an Flanken des Transposons Durch Doppelstrangbrüche sind Rearrangements / Deletionen möglich (Konservative und) Replikative Transposition Mobile genetische Elemente (Bakterien) Insertion Sequences ITR: Transposase: Inverted terminal repeats Erkennungssequenz zum Ausschneiden Enzym zum Ausschneiden des Transposons und zum Einsetzen in beliebige Zielsequenz Composite Transposons 2 IS-Elemente können DNA, die zwischen ihnen liegt, „mobilisieren“: Transposition anderer Gene R-Plasmide: vermitteln multiple Antibiotikaresistenz Problem in der Klinik Beispiel: TnA-Familie (Bakterien) TnA-Transposons können NUR replikative Transposition Resolvase für Auflösung des Cointegrates erforderlich Resolvase führt zur Rekombination von res - sites in den direct repeats von Tn3 Eukaryonten: Controlling elements (Mais) Barbara McClintock (1950s): bestimmte genetische Faktoren bewirken hohes Maß an ChromosomenBrüchen in den genetischen Loci wo sie auftreten Ds (dissociation) - cytologisch detektierbar oder auch durch Ausprägung rezessiver Eigenschaften Ds Aktivierung ist abhängig von weiterem nicht-gekoppelten Gen (Ac activator) das sich auch nicht auf einen bestimmten Lokus mappen lässt... 1983 Nobelpreis für Medizin für die Entdeckung von „jumping genes“ Controlling elements (Mais) Autonom: normale Transposons inverted repeats an den Enden unterschiedliche Länge und Kodierungskapazität Nicht-Autonom: ähneln autonomen, aber mit internen Deletionen braucht autonomes Element der Familie für Aktivierung P elements (Drosophila) Transposase-Gene mit Introns 0.5-2.9 Kb Größe aber immer perfekter 31 bp inverted repeat an Termini Transposase mRNA wird nur in Keimzellen korrekt gespleißt nur dort ist Transposase-Aktivität vorhanden P element braucht Transposase für Transposition diese kann aber auch von einem anderen P Element kommen Transposition wird von einem (P-Element kodierten?) Repressor gehemmt Gentransfer/identifikation über P elements Kombination eines PElements mit einem inserierten Gen und eines intakten P elements führt zur Insertion von Fremdgenen in die Keimbahn: ...transgene Fliege... Transposon-tagging: zufällige Insertion von Transposons führt zu verschiedenen Phänotypen verantwortliches Gen kann bei bekannter Transposonsequenz identifiziert werden Rekombination durch Transposons Retrotransposition Retrotransposition Transposition über RNA-Intermediat / reverse Transkription d.h. Retrotransposon verbleibt in der DNA partielle Excision durch Rekombination der LTRs ist aber möglich „Life cycle“: bei Retroviren vom Virus aus gesehen (RNA) bei Retro(trans)posons von integrierter DNA aus... Retroelemente Retroviraler Lebenszyklus provirus Reverse Transkription U3 R U5 U3 R U5 AAA tRNA dient als Primer AAA Verlängerung in linke LTR AAA Degradation der Hybrid-RNA AAA Template switch zu rechter LTR AAA Verlängerung Meiste RNA wird entfernt Verlängerung des 2. Strangs Template switch zu linker LTR Kompletierung Integration Transkription des viralen Genoms „linke“ LTR-Sequenz initiiert Transkription LTR-Sequenzen enthalten Promotor / Enhancer „rechte“ LTR-Sequenz dient als polyA-Signal retrovirale Vektoren für starke Expression anderer Gene! Retrotransposons fakultativ oder nicht Retrotransposons Retrovirus-like Retrotransposons: alles wie bei Retroviren aber keine Verpackung in Hülle = virale Superfamilie nicht-retrovirale Retrotransposons: keine LTRs, d.h. Unterschiede bei reverser Transkription/Integration = nicht-virale Superfamilie Ty-Elemente (Hefe) virale Superfamilie Ty-Transposition geht über RNA-Intermediat, da: Erhöhung der Transkription über Gal-Promotor auch die Transposition erhöht, und da alle transponierten Ty-Elemente kein Intron mehr haben... = klassischer Retrotranspositionsassay LINE-Elemente (Mensch) nicht-virale Superfamilie LINE = long interspersed nuclear elements Viele Kopien im menschlichen Genom, viele davon sind defekt, manche können noch transponieren v.a. in nicht-kodierenden Regionen (z.B. in Introns) Reverse Transkription / Integration von LINE-Elementen „processed pseudogenes“ gespleißte mRNAs sind revers transkribiert worden und wurden durch einen ähnlichen Mechanismus wie LINE Elemente ins Genom inseriert SINE Elemente: Alu-repeats (Mensch) nicht-virale Superfamilie Alu-repeats sind häufigstes repetitives Element im menschlichen Genom (ca. alle 3000 bp), stammen von 7SL-RNA (SRP) ab und sind imperfekte Tandem-Duplikate, manche Alu-Elemente werden noch aktiv transkribiert, d.h. sie könnten sich noch weiter vermehren... Alu-repeats sind Rekombinations-Hotspots und können zu Deletionen oder Rearrangements führen - entsprechende Krankheiten sind bekannt Genomevolution durch repetitive Elemente Grün: Alu Blau: B1 Rot: L1 (LINE) Gelb: L1 repetitive Elemente haben sich aus gemeinsamen Vorläufern entwickelt (7SL RNA von SRP im Falle von Alu / B1) und haben sich relativ spät vermehrt Genomregulation durch repetitive Elemente Aktivierung: Retrotransposons werden vor allem in Eizellen / Embryos exprimiert dabei werden Fusionstranskripte von Transposon und mRNAs gebildet der originalen mRNA entsprechende oder aber neue Funktion ...Regulation der Embryonalentwicklung durch Retrotransposons...? Genomregulation durch repetitive Elemente Suppression: LTRs können Transkription des Retrotransposons in BEIDE Richtungen bewirken es entstehen doppel-strängige RNAs und über den RNAInterferenzweg siRNAs siRNAs vermitteln an homologer DNA die Assemblierung von Heterochromatin ...Regulation der Chromatinstruktur durch Retrotransposons...? Gentherapie Virale Vektoren für die Gentherapie Oncoretrovirale Vektoren (z.B. Murines Leukämie Virus, MLV): -integrierend, daher stabile Expression des Transgens -bevorzugte Integration in/um Promoter -LTRs, daher Gefahr der Aktivierung zellulärer Gene (sh. Therapie von SCID-X1) -nur für sich teilende Zellen Adenovirale Vektoren: -episomal, daher transiente Expression des Transgens -auch für nicht-teilende Zellen -Gefahr der Immunantwort (sh. Fall Jesse Gelsinger) Adeno-assoziierte Vektoren (AAV) -nicht-autonom, kleines ss-DNA-Genom -meist episomal, in <10% integrierend (passiv, an DSB-Orten im Zuge von NHEJ) Lentivirale Vektoren: -integrierend, daher stabile Expression des Transgens -bevorzugte Integration innerhalb transkribierter Regionen -LTRs, aber Gefahr der Aktivierung zellulärer Gene geringer als bei oncoretroviralen Vektoren -auch nicht-teilende Zellen Thomas, Nature Rev Genet 4:346-358,2003 Leukämie nach Gentherapie von SCID-X1 •SCID-X1: γc-Kette der Zytokin-Rezeptoren defekt, daher keine Entwicklung von B, T und NK Zellen; Hauptform von SCID in Mensch, ca. 1/80000 Geburten •ex vivo-Strategie: Transduktion von autologen hämatopoietischen Stammzellen mit Vektor (basierend auf MLV) und Re-Infusion •9 von 10 Kindern in klinischen Versuch zeigten deutliche Verbesserung des Immunsystems •aber: nach mehreren Monaten in zwei Kindern T-Zell-Leukämie •Ursache: insertionale Oncogenese durch Insertion des Vektors nahe Promoter von LMO2; dadurch Aktivierung von LMO2 (=Transkr.-faktor für Hämatopoiese) •Integrationsort in jeder transduzierten Zelle anders! d.h. bei Millionen von transduzierten Zellen 2 x Integration nahe LMO2 möglich (MLV bevorzugt in Promoternähe!); dann Selektion wegen Wachstumsvorteil •weitere begünstigende Faktoren: γc hat starke anti-apoptotische Wirkung; reduzierte Immunüberwachung Williams, Science 302:400-401 (2003) Der Fall Jesse Gelsinger •Gentherapie von Ornithin-Transcarbamylase (OTC)-Defizienz •OTC ist Enzym im Harnsäurezyklus; Hyperammonämie bei Mangel •J. Gelsinger litt an milder Form, die durch Diät und Medikamente behandelbar ist. Er stellte sich für Gentherapie-Studie zur Verfügung, obwohl selbst nicht profitierend. •Todesursache war Überreaktion des Immunsystems auf Capsidproteine des Adenovirus Sleeping Beauty Gentherapie (zB Fanconi trial) SB ist künstlich erwecktes Transposon auf Grundlage von (inaktivem) Tc1-ähnl. Transposon in Fischen. Erweckung durch Rückmutation. SB-Transposons für den Gentransfer Sicherheit: Nicht-viral — keine immunologischen Nebenwirkungen keine LTR‘s — sollten keine Onkogene aktivieren können Therapiedauer: Chromosomale Integration — lebenslange Expression des Transgens bevorzugter Zielort: ATATATAT (Palindrom/ Sekundärstruktur) Alternative: Gen-Reparatur •Korrektur einer Mutation am normalen Genort •z.B. über gene replacement / gene targeting: genutzt für Herstellung von Ko-Mäusen aber sehr ineffizient (nicht-homologe Insertion 1000x häufiger) •neue Strategie: mit ss-Oligos (ca. 35-90 nt lang; geschützte Enden durch modifizierte Nukleotide) Modelle zur Gene repair durch Oligos: 5‘ G 3‘ 3‘ C 5‘ 3‘ 5‘ 3‘ 3‘ T G T 5‘ 5‘ C Mismatch-Reparatur 3‘ 5‘ Schnitt und Insertion