Was ist die optimale Sequenz?
Werbung

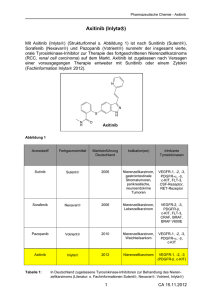
PHARMA FORTGESCHRITTENES NIERENZELLKARZINOM Was ist die optimale Sequenz? Mit Sequenztherapien lässt sich ein Fortschreiten der Erkrankung häufig verzögern und das Überleben verlängern. Welche Reihenfolge zielgerichteter Substanzen am günstigsten ist, hängt auch vom Alter der Patienten ab, wie Studien belegen. ährlich wird bei circa 15 100 Menschen in Deutschland ein Nierenzellkarzinom diagnostiziert, die Erkrankungsraten sind bei Männern höher als bei Frauen. Häufig werden die Tumoren in frühen Stadien erkannt, die Fünf-Jahres-Überlebensraten liegen für alle Stadien gesamt nach Angaben des Robert Koch-Instituts in Berlin (2012) bei circa 75 Prozent. In fortgeschrittenen Stadien ist die Prognose ungünstiger, sie hat sich aber durch die Neuentwicklung von Substanzen deutlich verbessert: „Zielgerichtete Therapien wie Sorafenib haben beim metastasierten Nierenzellkarzinom eine deutliche Verlängerung des Überlebens ermöglicht“, berichtete Priv.-Doz. Dr. med. Hubert Rudolf Kübler, Leitender Oberarzt an der Urologischen Klinik und Poliklinik am Klinikum rechts der Isar der Technischen Universität München. J Überlebenszeiten wurden deutlich verlängert Lagen in der früheren Ära der Zytokintherapie die Überlebenszeiten beim metastasierten Nierenzellkarzinom (mRCC) bei circa 13 Monaten, lassen sich nun durch die Anwendung „zielgerichteter“ Substanzen oft Überlebenszeiten von mehr als zwei Jahren erzielen. Therapiesequenzen können eine Dauertherapie der Patienten ermöglichen und damit die Erkrankung stabilisieren. „Allerdings ist gegenwärtig unklar, welche Sequenzen der sieben verfügbaren Substanzen in dieser Hinsicht optimal wirksam sind“, sagte Kübler. Die Frage der bestmöglichen Behandlungssequenz wurde in der offenen, randomisierten SWITCH1-Studie (JCO 2014; 32 [Suppl. 4]: Abstr. 393) geprüft: die Sequenz Sorafenib in der Erstlinie und Suni- A 1894 tinib in der Zweitlinie (So-Su) und die umgekehrte Reihenfolge, Sunitinib in der Erst- und Sorafenib in der Zweitlinie bei Progression oder intolerabler Toxizität (Su-So). 365 unvorbehandelte mRCC-Patienten, für die eine Zytokintherapie nicht in Frage kam, wurden 1:1 randomisiert und erhielten in sechswöchigen Zyklen entweder zweimal täglich 400 mg Sorafenib oder einmal täglich 50 mg Sunitinib für vier Wochen, gefolgt von einer Woche Pause. Bei Krankheitsprogress oder Unverträglichkeit der Therapie wurde auf den jeweils anderen Wirkstoff gewechselt. Weder im primären Studienendpunkt, dem Gesamt-Progressionsfreien Überleben (tPFS), noch im Gesamtüberleben (OS) gab es einen statistisch signifikanten Unterschied zwischen beiden Sequenzen, also auch keine Überlegenheit der Sequenz Sorafenib als Erstlinientherapie und Sunitinib als Zweitline. Eine retrospektive, hypothesen-generierende Subgruppenanalyse der finalen Daten zum OS ergab jedoch, dass Patienten älter als 65 Jahre unter So-Su im Median 11,7 Monate länger lebten, nämlich median 31,5 Monate, als unter der umgekehrten Sequenz Su-So (OS: 19,8 Monate; p = 0,04). Jüngere Patienten (≤ 65 Jahre) profitierten hingegen offenbar eher von der Sequenz Su-So (OS: 43,5 Monate; SoSu: 25,8 Monate; p = 0,07). Warum das Alter der Patienten unter der jeweiligen Sequenz das Gesamtüberleben beeinflusst, sei zurzeit unklar, sagte Kübler. Ältere Patienten ließen sich aber mit der Sequenz So-Su um 4,2 Monate länger behandeln als bei umgekehrter Reihenfolge Su-So. „Diese längere Therapiedauer der So-Su-Sequenz bei Patienten über 65 Jahren könnte eine Folge der besseren Verträglichkeit von Sorafenib in der Erstlinie und der sehr guten Krankheitskontrollrate von Sunitinib in der Zweitlinie sein“, so Küblers Einschätzung. Immuntherapien rücken stark in den Fokus der Forschung Sorafenib ist beim Nierenzellkarzinom zur Behandlung von Patienten mit fortgeschrittener Erkrankung indiziert, wenn es unter der Behandlung mit Interferon alpha oder mit Interleukin 2 zum Progress kam oder eine Zytokintherapie nicht indiziert ist. Zytokinbehandlungen gehören zu den „frühen“ Immuntherapien. In den Fokus der aktuellen Forschung rücken zunehmend auch weitere immunologische Strategien, bei denen zum Beispiel eine gegen Tumorzellen gerichtete Immunantwort von T-Zellen stimuliert wird. BayerHealthCare entwickelt für die Erforschung solch neuer Strategien eine Plattform in Kooperation mit dem Deutschen Krebsforschungszentrum (DKFZ) in Heidelberg. Der Biologe und Arzt Prof. Dr. med. Rienk Offringa ist Leiter des gemeinsamen Forschungslabors am DKFZ. Besonders vielversprechend seien eine Aktivierung von T-Zellen gegen Tumorzellen durch Antikörper, die hemmende Signale (Immun-Checkpoints) antagonisieren, bispezifische Antikörper, die T- und Tumorzellen miteinander verbinden und die Lyse der Krebszellen auslösen, tumorinfiltrierende Lymphozyten (TIL) aus Biopsien, die ex vivo vermehrt und dem Patienten reinfundiert werden, und die Infusion autologer T-Zellen, die Antigenrezeptoren mit Spezifität für Tumor▄ zellen exprimieren. Dr. rer. nat. Nicola Siegmund-Schultze Quelle: Presse Campus Onkologie in Berlin: „Klinische Praxis und Trends in der OnkologieForschung“, Bayer HealthCare. Deutsches Ärzteblatt | Jg. 112 | Heft 45 | 6. November 2015