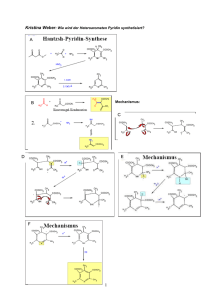
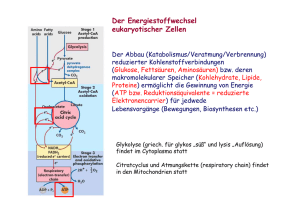
Kohlenhydrate und Kohlenhydrat-Stoffwechsel.
Werbung

1 Kohlenhydrate und Kohlenhydrat-Stoffwechsel. Ziel dieses Versuches ist es, zum Einen durch qualitative Analyse ausgewählter Zucker Einblick in deren chemische Eigenschaften und deren Bedeutung zu erhalten, zum Anderen durch kinetische Messungen an einer "Teilstrecke" der Glycolyse Charakteristika dieses Energie-erzeugenden Stoffwechselprozesses besser zu verstehen. Stichworte zur Vorbereitung Struktur und Chemie der Zucker. Definition und Beispiele für : Aldosen, Ketosen, Hexosen, Pentosen, Triosen etc. Glucose: offenkettige Form, Haworth-Darstellung. Definition und Beispiele für: Monosaccharide, Oligosaccharide, Polysaccharide. Kohlenhydrate als Energiereserve und als Baustoffe: Stärke, Glycogen, Cellulose. α- und ß-glycosidische Bindung. Kohlenhydratstoffwechsel: Aminozucker, Zuckeralkohole, On- und Uronsäuren, aerobe und anaerobe Glycolyse, Substratkettenphosphorylierung, Oxidation eines Thiohalbacetals, Phosphorolyse eines Thioesters und ATP-Synthese, Energieausbeute der Glycolyse. Beziehung der Glycolyse zu anderen Stoffwechselwegen. Fructose- und Galactosestoffwechsel. Einführung. Als "Kohlenhydrate" bezeichnet man Polyhydroxyaldehyde und -ketone und ihre oligomeren und polymeren Verbindungen, die durch Hydrolyse wieder in ihre monomeren Bausteine, die "Zucker" : Glucose, Fructose, Galactose, Mannose etc. zerlegt werden können. Von großer Bedeutung sind auch Zucker, bei denen Hydroxyl- oder Aldehydfunktionen zu Säurefunktionen oxidiert sind (Zuckersäuren) oder Zucker bei denen eine Hydroxylgruppe durch eine Aminogruppen ersetzt ist. (Aminozucker) Dabei kommt der Glucose eine zentrale Bedeutung als Energieträger in allen pflanzlichen und tierischen Organismen zu. Unter anaeroben Bedingen können viele Einzeller, die weder zur Photosynthese noch zur Lithotrophie (Energiegewinnung durch Oxidation anorganischer Substanzen) befähigt sind, ihre Energie letztlich nur durch Glycolyse, den Abbau des C6-Körpers Glucose zu C3- oder C2-Körpern, erzeugen. Einige Zellen und Gewebe höherer Organismen verwenden aus unterschiedlichen Gründen nur Glucose als alleinige Energiequelle und bauen diese glycolytisch - auch in Gegenwart von Sauerstoff - lediglich zu Lactat ab. (Glaskörper, Zellen der Cornea, Erythrozyten). 2 Versuch 1 Reduzierende Wirkung von Aldosen und Ketosen Prinzip: In alkalischer Lösung reagieren Aldosen (z.B. Glucose) und Ketosen (z.B. Fructose) mit verschiedenen Oxidationsmitteln, die dabei reduziert werden. Bei den sogenannten "Reduktionsproben" werden die Zucker durch leicht reduzierbare Metallionen oder Farbstoffe zu den entsprechenden "On-säuren" oxidiert. (z.B. die Glucose zu Gluconsäure). So werden z.B. Cu 2+ - Ionen zu unlöslichem Cu2O + (Fehlingsche Reaktion) , Ag -Ionen zu metallischem Silber (Silberspiegel an einer Glasoberfläche) oder verschiedene Farbstoffe zu ihren farblosen "Leuko"-formen reduziert. Beispielsweise werden dunkelblaue Lösungen von Methylenblau weitgehend entfärbt. (Es entsteht dabei das Leukomethylenblau, welches allerdings durch Luftsauerstoff leicht wieder reoxidiert werden kann.) Eine positive Reaktion wird bei einfachen Zuckern und bei Oligosacchariden beobachtet, sofern sie eine reduzierende Gruppe enthalten. Glycosidische Bindungen werden nicht oxidiert. Nicht reduzierend wirken daher Saccharose (die gleichzeitig ein Glucosid und ein Fructosid darstellt) und Trehalose, in der zwei halbacetalische Gruppen von zwei Glucosemolekülen ein Vollacetal bilden. Aus diesen Disacchariden entstehen erst nach hydrolytischer Spaltung reduzierende Zucker. Diese Spaltung kann im Falle der Saccharose enzymatisch durch die Invertase erfolgen. Die verschiedenen Zucker sind unter basischen Bedingungen über ein gemeinsames Endiol ineinander überführbar. Als Beispiel für die Glucose / Fructose / Mannose - Umwandlung sei die "Lobry de Bruyn-van Ekenstein Umlagerung" genannt : 3 In der Medizin wird häufig eine quantitative Bestimmung von Glucose benötigt. In der Praxis benützt man dafür ein spezifisches Enzym (Glucoseoxidase), das nur Glucose oxidieren kann. (Siehe Versuch Organstoffwechsel) Lösungen und Apparate 1. 1%ige Lösungen der Zucker: Glucose, Fructose und Saccharose zu Vergleichszwecken. 2. Invertase-Lösung (1 mg/ml in 0.1 M Na-Acetat, pH 4.7) 3. 1%ige wässrige Methylenblaulösung 4. 0.02 N NaOH 5. 0.5 N NaOH 6. Inkubator (Temperatureinstellung 56 °C) Durchführung 5 Eppendorfgefäße (1.2 ml) beschriften (1 - 5) und wie folgt beschicken mit: H2O, Glucose-, Fructose-,Saccharoselösung oder der unbekannten Probe, der Methylenblaulösung und der 0.02 N NaOH. Gefäß Nr. 50 µl 5 µl 1000 µl 1 H2O 2 3 4 5 Glucose Fructose Saccharose unbekannte Probe 1 %ige Methylenblaulösung in alle Gefäße 0.02 N NaOH in alle Gefäße Gefäße verschließen, kurz schütteln, in den Inkubator stellen und im Abstand von ca. 30 sec die Entfärbung in den Gefäßen überprüfen. Wenn in einem der Gefäße erste Entfärbungstendenzen sichtbar werden, die Geschwindigkeit der Entfärbung mit anderen Gefäßen vergleichen. Bei den Gefäßen, in denen eine Entfärbung stattfindet, die Zeit notieren, die zur vollständigen Entfärbung notwendig war. Wie verhielt sich Gefäß Nr. 5 (unbekannte Probe) ? Das Experiment in gleicher Weise mit 0.5 N NaOH wiederholen. Achten Sie dabei auf Unterschiede in den Entfärbungsgeschwindigkeiten im Vergleich zum vorhergehenden Experiment. Zeit bis zur vollständigen Entfärbung ebenfalls möglichst genau protokollieren! Durchführung mit vorheriger Invertasebehandlung Gefäß Nr. 50 µl 10 µl 5 µl 1000 µl 1 H2O 2 3 4 5 Glucose Fructose Saccharose Unbekannte Probe Invertase-Lösung in alle Gefäße 5 min bei 56 oC inkubieren und danach hinzufügen: 1%ige Methylenblaulösung in alle Gefäße 0.5 N NaOH in alle Gefäße Achten Sie hier besonders auf das Verhalten von Gefäß Nr. 4 im Vergleich zu den vorherigen Experimenten. Falls Gefäß Nr. 5 (unbekannte Probe) vorher nicht entfärbt wurde, welches Verhalten zeigt sich jetzt ? 4 Versuch 2: Reversible Teilreaktion der Glycolyse. Die aus 11 enzymatischen Schritten bestehende Glycolyse ist insgesamt exergon, dabei wird ein Teil der Energie zur Synthese von ATP verwendet. Drei dieser Schritte (1., 3. und 10.) sind stark exergon: Die Hexokinase- , Phosphofructokinase- und die Pyruvatkinase-Reaktion ; das Gleichgewicht liegt bei diesen Reaktionen also weitgehend auf der Seite der Produkte: Glucose-6phosphat, Fructose-1,6-bisphosphat und Pyruvat.. Alle anderen Schritte sind unter physiologischen Bedingungen mehr oder weniger reversibel und stehen auch der Gluconeogenese zur Verfügung. Kinetische Experimente an diesem "mittleren, reversiblen" Bereich (von der Aldolase bis zur Phosphoglyceratkinase) sind Gegenstand dieses Versuchs. Lehrbuch der Biochemie zur Hand nehmen ! Im Mittelpunkt unserer Experimente steht der Abschnitt der Glycolyse von der Triosephosphat-isomerase bis zur Phosphoglycerat-kinase : 1. Die Isomerisierung der Triosen 2. Die anschließende Oxidation einer der Triosen durch NAD bei gleichzeitiger Produktion einer energiereichen Verbindung 3. Die Produktion von ATP mit Hilfe dieser energiereichen Verbindung Den drei Schritten geht die Aldolase voraus. Im Verlauf dieser Lyase-Reaktion erfolgt der Übergang von: Hexosen zu Triosen Triosen zu Hexosen in Glycolyse-Richtung in Gluconeogenese-Richtung Der Einfluß dieser Gleichgewichtsreaktion auf die nachfolgenden Triose-Reaktionen soll ebenfalls untersucht werden. Alle für diese Experimente zur Verfügung stehenden Substrate / Cosubstrate und Enzyme sind im nachfolgenden Schema kursiv und unterstrichen: Dihydroxyacetonphosphat, NAD, ADP, HPO42- und die Enzyme Aldolase, Triosephophat- isomerase, Glyceraldehydphosphat-dehydrogenase und Phosphoglycerat-kinase. 5 Überblick. Reversible Teilreaktion der Glycolyse. Aldolase("ALDO"): Fructose-1,6-bisphosphat ↔ Glyceraldehyd-3-phosphat + Dihydroxyacetonphosphat Zu den Triosen Zu den Hexosen Triosephosphat-isomerase ("TIM"): Dihydroxyacetonphosphat (DHAP) ↔ Glyceraldehyd-3-phosphat Glyceraldehyd-3-phosphat-dehydrogenase ("GAPDH"): Glyceraldehyd-3-phosphat + NAD + HPO42- ↔ 1,3-Bisphosphoglycerat + NADH + H+ HAsO42- statt HPO42Entkopplung durch Arsenat Keine Bildung von 1,3-Bisphosphoglycerat und damit keine ATP-Bildung Phosphoglycerat-kinase("PGK") 1,3-Bisphosphoglycerat + ADP ↔ 3-Phosphoglycerat (3-PG) + ATP Die Möglichkeit der einfachen photometrische Verfolgung der NADH - Bildung ist die Basis für vielfältige und empfindliche kinetische Untersuchungen an dieser Glycolyse-Teilstrecke. NADH besitzt im Gegensatz zu seiner oxidierten Form (NAD) ein hohes Absoptionsmaximum bei 340 nm. Absorptionskoeffizient ε340 = 6200 (mol/l)-1.cm-1. Im Filterphotometer wird bei 366 nm gemessen: ε366 = 3200 (mol/l)-1.cm-1. (Zur Erinnerung : Siehe „Biochemische Labormethoden“) 6 Wie man aus dem Schema weiter entnehmen kann, erfolgt innerhalb dieser Kette einer der beiden ATP-Synthese-Schritte der Glycolyse. Wenn wir nun bei der GAPDH statt Phosphat ( HPO42- ) Arsenat ( HAsO42- ) anbieten, entsteht statt 1,3-Bisphosphoglycerat 1-Arseno, 3-phospho-glycerat, welches spontan zu 3-Phospho-glycerat hydrolysiert. Auf diese Weise wird die NADH - Bildung von der ATP-Bildung in der PGK "entkoppelt " . Die GAPDH-Reaktion wird unabhängig vom ADP-Angebot in der nachfolgenden PGK-Reaktion: die NADH-Produktion läuft entsprechend schneller ab. Alle folgenden gekoppelten Reaktionen finden in Halbmikroküvetten statt. Es wird zunächst 500 µl 0.1 M TRIS-Puffer, pH 7.7 vorgelegt. Die nachfolgenden Zugaben von Enzymen erfolgen in 2 bis 10 µl-Portionen, die der Substrate in 5 bis 50 µl-Portionen. Die vorbereiteten Enzymlösungen enthalten je ca. 1000 U / ml, die Konzentrationen der zur Verfügung gestellten Stammlösungen der Substrate/Cosubstrate betragen 10 mmol/l bei NAD, 40 mmol/l bei Dihydroxyacetonphosphat und ADP und 500 mmol/l bei Phosphat. Dem Ansatz wird noch 1 µl 1 mol/l Dithiothreitol (DTT) zugesetzt zum Schutz der essentiellen SH-Gruppen der GAPDH. Als Entkoppler der Substratkettenphosphorylierung steht 100 mmol/l Arsenat und als irreversibler Inhibitor der GAPDH steht 0.5 mol/l Iodacetamid (SH-Reagenz) zur Verfügung. Bei den nachfolgend beschriebenen Aufgaben wird nach Zugabe aller Enzyme und Substrate am Photometer die Absorption bei 340 nm (oder 366 nm bei Verwendung eines Filterphotometers) im 10 sec Abstand bis zum Stillstand der Reaktion notiert (d.h. bis keine Absorptionsänderung mehr stattfindet und die Reaktion damit ihr Gleichgewicht erreicht hat). (Nach Rücksprache mit dem Betreuer können an den Aufgaben bei Bedarf auch kleine Veränderungen vorgenommen werden, bezüglich Abfolge und Volumina der einzelnen Zugaben.) 1. Aufgabe (Äquimolare Konzentrationen der Substrate/Cosubstrate: ADP, NAD, Dihydroxyacetonphosphat zu Beginn der Reaktion) (ohne Aldolase) 500 µl TRIS-Puffer 0.1 M, pH 7.7 2 µl TIM (2 U / 2 µl) 2 µl GAPDH (2 U / 2 µl) 2 µl PGK (2 U / 2 µl) Berechnen Sie die Konzentration der Substrate bei Reaktionsstart ! 1 µl DTT 1 mol/l 20 µl NAD 10 mmol/l 5 µl ADP 40 mmol/l 20 µl Phosphat 0.5 mol/l System etwa 2 min bei 340 oder 366 nm beobachten (Absorption notieren) und dann starten durch Zugabe von : 5 µl DHAP 40 mmol/l Berechnen Sie aus der Absorptionsdifferenz (AE - AS) die Konzentration des gebildeten NADH AS : Absorption bei Reaktionsstart AE : Absorption nach Stillstand der Reaktion 7 Wieviel eingesetztes NAD wurde zu NADH reduziert ? Versuchen Sie die Anfangsgeschwindigkeit ("Anfangssteigung") zu ermitteln aus der Absorptionsänderung in den ersten 20 oder 60 Sekunden. (V20 oder V60, erfahrungsgemäß liefert V60 den zuverlässigeren Wert. Berechnungen siehe Protokollvordruck ! ) Variationen der Experimente: Statt mit Dihydroxyacetonphosphat kann auch mit ADP, NAD oder einem der Enzyme gestartet werden d.h. die Abfolge der Zugaben kann selbstverständlich geändert werden. Die Reaktion startet erst dann (d.h. die NADH-Bildung beginnt erst dann) wenn das System komplett ist. Berechnung der Gleichgewichtskonstanten K und der Gibbs' freien Standardenthalpie ∆G° '. Für unsere Reaktion: TIM, GAPDH, PGK DHAP + NAD + ADP + P 3-PG + NADH + ATP gilt bei obigen äquimolaren Ausgangsbedingungen für die drei Quotienten: [3-PG] / [DHAP] = [NADH] / [NAD] = [ATP] / [ADP] während der gesamten Reaktion (bis zur Erreichung des Gleichgewichts). Nun kann das Massenwirkungsgesetz folgendermaßen formuliert werden: [3-PG] . [NADH] K= . . . [ATP] [DHAP] [NAD] [ADP] . 1 oder: K = ( [NADH] / [NAD] ) 3 . 1 / [P] [P] Aus dem [NADH]/[NAD] -Quotient läßt sich also leicht die Gleichgewichtskonstante unter den gegebenen Bedingungen ausrechnen, da die relativ hohe Phosphatkonzentration ( [P] ) sich während der Reaktion praktisch nicht ändert. Diese Gleichgewichtskonstante entspricht dem Produkt der drei einzelnen Gleichgewichtskonstanten der TIM-, GAPDH- und der PGK-Reaktion: K = KTIM . KGAPDH . KPGK Diese Konstanten können vom amerikanischen National Institute of Standards and Technology (NIST) geholt werden. (http://wwwbmcd.nist.gov:8080/enzyme/enzyme.html). Auf freiwilliger Basis dürfen Interessierte die Übereinstimmung ihrer experimentellen Daten mit den Literatur-Daten überprüfen. Aus der Gleichgewichtskonstanten kann ferner noch die Gibbs' freie Standardenthalpie berechnet werden : ∆G° ' = − R . T . ln K. (Allgemeine Gaskonstante R = 8.314 J . mol-1 . K-1 T = absolute Temperatur) Siehe Rechenbeispiel am Ende dieser Praktikumsvorschrift ! 8 2. Aufgabe ( Einfluss der Aldolase auf die Reaktion ) 500 µl TRIS-Puffer 0.1 M, pH 7.7 5 µl ALDO (5 U / 5 µl) 2 µl TIM (2 U / 2 µl) 2 µl GAPDH (2 U / 2 µl) Berechnen Sie die Konzentration der Substrate bei Reaktionsstart ! 2 µl PGK (2 U / 2 µl) 1 µl DTT 1 mol/l 20 µl NAD 10 mmol/l 5 µl DHAP 40 mmol/l 20 µl Phosphat 0.5 mol/l System etwa 2 min bei 340 nm oder 366 nm beobachten (Absorption notieren) und dann starten durch Zugabe von: 5 µl ADP 40 mmol/l Wie wirkt sich die zusätzliche Aldolase aus, im Vergleich zum, sonst identischen, vorhergehenden Experiment ? Achten Sie auf evtl. andere Anfangsgeschwindigkeiten. Wie wäre eine geringere Geschwindigkeit der NADH-Bildung zu erklären ? 3. Aufgabe ( Entkopplung der GAPDH - Reaktion durch Arsenat, 3-PG entsteht jetzt auch in Abwesenheit von ADP und PGK) 500 µl TRIS-Puffer 0.1 M, pH 7.7 2 µl TIM (2 U / 2 µl) 2 µl GAPDH (2 U / 2 µl) Berechnen Sie die Konzentration der Substrate bei Reaktionsstart ! 1 µl DTT 1 mol/l 10 µl NAD 10 mmol/l 50 µl DHAP 40 mmol/l System etwa 2 min bei 340 nm oder 366 nm beobachten (Absorption notieren) und dann starten durch Zugabe von: 20 µl Arsenat 100 mmol/l Rechnen Sie hier nach, ob unter diesen Bedingungen das eingesetzte NAD vollständig zu NADH reduziert wurde. 4. Aufgabe Wiederholen Sie das vorhergehende Experiment . Wenn ungefähr ein Drittel der Endabsorption dieses Experiments erreicht ist, geben Sie 5 µl Jodacetamid hinzu. Beobachtung ? 9 Fragen 1. Wie verhält sich die, aus den Bausteinen Glucose und Fructose bestehende Saccharose bei den sogenannten Reduktionsproben, wie z. B. bei der Fehlingschen Probe? 1. Ist die Verknüpfung zwischen den Bausteinen der Saccharose α-glycosidischer oder ß-glycosidischer Natur ? Oder beides ? Erklärung ? 2. Was ist ein Halbacetal ? 3. Was versteht man unter pyranosiden und furanosiden Formen der Zucker ? 4. Wie entstehen sie aus der offenkettigen Form ? 5. Glucose und Fructose: Vorwiegend Furanoside oder Pyranoside ? 6. Bei der phosphorolytischen Spaltung von Glycogen entsteht Glucose-1-phosphat, welches dann zu Glucose-6-phosphat isomerisiert werden kann. Wie unterscheiden sich die beiden Zuckerphosphate bezüglich Energieinhalt und Art der Phosphatbindung ? 7. Wie heißt das Enzym, welches diese Isomerisierung katalysiert ? Wo liegt das Gleichgewicht ? 8. Im Verlauf der Glycolyse spielen Hexose- und Triosephosphate mit sehr unterschiedlichen Energieinhalten (freier Energie der Hydrolyse) eine Rolle: Beschreiben Sie die Unterschiede zwischen normalen Phosphorsäureestern, den Gemischtsäureanhydriden und Enolester. 9. Welche Bedeutung haben letztere bei der ATP- Synthese ? 10. Was versteht man unter "Gruppenüberträgerpotential" ? 11. Nennen Sie Einzelheiten der GAPDH -Reaktion. Welche Rolle spielen essentielle SH-Guppen des Enzyms ? Skizzieren Sie die Oxidation des Thiohalbacetals zum Thioester durch NAD und die anschließende phosphorolytische Spaltung des Thioesters. 12. Was versteht man unter "Substratkettenphosphorylierung" ? 13. Welche Auswirkungen auf das Enzym haben Alkylierungsmittel, die die SHGruppen der GAPDH in stabile Thioether umwandeln ? 14. Beschreiben Sie den Unterschied zwischen Hemmung und Entkopplung der Substratkettenphosphorylierung. 15. Welche Schritte der Glycolyse sind irreversibel ? 16. In welchem Zellkompartiment findet die Glycolyse statt ? 17. Welche Zellen und Gewebe des Menschen gewinnen ihre Energie ausschließlich durch Glycolyse ? Nennen Sie die Gründe für den Verzicht auf den energetisch viel ergiebigeren vollständigen Abbau der Glucose zu CO2 und H2O. 18.Angenommen, ∆G°' für DHAP+NAD+ADP+P ↔ 3-PG+NADH+ATP wäre positiv, unsere Reaktion also endergon (unter Standardbedingungen !), warum würde trotzdem zumindest zu Beginn, 3-PG, NADH und ATP gebildet ? Betrachten Sie dazu die Gleichung: ∆G = ∆G°' + RT ln ( [3-PG][NADH][ATP] / [DHAP][NAD][ADP][P] ) Erläutern Sie die Unterschiede zwischen freier Enthalpie ∆G und freier Standardenthalpie ∆G°' . Welche Rolle spielen die Konzentrationen der Stoffe ? Welchen Wert nimmt ∆G an, wenn die Reaktion zum Stillstand gekommen ist und damit ihr Gleichgewicht erreicht hat ? (Siehe auch Taschenatlas der Biochemie 2. Auflage S. 16/17). 10 Protokoll zum Versuch Kohlenhydrate / Kohlenhydratstoffwechsel 1. Reduzierende Wirkung von Aldosen und Ketosen mit 0.02 N NaOH Gefäß Nr. 1 2 3 4 5 H2O Glucose Fructose Saccharose unbekannte Probe Zeit [min] bis zur vollständigen Entfärbung mit 0.5 N NaOH Gefäß Nr. 1 2 3 4 5 H2O Glucose Fructose Saccharose unbekannte Probe Zeit [min] bis zur vollständigen Entfärbung nach Behandlung mit Invertase Gefäß Nr. Zeit [min] bis zur vollständigen Entfärbung Kommentar: 1 2 3 4 5 H2O Glucose Fructose Saccharose unbekannte Probe 11 2. Reversible Teilreaktion der Glycolyse. Berechnung von V20 bzw. V60 und [NAD]S , [NAD]E, [NADH]E : V20 bzw. V60 Anfangsgeschwindigkeit 20 bzw. 60 sec. nach Reaktionsstart V20 = 5.107 . (A20 - AS) / ε [nmol/l . sec-1] V60 = 1.67.107 . (A60 - AS) / ε [nmol/l . sec-1] [NAD]S NAD-Startkonzentration [NAD]E NAD-Endkonzentration [NADH]E NADH-Endkonzentration [NADH]E = 103 . (AE − AS) / ε [mmol/l] [NAD]E = [NAD]S − [NADH]E [mmol/l] 1. Aufgabe AS A20 A60 AE Absorption bei Reaktionsstart Absorption nach 20 sec Absorption nach 60 sec Absorption bei Reaktionsende 2. Aufgabe AS A20 A60 AE AS A20 A60 AE V20 V60 [NAD]S [NAD]E [NADH]E [NADH]E / [NAD]E (nmol/l) . sec-1 (nmol/l) . sec-1 mmol/l mmol/l mmol/l V20 V60 [NAD]S [NAD]E [NADH]E [NADH]E / [NAD]E (nmol/l) . sec-1 (nmol/l) . sec-1 mmol/l mmol/l mmol/l V20 V60 [NAD]S [NAD]E [NADH]E [NADH]E / [NAD]E (nmol/l) . sec-1 (nmol/l) . sec-1 mmol/l mmol/l mmol/l V20 V60 [NAD]S [NAD]E [NADH]E [NADH]E / [NAD]E (nmol/l) . sec-1 (nmol/l) . sec-1 mmol/l mmol/l mmol/l Entkopplung der GAPDH durch Arsenat Absorption bei Reaktionsstart Absorption nach 20 sec Absorption nach 60 sec Absorption bei Reaktionsende 4. Aufgabe ε340 = 6200 (mol/l)-1 . cm-1 (Monochromator 340 nm) ε366 = 3300 (mol/l)-1 . cm-1 (Filterphotometer Eppendorf) Einfluß der Aldolase auf die Reaktion Absorption bei Reaktionsstart Absorption nach 20 sec Absorption nach 60 sec Absorption bei Reaktionsende 3. Aufgabe AS A20 A60 AE Äquimolare Konzentrationen von NAD, DHAP, ADP Hemmung der GAPDH durch Iodacetamid Absorption bei Reaktionsstart Absorption nach 20 sec Absorption nach 60 sec Absorption bei Reaktionsende 12 Kommentare zur 1. Aufgabe: (Äquimolare Konzentrationen von NAD, ADP, DHAP) Welche Gleichgewichtskonstante für die Reaktion: NAD + DHAP + ADP + P ↔ NADH + 3-GP + ATP ergibt sich aus dem NADH zu NAD Verhältnis unter den gegebenen Bedingungen ? Welcher Wert ergibt sich für die Gibbs' freie Standardenthalpie ∆G°' ? Welche Aussage steckt in diesen Konstanten ? Kommentare zur 2. Aufgabe: (Gegenwart von Aldolase) Geben Sie eine Begründung, falls die Anfangsgeschwindigkeit im Vergleich zur 1. Aufgabe niedriger oder höher ist (bei sonst gleichen Substratkonzentrationen). Kommentare zur 3. Aufgabe: (Entkopplung durch Arsenat) Vergleichen Sie Anfangsgeschwindigkeit und NADH-Endkonzentration mit den vorherigen Daten. Wird NAD vollständig zu NADH umgesetzt, nachdem die ATP-Synthese "abgekoppelt" wurde ? Kommentare zur 4. Aufgabe: (Wirkung des Alkylierungsmittels Jodacetamid) 13 Beispiel für die Berechnung der Gleichgewichtskonstanten K und der Gibbs' freien Standardenthalpie ∆G°' der Reaktion: TIM, GAPDH, PGK DHAP + NAD + ADP + P 3-PG + NADH + ATP (1. Aufgabe von Versuch 2) Berechnung der NAD-Startkonzentration: Das Gesamtvolumen in der Küvette war 557 µl davon war: 20 µl 10 mmol/l NAD (die NAD-Lösung wurde damit 1: 27.85 verdünnt) Also: 10 / 27.85 = 0.359 [NAD]Start = 0.359 mmol/l Am Eppendorf-Photometer wurde nun folgende Absorptionsdifferenz (AE - AS) nach Erreichung des Gleichgewichtes erhalten: Daraus ergibt sich bei ε366 = ∆A = 0.5 (war tatsächlich so: exakt 0.1 → 0.6) 3300 (mol/l)-1 . cm-1 NADH-Endkonzentration also: NAD-Endkonzentration: [NAD]Ende = die NADH-Konzentration: 0.5 / 3300 = 1.515 . 10-4 [NADH]Ende = 0.151 mmol/l [NAD]Start − [NADH]Ende [NAD]Ende = 0.208 mmol/l Bei Erreichung des Gleichgewichts ergibt sich also folgender NADH / NAD-Quotient: [NADH] / [NAD] = 0.726 Berechnung der Phosphatkonzentration: (ändert sich während der Reaktion praktisch nicht) 20 µl 0.5 mol/l Phosphat 1 : 27.85 verdünnt (wie oben) [P] = 0.018 mol/l In unsere Gleichung K = ( [NADH] / [NAD] ) 3 . 1 / [P] eingesetzt, ergibt sich: K = 21.26 Daraus läßt sich folgende Gibbs' freie Standardenthalpie errechnen: ∆G°' = − R .T. ln K = − 8.314 . 300 . ln 21.26 = − 7624 J . mol-1 ∆G°' = − 7.6 kJ . mol-1