Mikrobiolobie - Bakteriologie I
Werbung
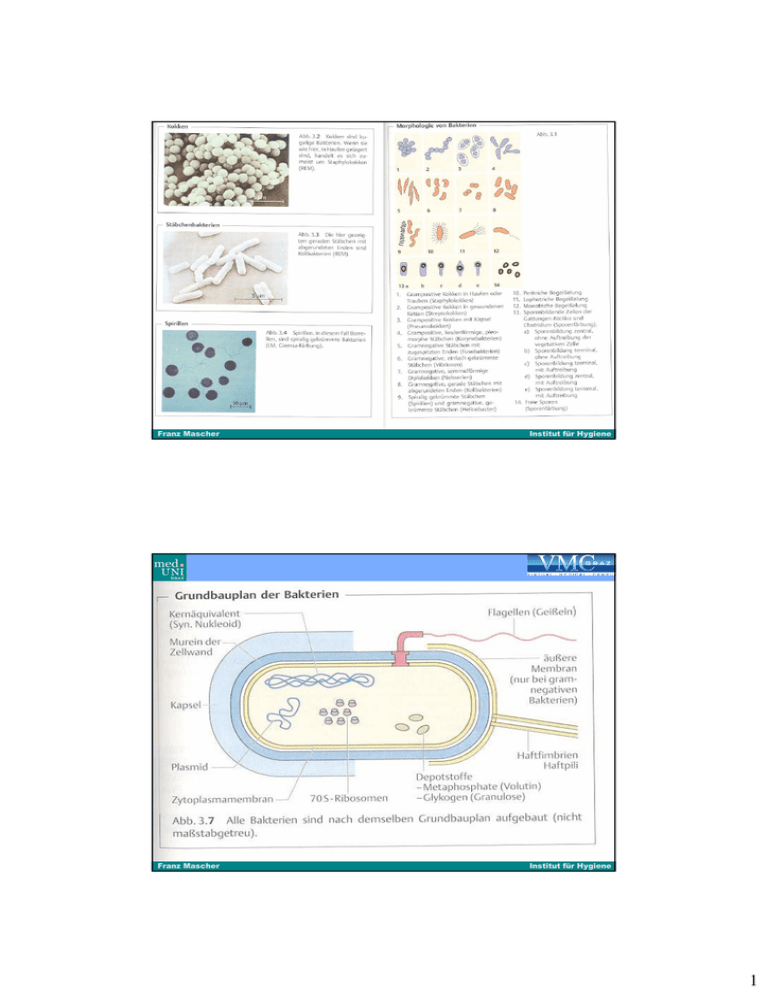
1 Feinstruktur - Prokaryontes Kernäquivalent: Nukleoid = "nacktes" DNA-Molekül. Dieses prokaryonte Kernäquivalent entspricht funktionell dem eukaryonten Zellkern. Bei der Vermehrung der Bakterien steht am Anfang immer die Reduplikation des Nukleoids. - Plasmide: extrachromosomale, ringförmige, doppelsträngige DNAStruktur: Pathogenitäts- Resistenzplasmide und metabolische Plasmide - Zytoplasma: große Zahl von in Wasser gelösten nieder- und hochmolekularen Stoffen, RNS, und viele Ribosomen (70S; Proteinbiosynthese), Reservestoffe in unlöslicher Form - Zytoplasmamembran = "unit membrane": Phospholipiddoppelschicht mit eingebetteten Polypeptidmolekülen. * semipermeabel * aktiver Transport von außen nach innen (spezif. Permeasen) * ausschleusen von Proteinen (Exoenzyme, Exotoxine) nach außen * Sitz zahlreicher Enzyme für die Biosynthese von Zellwandstrukturelementen (+Ribosomen) Zellwand + Schutz des Protoplasten vor äußeren Noxen + Abbau der osmotischen Druckdifferenz + Formgebung der Zelle Mureinschicht: (verantw. für die Rigidität d. Zellwand): - Polysaccharidketten (abwechselnd N-Acetylmuraminsäure[MUR] und N-Acetylglucosamin [GLU]); Ketten sind durch Peptide miteinander verbunden. Grampos. Bakterien: bis 40 Mureinschichten; 30% der Trockenmasse der Zellwand. gramneg. Bakterien: 10% der Trockenmasse der Zellwand. Äußere Membran: (nur bei gramnegativen Bakterien vorhanden): "unit membrane" über Lipoproteine mit dem Murein verbunden. Die äußere Membran enthält Porinproteine, die Kanäle oder Poren bilden. Weiters ist an die äußere Membran das Lipopolysaccharid (LPS) angelagert, das auch als Endotoxin!!! bezeichnet wird (Lipid A Kernpolysacch.(Core) - O-spezifischen Ketten! Typisierung). Endotoxin stimuliert Makrophagen zur Produktion des endogenen, hitzestabilen Pyrogens Interleukin 1. 2 3 Kapseln: Schleim aus Polysacchariden: Schutz vor Phagocytose, lytischen Enzymen, Phagen, Antigenstruktur (K-Antigene; ca 80 Serotypen bei Pneumokokken). Geißeln: Beweglichkeit; Protein Flagellin; Geißelproteine sind gute Antigene (H-Antigen der Enterobakterien). Sie dienen zusammen mit dem O-Antigen (O-spez. Kette d. LPS) der Typisierung dieser Bakterien. Pili, Fimbrien, Glykokalix: oberflächliche Anhangsgebilde, die kürzer sind als Geißeln.Fimbrien und Pili sind zarte Proteinfäden, die für adhäsive Vorgänge (Kolonisierung von Schleimhäuten) verantwortlich sind (Adhäsine). Konjugationspili sind fädige Proteinhohlrohre, welche die Konjugation ermöglichen. Als Glykokalix werden Polysaccharidfäden bezeichnet, die das "Kleben" an Zellen oder glatten Oberflächen ermöglichen. Bakteriensporen: Dauerformen, die das bakterielle Genom bei "ungünstigen äußeren Bedingungen" schützen. Zytoplasmamembran stülpt sich ein, wächst um das Nukleoid herum, schnürt sich ab und bildet einer doppelwandige Endospore. Sporen weisen erhebliche Resistenzen gegenüber chemischen und physikalischen Noxen auf. 4 Physiologie: Bakterienstoffwechsel (Gesamtheit d. chemischen Reaktionen in der Bakterienzelle) - anabol oder synthetisch: endergonisch (unter Energieverbrauch) * photosynthetisch * chemosynthetisch Aus einfachsten Nährstoffen können Bakterien in kurzer Zeit hochkomplizierte organische Moleküle synthetisieren. Anwendung in der technischen Mikrobiologie: z.B. Gewinnung von Antibiotika, Aminosäuren, Vitaminen - katabol: exergonisch (liefern Energie durch Nährstoffabbau) * lithotroph = anorganische Nährstoffe * organotroph = organische Nährstoffe Humanpathogene Bakterien sind chemosynthetisch - organotroph! + Energiequelle in Form von oxidierbaren organischen Substraten + C- und N-Quellen zur Synthese zahlreicher organischer Verbindungen + Mineralien (P, Ca, Mg..) als Aktivatoren von Enzymen + organische Verbindungen, die Bakterien nicht selbst synthetisieren Als Nährstoffe kommen praktisch alle in der Natur vorkommenden organischen Stoffe in Frage. Die Verarbeitung dieser Stoffe erfolgt über eine vielfältige Reihe enzymatischer Prozesse, die in 4 Phasen abläuft: 1) Verdauung: Spaltung organischer Energiequellen außerhalb der Zelle durch Exoenzyme (manchmal wichtige Pathogenitätsfaktoren!). 2) Aufnahme niedermolekularer Nährstoffe durch passive Diffusion oder aktiven Transport. 3) Vorbereitung zur Oxidation: z.B. Abspaltung von Carboxyl- oder Aminogruppen, Phosphorilierung... 4) Oxidation: Entzug von Elektronen und H2-Ionen. Je nach H2-Akzeptor unterscheidet man die Respiration oder Atmung: H2-Akzeptor ist der Sauerstoff anaerobe Respiration: H2-Akzeptor ist Sauerstoff als Bestandteil eines anorganischen Salzes Fermentation oder Gärung: H2-Akzeptor ist organische Verbindung 5 6 CHEMOTHERAPEUTIKA: chemisch-synthetisch hergestellte, antimikrobiell wirksame Substanzen, wie z.B. Sulfonamide ANTIBIOTIKA: biosynthetisch gewonnene, antimikrobiell wirksame Naturstoffe, wie z.B. Penicillin BAKTERIOSTASE: reversible antibiotische Hemmung des Wachstums bzw. der Vermehrung einer Bakterienpopulation z.B. Sulfonamide, Tetracycline... BAKTERIZIDIE: irreversible Schädigung und Abtötung einer Bakterienpopulation z.B. Penicilline, Cephalosporine... 7 Resistenz Bakterielle Eigenschaft, Antibiotikakonzentrationen, die im Makroorganismus erreicht werden können, zu tolerieren („klinische Resistenz“)! 1. natürliche Resistenz: stets vorhandene Unempfindlichkeit, d.h. Lücke im Wirkungsspektrum des Antibiotikums 2. erworbene (chromosomale) Resistenz (primär oder sekundär): Mutation im Chromosom lokalisiertere Gene; nur unter Selektionsdruck kann sich eine resistente Population entwickeln! 3. extrachromosomale ("infektiöse") Resistenz: extrachromosomale Gene als Träger von Resistenzfaktoren (Plasmide) Resistenzeigenschaften können durch parasexuelle Prozesse übertragen werden: + Konjugation: Übertragung von DNA über Plasmabrücken + Transformation: Übertragung von DNA von lysierten Zellen auf spezifische Akzeptoren + Transduktion: Übertragung von Bakterien-DNA durch Phagen (versehentliches "Miteinpacken" von Bakterien-DNA) 8 Veränderung des Arzneimittelrezeptors Antibiotika haben verschiedene Angriffspunkte in der Bakterienzelle. Wird durch Mutation die Struktur dieser Angriffspunkte verändert, so kann das Antibiotikum keine Bindung mehr eingehen und wird wirkungslos. Beispiel: Streptomycin-Resistenz: beruht auf einer Veränderung der 30-S-Ribosomen-Untereinheiten Veränderung der Penetration des Antibiotikums Bevor der Wirkstoff seinen Rezeptor erreicht, muss er durch die Zellwand penetrieren. Durch Veränderungen im aktiven Transportgeschehen oder durch eine herabgesetzte Permeabilität der äußeren Membran kann das Antibiotikum nicht mehr in die Bakterienzelle gelangen. Inaktivierung des Antibiotikums Je nach Antibiotikum sind unterschiedliche Enzyme dafür verantwortlich. Beispiel: β-Lactamasen: bewirken hydrolytische Spaltung des β-Lactam-Rings von Penicillinen und Cephalosporinen Resistenzmechanismen Inaktivierende Enzyme: Hydrolyse oder Modifikation des Antibiotikums z.B. Betalactamase (hydrolysiert Betalactamring) Resistente Zielmoleküle: Durch Mutation werden Gen-Produkte gebildet, die eine geringere Affinität zum Antibiotikum aufweisen. Permeabilitätsmechanismen: Reduzierter Influx bzw Efflux 9 Chemotherapeutika: Antimikrobielle Wirkstoffe! * Wirkungsspektrum: (natürliche Resistenz) Schmalspektrum - Breitspektrum bakteriostatisch - bakterizid * Wirkungsweise: * Wirkungsmechanismen (Pharmakodynamik): Angriffspunkt ist Zellwand, Zytoplasmamembran oder Proteinsynthese * Pharmakokinetik: Resorption, Bindung an Serumeiweiß, Verteilung, Gewebsdiffusion, Umbau, Abbau, Metabolisierung und Ausscheidung * chemisch-physikalische Eigenschaften pH-Optimum, Stabilität, Löslichkeit * Nebenerscheinungen Toxizität, Allergie, Eliminierung der Normalflora * Resistenzlage Virulenzfaktoren + als Strukturelemente der Bakterienzelle (nicht toxisch) + als Stoffwechselprodukte (extrazellulär bzw. toxisch) Biologische Funktion der Virulenzfaktoren - Adhäsion: zur Kolonisation mittels wirtspezifischer Adhäsine (z.B. Fimbrien, Pili) - Invasion/Ausbreitung: gewebsschädigende Exoenzyme (z.B. Streptokinase, Hyaluronidase, Kollagenase, Proteasen...) - Toxine: Endotoxine (werden bei Zelltod frei; z.B. LPS) Exotoxine (Eiweißstoffe, die von Bakterium nach Außen abgegeben werden) Zytotoxine, Neurotoxine, Enterotoxine 10 11 Strategien gegen Infektabwehr des Wirtes: - Antiphagocytose: Kapseln, Phagocytentoxine ... - Immuntoleranz: Molekulare Mimikry (das Immunsystem erkennt Bakterien nicht als fremd) - Antigenvariation: Variabilität der Antigenproteine (z.B. Pili..) - IgA-Proteasen: Bakterien zerstören spez. Antikörper Epidemiologie Lehre über Ursache, Entstehung und Verbreitung von Krankheiten! Infektionskette: a) Infektionsquelle: primäre Qu. (Ort, an dem sich Erreger aufhält oder vermehrt; Mensch, Tier=Zoonosen), Inkubationsausscheider, Rekonvaleszenzausscheider, Dauerausscheider sekundäre Quellen (Wasser, Boden, Luft) b) Übertragungsweg: Tröpfcheninfektion (z.B. Erkältungskrankheiten) Kontakt- und Schmierinfektion (z.B. Geschlechtskrankheiten) c) empfindliches Individuum: Eigenschaften der Erregers (z.B. Virulenz) und des Makroorganismus (z.B. Abwehrvermögen) 12 13 14 15 16 Züchtung oder Kultivierung von Bakterien Bakterien außerhalb ihres natürlichen Standortes zur Vermehrung bringen. Inokulation: Verbringung bakterienhältigen Materials in ein Kulturmedium Inkubation: "Bebrütung" der beimpften Kulturmedien Kultur: die durch Vermehrung entstandene Bakterienpopulation flüssige Kulturmedien: Nährbouillon (Fleischextrakt, Pepton, Glucose) feste Kulturmedien: Nährbouillon + 2% Agar (Polysaccharid aus Seetang) - Minimalmedium: "Existenzminimum" - Optimalmedium: Substrate im Überfluss - Selektivmedium: selektiv für einzelne Keimgruppen wachstumshemmend; zur Anreicherung "interessanter" Keime um sie von Begleitflora zu trennen - Differentialmedium: enthalten Stoffe, welche von einzelnen Bakterienarten metabolisiert werden --> Stoffwechselprodukte werden z.B. durch Farbindikatoren angezeigt ("Bunte Reihe") Direkter Nachweis von Bakterien oder deren Produkten * Mikroskop: nativ - Einfachfärbungen - Differentialfärbungen Form- und Größe der Zellen, Flagellen, Kapseln, Sporen usw., Pseudozellverbände, Färbeverhalten * Kultivierung: auf festen und flüssigen Nährmedien - Makroskopisch-morphologische Merkmale der Kolonien Physiologische Merkmale - Wachstumsbedingungen (t°C, pH, pO2, pCO2, osmot.Druck, Nährstoffe,Mineralien ) - Stoffwechseleigenschaften (Verwertung von C- und N-Quellen, Nachweis von Stoffwechselprodukten und Enzymen) - Chemische Merkmale (DNA-Struktur, Antigen-Struktur) 17 • Schnelltest zur Unterscheidung von • Staphylokokken positiv und Streptokokken negativ • Durchführung: Bakterienkolonie wird mit einem Tropfen 3%iger H2O2-Lösung beträufelt. Aufsteigende Gasblasen zeigen die Anwesenheit des Atmungskettenenzyms Katalase an. 18 • Schnelltest zur Unterscheidung von: • Staphylococcus aureus ! positiv Staph. ! negativ Staph. epidermidis • Durchführung: Bakterienkolonie wird auf einen Objektträger aufgebracht und mit einem Tropfen Latexsuspension verrührt. Die Latexteilchen sind mit Humanfibrinogen und IgG beschichtet. Bei positiver Reaktion kommt es zur Klumpenbildung. Prinzip: Zur Agglutination kommt es durch Bindung des IgG an das an der Zelloberfläche von Staph. Staph. aureusaureus-Stämmen lokalisierte Protein A und durch den ClumpingClumping-Faktor, Faktor, der mit Fibrinogen reagiert. BUNTE REIHE Identifizierung von Enterobacteriaceae Kligler Dextrose Lactose H2SBildung Zuckerspaltung Indol Harnstoff Citrat Nitrat Beweglichkeit Glucose Tryptophan Harnstoff Kohlenstoff- Nitrat Lactose zu Ammonium- quelle ! Saccarose carbonat Nitrit beweglich unbeweglich 19 BUNTE REIHE Farbumschläge bei positiven Reaktionen und Zusatz von Reagenzien Harnstoffreagenz: Indolreagenz: Phenolphtalein p-Dimethylaminobenzaldahyd Nitratreagenzien: Sulfanilsäure α-Naphthylamin Essigsäure 20 Das Testsystem beruht auf dem Prinzip der Bunten Reihe : In einem Teststreifen mit 20 Mikroröhrchen befinden sich verschiedene dehydrierte Testsubstanzen, die mit einer Bakteriensuspension in Aqua dest. befüllt werden. Der Test wird anschließend bei 37°C ca. 24 Std. bebrütet. Ein meist indikatorbedingter Farbumschlag zeigt an, ob die getesteten Substanzen von Bakterien umgesetzt wurden. Anhand der positiven Reaktionen lässt sich ein Zahlencode erstellen, der zur Identifizierung der Keime führt. + + + QNPG ADH LDC 5 + + + ODC ‚CIT H2S URE TDA IND 1 4 VP + + GEL GLU MAN IND 4 + SOR RHA SAC MEL AMY ARA OX 5 2 1 Kodierungsprinzip des API-Systems z.B.: Escherichia coli Gelbe Seite : Anreicherungsmedium für alle Bakterien Rote Seite: Selektivmedium für gram-neg. Bakterien Weiße Seite: Selektivmedium für Enterokokken Häufigste Erreger bakterieller Harnwegsinfektionen: akute Infektionen, nicht hospitalisierte Patienten Escherichia coli chronische Infektionen hospitalisierte, kathederisierte Patienten Proteus, Pseudomonaden, Klebsiella Enterobacter, Enterococci, Staphylococci 21 22











