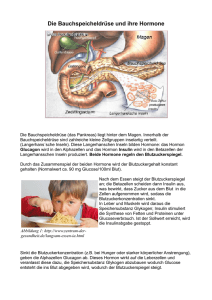
Biologische Aktivität verschiedener Insulinderivate in
Werbung

Hoppe-Seyler'S Z. Physiol. Chem. Bd. 356, S. 647 - 651, Juni 1975 Biologische Aktivität verschiedener Insulinderivate in vivo und in vitro Klaus Rager und Ulrike Buss (Der Schriftleitung zugegangen am 9. Januar 1975) Herrn Prof. Dr. Dr. G. Weitzel zum 60. Geburtstag gewidmet Zusammenfassung: Die Aktivität von Des-octapeptid-insulin, Des-AsnA21-des-AlaB30-insulin, Des-GlyA1 -des-PheBMnsulin und Trimethionylinsulin wurde in vitro und in vivo untersucht. Gemessen wurde in vitro am isolierten Zwerchfell der Ratte der Glucose-Schwund im Inkubationsmedium und der Glucose-Einbau in das Glykogen des Zwerchfells sowie die antilipolytische Aktivität an der isolierten Fettzelle. In vivo wurde der Einbau von [U-14C]Glucose nach intraperitonealer Injektion in das Glykogen des Zwerchfells und des Nebenhodenfettgewebes sowie der Einbau von 14C aus [U-14C]Glucose in die Lipide des Nebenhodenfettgewebes der Ratte gemessen. Im Vergleich zu Rinderinsulin zeigte Des-octapeptid-insulin mit den angewandten Untersuchungsmethoden eine biologische Aktivität von 0.5 -1.0%, Des-AsnA21-des-AlaB30-insulin von 1.4 - 3.5%, Des-GlyA1-des-PheB^insulin von 2.1 - 5.9% und Trimethionylinsulin von 14.0 31.5%. Die untersuchten Insulinderivate zeigten in vitro und in vivo eine gute Übereinstimmung der biologischen Aktivität. Zusammen mit früheren Untersuchungen ergibt sich eine umfassende Charakterisierung der biologischen Aktivität für diese Insulin derivate. Biological Activity in vitro and in vivo of Different Insulin Derivatives Summary: The biological activities of des-octapeptide-insulin, des-AsnA21-des-AlaB30-insulin, des-GlyA1-des-PheB ^insulin and trimethionylinsulin were studied in vitro and in vivo. In vitro we measured, using the isolated diaphragm of the rat, the disappearance rate of glucose in the incubation medium, the incorporation of glucose into the glycogen of the diaphragm and the antilipolytic activity in the isolated fat cell model. The incorporation of [U-14C]glucose after intraperitoneal injection into the glycogen of the diaphragm and the fat pad tissue was studied in vivo, as well as the incorporation of 14 C from [U-14C]glucose into the lipids of the fat pad tissue of the rat. In comparison to bovine insulin, des-octapeptideinsulin showed, with the methods used, a biological activity,of 0.5 - 1.0%, des-AsnA21-des-AlaB30-insulin 1.4 - 3.5%, des-GlyA1-des-PheB1- Postanschrift: Dr. K. Rager, Abteilung für Endokrinologische Laboratoriumsdiagnostik der Univ.-Kinderklinik, D-74 Tübingen, Rümelinstr. 23. Enzym: Glucose-Oxidase, |3-D-Glucose:Sauerstoff-l-Oxidoreduktase (EC 1.1.3.4). Unauthenticated Download Date | 5/11/16 8:26 PM 648 K. Rager und U. Buss Bd. 356(1975) insulin 2.1 - 5.9% and trimethionylinsulin 14.0-31.5%. The studied insulin derivatives compared well in their activities in vitro and in vivo. Together with earlier studies, a good characterization of the biological activities of these four insulin derivatives has now been achieved. In einer früheren Untersuchung11 wurde die Aktivität von Des-octapeptidB23' -insulin, Des-AsnA21-des-AlaB30-insulin, Des-GlyA1-des-PheB1insulinund7VA1,7VB1,JVB29-Trimethionyl-insulin in verschiedenen In-vitro-Testsund immunologisch. untersucht. In der vorliegenden Arbeit werden diese In-vitro-Ergebnisse ergänzt und ein Vergleich zu der In-vivo-Aktivität dieser Insulinderivate unternommen. Die Untersuchung chemisch abgewandelter Insulinderivate ergibt die Möglichkeit, zwischen Struktur und Wirkung des Insulinmoleküls Beziehungen zu erkennen. 2) In-vivo-Untersuchungen Die Durchführung der Versuche erfolgte in Anlehnung an Rafaelsenl 6 ' 7 'wie l.c.l8^ beschrieben. Nach intraperitonealer Injektion von NaCl, Rinderinsulin oder den untersuchten Insulinderivaten zusammen mit [U-l4C]Glucose bei der Ratte wurde der Einbau von [ l4C]Glucose in das Glykogen des Zwerchfells und des Nebenhodenfettkörpers sowie der Einbau von 14C in die Lipide des Nebenhodenfettkörpers bestimmt. Rinderinsulin steigerte den Einbau von [U-14C]Glucose in das Glykogen des Zwerchfells in einer Dosierung von 400 ng/100 g Körpergewicht um das 3.2 bis 3.9fache, in das Glykogen des Nebenhodenfettgewebes um das 2.1- bis 3.3fache und den Einbau von 14C in die Lipide des Nebenhodenfettgewebes um das 9- bis 11 fache im Vergleich zu den Kontrollen ohne Insulinzugabe. Durchschnittlich 64% des wiedergefundenen 14C fanden sich im Glykogen des Zwerchfells, 12% im Glykogen des Nebenhodenfettgewebes und 37% in den Lipiden des Nebenhodenfettkörpers nach maximaler Insulinzugabe. Material und Methoden Rinderinsulin, kristallin, 27 /mg (Fa. Hoechst). Desoctapeptidinsulin, Des-AsnA21-des-AlaB30-insulin, Des-GlyA1-des-PheBl-insulin und Trimethionylinsulin wurden von Prof. F. H. Carpenter, University of California, Berkeley, zur Verfugung gestellt. Bestimmung der Insulinaktivitäten 1) In-vitro-Untersuchungen a) Glucose-Schwund aus dem Inkubationsmedium am Diaphragma der Ratte. Gewinnung und Verwendung der Diaphragmen sowie Pufferlösungen nach l.cJ2J. Bestimmung der Glucosekonzentration mit Glucose-Oxidase (Boehringer-Test). Rinderinsulin bewirkte in maximaler Dosierung eine 3.4 - S.Ofache Steigerung des Glucoseschwundes des Basiswertes ohne Insulinzugabe. b) GlykogenbeStimmung: Aus dem gleichen Ansatz, in dem der Glucoseschwund im Inkubationsmedium gemessen wurde (s. oben), wurde die Glykogenkonzentration im Zwerchfell gemessen. Durchführung des Tests wie l.cJ3'4!, Messung des Glykogens nach der Anthronmethodel5!. Der Basiswert konnte durch Rinderinsulin in der maximal verwendeten Konzentration von /m/ Inkubationsmedium um das 2.8 - 4.6fache in verschiedenen Testansätzen gesteigert werden. c) Antilipolytische Aktivität: Gemessen wurde die Hemmung der Adrenalin-induzierten Lipolyse an isolierten Fettzellen durch Bestimmung der Konzentration der freien Fettsäuren wie l.cJ1>2^ beschrieben. Die Adrenalin-induzierte Lipolyse ohne Rinderinsulinzugabe war um das 10- bis 15fache höher als die Ergebnisse bei Zugabe von 50 Rinderinsulin/m/ Inkubationslösung. Ergebnisse In-vitro-Untersuchungen (Tab. 1) Des-octapeptid-insulin zeigte eine Aktivität von knapp l % in den hier angewandten biologischen In-vitro-Tests. Es zeigte sich kein signifikanter Unterschied in der Wirksamkeit am Zwerchfell der Ratte bei der Messung der Glykogensynthese im Zwerchfell und dem Glucoseschwund aus dem Inkubationsmedium einerseits und der antilipolytischen Aktivität an isolierten Fettzellen andererseits. Des-AsnA21-des-AlaB30-insulin zeigte eine durchschnittliche biologische Aktivität von 2.0 - 3.5% in den angewandten In-vitro-Testverfahren. Des-GlyA1-des-PheB1-insulin zeigte eine Aktivität von durchschnittlich 5%; Die biologische Aktivität von Trimethionylinsulin betrug am Rattenzwerchfell 28 - 31 %, während die antilipolytische Aktivität 14% betrug. In-vivo-Untersuchungen (Tab. 2) Die Wirkung der untersuchten Insulinderivate in vivo nach intraperitonealer Injektion auf den Einbau von markierter Glucose in das Glykogen des Unauthenticated Download Date | 5/11/16 8:26 PM 649 Aktivität verschiedener Insulinderivate Bd. 356 (1975) Zwerchfells und das Glykogen des Rattennebenhodenfettgewebes sowie der Inkorporation von 14 C aus [U-14C]Glucose in die Lipide des Rattennebenhodenfettgewebes zeigte eine sehr gute Übereinstimmung mit den In-vitro-Befunden. Die biologische Aktivität von Des-octapeptid-insulin, Des-AsnA21-des-AlaB30-insulin und Des-GlyAl-des-PheBl-insulin fand sich im selben Bereich wie bei den In-vitro-Befunden, während Trimethionylinsulin in vivo nur eine biologische Aktivität von 14 - 18% zeigte, im Vergleich zu Rinderinsulin. Diskussion 1) Die vorliegende Arbeit zeigt, daß die früher festgestellten Ergebnisse für die In-vitro-Aktivität der untersuchten Insulin-Derivate^1'9' überraschend mit den Befunden der In-vivo-Aktivität übereinstimmen. In verschiedenen Untersuchungen110"15' konnte gezeigt werden, daß die bio- logische Wirksamkeit verschiedener Insulinderivate weitgehend mit der Konformation des Insulinmoleküls (gemessen mit Circulardichroismus) parallel geht. Tritt eine deutliche Änderung in der Konformation ein, wie bei Des-octapeptidinsulin, so geht dies mit einem weitgehenden biologischen Wirkungsverlust einher. Ähnliche Konformationsänderungen finden sich bei Entfernung der endständigen Aminosäure des Carboxylendes der -Kette und Entfernung der./Vterminalen Aminosäure der -Kette, während am Af-terminalen Ende der B-Kette der Verlust einer Aminosäure (Phe) keinen Effekt auf die biologische Wirksamkeit und den Circulardichroismus hat. Lediglich Trimethionylinsulin hatte eine geringere Aktivität bei den hier angewandten biologischen In-vivo-Testverfahren. Die Unterschiede waren jedoch nicht statistisch signifikant (p = 0.01). Auffallend ist auch, daß Trimethionylinsulin im Mäusefalltest1161 eine Aktivität von 34% zeigte[1]. Tab. 1. In-vitro-Wirkung der Insulinderivate: a) auf die Glykogenbüdung des Rattenzwerchfells; b) auf den Glucose seh wund aus dem Inkubationsmedium bei Inkubation des Rattenzwerchfells. c) Antilipolytische Wirkung; Messung der Konzentration an freien Fettsäuren im Inkubationsmedium nach Stimulierung der Lipolyse durch Adrenalin. Die Wirkung des Rinderinsulins wurde gleich 100% gesetzt. n Insulinkonzentrat [ng/m/ Inkub.] Aktivität [%] ± 1SD Des-octapeptid-insulin 15 Des-AsnA21-des-AlaB30-insulin Des-GlyA1-des-PheB ^insulin 15 14 500 160 0.5 ± 0.09 3.5 ±0.19 Trimethionylinsulin 15 Des-octapeptid-insulin Des-AsnA21-des-AlaB30-insuün Des-GlyA ^des-Phe8 * -insulin 22 Insulinderivat a) b) Trimethionylinsulin c) 25 24 18 Des-octapep tid-insulin Des-AsnA2 1-des-AlaB30-insulin Des-GlyA1-des-PheB ^insulin 22 Trimethionylinsulin 24 23 21 100 20 28 5.1 ± 1.0 500 160 100 20 0.7 ± 0.14 2.0 ± 0.44 5.9 ± 1.17 31.5 ±5.5 500 160 200 2 0.9 ± 0.03 2.4 ± 0.18 3.2 ± 0.50 ± 4.3 14.0 ± 0.90 Unauthenticated Download Date | 5/11/16 8:26 PM 650 K. Rager und U. Buss Bd. 356 (1975) Tab. 2. Wirkung der Insulinderivate in vivo: a) auf die Inkorporation von [U-14C]Glucose in das Glykogen des Rattenzwerchfells; b) auf die Inkorporationvon 14C aus [U-14C]Glucose in die Lipide des Rattennebenhodenfettgevvebes; c) auf die Inkorporation von [U-14C]Glucose in das Glykogen des Rattennebenhodenfettkörpers. Die Wirkung des Rinderinsulins wurde gleich 100% gesetzt. n Insulinkonzentrat [ng/Tier] Aktivität [%] ± 1 SD Des-octapeptid-insulin Des-AsnA21-des-AlaB30-insulin 9 8 800 160 0.8 ± 0.19 1.5 ± 0.7 Des-GlyA 1 -des-PheB1 -insulin 9 160 Tr ime thio ny 1 in sulin 7 40 Des-octapeptid-insulin Des-AsnA21-des-AlaB30-insulin Des-GlyA ^des-Phe8 * -insuhn Trimethionylinsuh'n 9 14 12 10 800 160 160 40 3.4 ± 1.59 16.6 ± 2.70 Des-octapeptid-insulin Des-AsnA21-des-AlaB30-insulin Des-GlyA ^des-Phe8 ^insulin Trimethionylinsulin 9 10 12 11 800 160 160 40 0.8 ± 0 . 3 2 1.8± 0.43 2.7 ± 0.67 18.0 ± 3.41 Insulinderivat a) b) c) 2.1 ± 0.9 14.5 ± 5.4 1.0 ± 0.24 2.4 ± 1.32 4) Das Fehlen der W-terminalen Aminosäuren GlyA1 und PheB1 führt zu einem weitgehenden Wirkungsverlust dieses Insulin de rivats. Wie aus den Untersuchungen an Hybridinsulinen hervorgeht1221, ist GlyA1 für die biologische Aktivität wesentlich. Dieses ist in kristallinem Zustand an der Oberfläche des Insulinmoleküls lokalisiert^231, so daß die Bedeutung dieser Aminosäure mit ihrer Lokalisation im Insulinmolekül parallel gehen könnte, da in der Literatur^101 Anzeichen dafür vorliegen, daß die Konformation des Insulinmoleküls in Lösung ähnlich der Kristallkonfor3) Aus der Literatur1191 ist bekannt, daß AlaB3° mation ist. für die Aktivität des Insulins nicht essentiell ist. Dagegen kann Phe31 ohne Wirkungsverlust entDes-AsnA21-des-AlaB30-insulin zeigt einen prakfernt werden^24'251. tisch vollständigen Wirkungsverlust, wie aus un1 seren Befunden und dem Schrifttum hervorgeht^ . 5) Die Maskierung der freien Aminogruppen mit Methionin in AI, B l und B29 fuhrt zu einem Die Desamidierung von AsnA21 führt .nur zu geringem Wirkungsverlust120'211. Aus diesen BefunWirkungsverlust, der jedoch nicht so weitgehend A21 den könnte man vermuten, daß Asp für die ist wie bei den anderen untersuchten InsulinderiInsulinaktivität notwendig ist. Nach Abtrennung vaten. A^-Ac-insulin1261 und WA1-(3-Carboxyvon AsnA21 auftretende Konformationsänderunpropionyl)insulin (A^-Suc-insulin/121 zeigen eine deutliche Minderung der biologischen Aktigen[121 gehen mit dieser Beobachtung parallel. 2) Die Abspaltung der letzten 8 Aminosäurereste der B-Kette (B 23 - B 30) führt zu einem fast vollständigen Aktivitätsverlust. Wie aus der Literatur hervorgeht, ist ArgB22 wesentlich für die Wirkung des Insulins^ 17>18 Die Abspaltung der letzten 3 Aminosäuren bewirkt dagegen eine geringe Minderung der biologischen Aktivität141, während die Entfernung der 5 endständigen Aminosäuren der B-Kette mit einer Veränderung der biologischen Aktivität und des Circulardichroismus einhergeht110>121. Unauthenticated Download Date | 5/11/16 8:26 PM Bd. 356(1975) Aktivität verschiedener Insulinderivate vität, während die Einführung der Acetyl- oder 3-Carboxypropionyl-Gruppe in B l oder B 29 weniger stark die biologische Aktivität minderten. So wäre es möglich, daß die Einführung der Methioningruppe in AI den Wirkungsverlust des Trimethionylinsulins im Vergleich zu Rinderinsulin verursacht. Literatur 1 Rager, K., Kemmler, W. & Schauder, P. (1969) diese Z. 350,717-720. 2 Weitzel, G., Renner, R. & Guglielmi, H. (1971) diese Z. 352, 1617-1630. 3 Weitzel, G., Renner, R., Kemmler, W. & Rager, K. (1912) diese Z. 353,980-986. 4 Weitzel, G., Renner, R., Guglielmi, H. (1972) diese Z. 353,535-539. 5 Seiter, S., Dayton, S., Novic, B. & Muntwyler, E. (l95Q)Arch. Biochem. 25,191 - 200. 6 Rafaelsen, O. J., Lauris, V. & Renold, A.E. (1965) Diabetes 14, 19-24. 7 Rafaelsen, 0. J. (1964) Acta Physiol. Scand. 61, 314-322. 8 Rager, K. (1973) Res. Exp. Med. 160, 96 - 99. 9 Carpenter, F. H. & Baum, W.E. (1962) /. Biol Chem. 237,409-411. 10 Brandenburg, D., Busse, W.-D., Gattner, H.-G., Zahn, H., Wollmer, A., Gliemann, J. & Puls, W. (1972) Proc. 12. Eur. Peptide Symp. Reinhardsbrunn, DDR, (Hanson, H. & Jakubke, H. D., Hrsg.) S. 270 - 283, North-Holland Publ. Co., Amsterdam. 11 Brandenburg, D., Gattner, H.-G., Weinert, M., Herbertz, L., Zahn, J. & Wollmer, A. (1970) Diabetes, 651 Proc. 7th Congr. Int. Diabetes Federation, Buenos Aires, (Rodriguez, R. R. & Vallence-Owen, J., Hrsg.) S. 363-377, Int. Congress Series 231, Excerpta Medica Foundation, Amsterdam. 12 Gliemann, J., & Gammeltoft, S. (1974) Diabetologia 10,105-113. 13 Freychet, P., Roth, J. & Nevüle, D. M. (1971) Proc. Nat. Acad. Sei. U.S.A. 68,1833 -1837. 14 Katsoyannis, P. G., Zahnt, C., Harris, A., & Meyer, R. J. (1971) Biochemistry 10, 3884 - 3889. 15 Weitzel, G., Eisele, K., Zöllner, H. & Weber, U. (1969) diese Z. 350, 1480 -1483. 16 Young, D. M. & Lewis, A. H. (1947) Science 105, 368 - 369. 17 Bünzli, H. F. & Bosshard, H. R. (1971) diese Z. 352, 1180-1182. 18 Weitzel, G., Weber, U., Martin, J. & Eisele, K. (1971) diese Z. 352,1005-1013. 19 Slobin, L. I. & Carpenter, F. H. (1963) Biochemistry 2,16-21. 20 Slobin, L. I. & Carpenter, F. H. (1963) Biochemistry 2,22-27. 1l Slobin, L. I. & Carpenter, F. H. (1970) Diabetologia 6,499-505. 22 Weber, U., Schneider, F., Köhler, P. & Weitzel, G. (1967) diese Z. 348,947-952. 23 Blundell, T. L., Dodson, G. G., Dodson, E., Hodgkin, D. C. & Vijayan, M. (1971) Recent Prog. Horm. Res. 27, l - 34. 24 Brandenburg, D. (1969) diese Z. 350, 741 - 750. 25 Weber, U. & Weitzel, G. (1968) diese Z. 349, 1431-1434. 26 Brandenburg, D., Gattner, H.-G. & Wollmer, A. (1972) diese Z. 353,599-617. Unauthenticated Download Date | 5/11/16 8:26 PM Unauthenticated Download Date | 5/11/16 8:26 PM