Plasmolyse und Deplasmolyse
Werbung

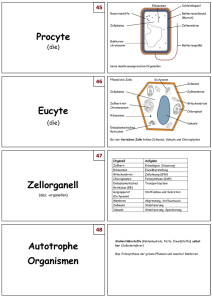
14.11.04 Protokoll über den Versuch vom 1.Kurstag dem 03.11.04 Plasmolyse und Deplasmolyse Einleitung: Unser Versuchsobjekt für diesen Tag war Allium cepa – die Küchenzwiebel. Zu aller erst fertigten wir einen möglichst dünnen Schnitt der Blattunterseite der Küchenzwiebel an um uns die Epidermiszellen von Allium cepa unter dem Mikroskop zu betrachten. Die prallen Vakuolen waren gut sichtbar, denn sie sind u.a. gefüllt mit Anthocyanen, die sie rot erscheinen lassen. Als nächstes machten wir uns mit den Vorgängen der Plasmolyse und Deplasmolyse vertraut. Die die Vakuole umgebende Membran – der Tonoplast – ist semipermeabel, d.h. sie ist für das Lösungsmittel (bspw. Wasser) jedoch nicht für die darin gelösten Stoffe (z.B. Saccharose) durchlässig. Gase und auch gelöste Stoffe haben immer das Bestreben sich gleichmäßig in einem Raum zu verteilen. Dieses bezeichnet man als Diffusion. Die Diffusion durch eine semipermeable Membran, wie die der Vakuole, bezeichnet man als Osmose. In der Vakuole befindet sich jedoch nicht nur Wasser, sondern auch gelöste Salze. Diese Salze sind osmotisch aktiv, das bedeutet, sie bauen ein osmotisches Potential () auf, das in MPa (Mega-Pascal) gemessen wird. Das osmotische Potential gibt an, wie stark die in der Vakuole enthaltene Lösung (mit den darin enthaltenen Salzen) Wasser (mit dem osmotischen Potential = 0) außerhalb der Vakuole „einsaugt“ um einen Konzentrationsausgleich zu schaffen. Dieses „Einsaugen“ von Wasser lässt die Vakuole prall werden und einen Druck auf die Zellwand ausüben, diesen Druck (, der die Pflanze überhaupt erst zum stehen bringt) bezeichnet man als Turgordruck oder Druckpotential (p). Ist in einer Lösung das Druckpotential p= 0, so ist das osmotische Potential gleich dem Wasserpotential (auch: dem osmotischen Potential von Wasser) w. Ist jedoch in der Vakuole p= 0, lastet kein Druck auf der Zellwand und die Zellmembran beginnt sich von der Zellwand zu lösen. Diesen Ablösungsvorgang bezeichnet man als Plasmolyse. Wir konnten ihn beobachten, als wir einen Tropfen einer 1,0 M KNO3 –Lösung unter dem Deckglas hindurchzogen, wo er mit unserer Epidermisschicht von Allium cepa in Berührung kam. Dieser Vorgang ist reversibel, d.h. als wir anschließend einen Tropfen Wasser hinzugaben begannen die Vakuolen dieses Wasser aufzunehmen und würden wieder prall. Diesen zweiten Vorgang bezeichnet man wiederum als Deplasmolyse, er ist einfach die Umkehrung der Plasmolyse. Material und Methoden: Als wir uns die Vorgänge der Plasmolyse und Deplasmolyse vergegenwärtigt hatten, kamen wir dann zu unserem eigentlichen Versuch. Wir versuchten mit Hilfe der Grenzplasmolyse das osmotische Potential der von uns eingesetzten Saccharose-Lösung zu bestimmten, genauer: wir versuchten die Konzentration der Saccharose-Lösung zu ermitteln, bei der 50% der von uns betrachteten Zellen Plasmolyse zeigen. Wir legten also einige Stückchen der Zwiebelblattepidermis von Allium cepa in Zuckerlösung der Konzentrationen 0,1 ; 0,15 ; 0,2 ; 0,25 ; 0,3 ; 0,35 ; 0,4 ; 0,45 ; 0,5 ; 0,55 bzw. 0,6 M und zählten nach einer 20 minütigen Einwirkzeit insgesamt 50 Zellen und versuchten zu bestimmten, bei wie viel Prozent Plasmolyse stattgefunden hatte. Ergebnisse: Dieser Versuch wurde an 4 Tischen durchgeführt, wobei folgende Ergebnisse bzw. folgende Mittelwerte herauskamen: Tisch 1 Tisch 2 Tisch 3 Tisch 4 Mittelwerte 0,1 0% 0% 0% 0% 0% 0,15 0% 0% 0% 0% 0% 0,2 0% 0% 0% 0% 0% 0,25 0% 12% 0% 0% 3% 0,3 0% 15% 0% 0% 3,8% 0,35 0% 20% 0% 0% 5% 0,4 0% 2% 0% 0% 0,5% 0,45 3% 0% 5% 50% 14,5% 0,5 40% 100% 90% 62% 73% 0,55 95% 100% 92% 81% 92% 0,6 98% 95% 95% 99% 83% 120% 100% Tisch 1 Prozent 80% Tisch 2 60% Tisch 3 Tisch 4 40% Mittelwerte 20% 0, 6 0, 5 0, 4 0, 3 0, 2 0, 1 0% Konzentration 100% 90% 80% 70% 60% 50% 40% 30% 20% 10% 0% 0, 6 0, 5 0, 4 0, 3 Mittelwerte 0, 2 0, 1 Prozent Mittelwerte Konzentration Aus diesen Werten ergibt sich, dass bei einer Konzentration von 0,48 M 50% der beobachteten Zellen Plasmolyse aufweisen. Um nun das osmotische Potential zu berechnen, benötigt man folgende Gleichung: = - c * R * T c = Konzentration der Lösung in kmol/m3 T = absolute Temperatur (237 + x °C) R = Gaskonstante (8,314 J/mol * K) In unserem Fall würde die Rechnung für eine Konzentration von 0,48 M und einer geschätzten Raumtemperatur von 22°C also wie folgt lauten: = - 0,48 kmol/m3 * 8314 J/kmol K * 295 K = - 1,177 MPa Das osmotische Potential der Saccharose-Lösung mit einer Konzentration von 0,48 M beträgt also – 1,177 MPa. Diskussion: Dieses Ergebnis ist, vor allem, wenn man das Rechenbeispiel im Praktikumsscript („Struktur und Funktion der Organismen“, Praktikum WS 2004/2005) betrachtet, gar nicht so unwahrscheinlich. Dennoch wäre noch einmal über die Diskrepanz der Ergebnisse der einzelnen Tische bei gleichen Konzentrationen nachzudenken. Zu erwarten wäre gewesen, dass die Ergebnisse der einzelnen Tische bzw. Versuchsgruppen sich deutlich ähnlicher sind bzw. dass es nicht so einen Sprunghaften Anstieg in den Prozentzahlen der Zellen, bei denen Plasmolyse aufgetreten ist, gibt. Vor allem sollte es ja eigentlich nicht möglich sein, dass man ab einer bestimmten Konzentration Zellen mit Plasmolyse bemerkt, dann jedoch, bei einer höheren (!) Konzentration wieder 0% der Zellen Plasmolyse aufweisen. Leider sind keine Erfahrungswerte aus früheren Kursen bekannt, möglicherweise kommen diese auf ein ähnliches Endergebnis, was dieses Ergebnis durchaus bekräftigen würde und mögliche Messungenauigkeiten bzw. –fehler nebensächlich macht. Alles in allem kann man jedoch sagen, dass der Versuch im Ganzen gesehen gelungen ist und man ein durchaus wahrscheinliches und vielleicht sogar zutreffendes Ergebnis erzielt hat. Literatur: Für diesen Versuch (und auch dieses Protokoll) war nur das Script zum Praktikum „Struktur und Funktion der Organismen“ vom Wintersemester 2004/2005 relevant und in Gebrauch.