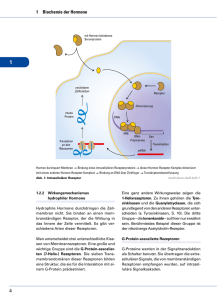
Kap.7.3 Somatoviscerales sensorisches System
Werbung

Physiologische Psychologie Kapitel: 7.3 somatoviscerales sensorisches System 7.3 Das somatoviscerale sensorisches System Somatosensorik: somatische Sensibilität teilt sich in in oberflächliche Sensibilität in Tiefensensibilität oberflächliche Sensibilität: Sinnesmodalität aus Reizung der Haut Haut [behaart & unbehaart] cutaner Sinn Tiefensensibilität [Kinesthesie]: Skelettmuskeln Sehnen Gelenke Viscerale Sensibilität: Sinnesmodalität aus Rezeptoren der inneren Organe Eingeweide Magen Darm Leber Lunge Herz Sensortypen & adäquate Reize: Mechanosensor Druck, Berührung, Spannung, Dehnung, Vibration Thermosensor Abkühlung, Erwärmung Chemosensor Metabolite: pH, pCO2; pO2, Glucose Nozizeptor Gewebeschädigung [Noxen], Hitze, Quetschung Kinesthesie: Wahrnehmung der über Körperposition & Gelenksstellung aus Rezeptoren in Gelenken Sehnen und Muskeln Kinesthetische Wahrnehmung : unbewusst mittels Dehnungsrezeptoren in Muskeln Veränderung der Muskellänge Rezeptoren in den Gelenken Bewegungsrichtung von Gliedmaßen chemische Rezeptoren Dehnung, Temperatur RezeptorInfo aus dem gastrointestianalen System meist nur dehnungsempfindlich -1- Physiologische Psychologie Kapitel: 7.3 somatoviscerales sensorisches System 7.3.2 Anatomie der Haut und ihre rezeptiven Organe Funktion der Haut: Zellschutz Thermoregulator Abkühlung – Schweiß Wärmekonservierung – Regulation der Durchblutung psychogalvanische Reaktion [Messung elektrodermaler Aktivität] Aufbau der Haut: besteht aus subcutanem Gewebe Dermis & oberhalb Epidermis Papillen – kleine Erweiterungen in Dermis und Epidermis enthält verschiedenartige Rezeptoren glatte unbehaarte Haut: Fingerspitzen Handflächen Zehen Fußsolen komplexe Mischung aus freien Nervenendigungen & Axonen enden in spezialisierte Rezeptoren behaarte Haut: enthält freie Nervenendigungen Ruffini-Körperchen Vater-Pacini-Lamellenkörperchen Merkel’sche Tastscheiben Schweißdrüsen Ruffini-Körperchen: Vibrationssensitive Rezeptoren sprechen auf Vertiefung der Haut an in der behaarten Haut Vater-Pacini-Lamellenkörperchen: spezialisierte eingekapselte somatosensorische Nervenendigung sensible für schnelle Vibrationen [kurze Berührungen] entdecken schmerzhafte Reize & Temperaturänderungen sind mit dem bloßen Auge sichtbar [ 0.5 X 1 mm] Meissner’sche Tastkörperchen: berührungssensible Rezeptoren in den Papillen glatter Haut Merkel’sche Tastscheiben: an der Basis der Epidermis generell in der Nähe der Meissner’schen Tastkörperchen in der Nachbarschaft von Schweißdrüsen sprechen auf Einbuchtungen der Haut an sensibel auf Berührungen -2- Physiologische Psychologie Kapitel: 7.3 somatoviscerales sensorisches System Mechanorezeptoren: Merkel’sche Tastscheiben Ruffini-Körperchen Meissner’sche Tastkörperchen Vater-Pacini-Lamellenkörperchen Kategorien von Mechanorezeptoren in unbehaarter glatter Haut: Tabelle 7.1pg.267 Carlson Merkelsche Tastscheiben rezeptives Feld kleine abrupte Kante Adaption niedrige Geschwindigkeit Ruffini-Körperchen rezeptives Feld große diffuse Kante niedrige Geschwindigkeit der Adaption Meissner’sche Tastkörperchen rezeptives Feld kleine abrupte Kante schnelle Adaption Vater-Pacini-Lamellenkörperchen rezeptives Feld große diffuse Kante schnelle Adaption 7.3.3 Wahrnehmung der Hautreizung Zwei-Punkt-Diskrimination: Fähigkeit Berührungsmerkmale zu unterscheiden [Zirkel] Abstand der gerade noch als getrennter Stimulierkennung zulässt Maß für das räumliche Auflösungvermögen der Haut für taktile Reize Diskriminationsmaße: hohe Diskrimination am Rücken Bauch [7 cm] niedrige Diskrimination auf Finger & Hand 5 und 15 mm sehr hohe auf Oberarm Ellenbogen Unterarm zwischen 4 und 7 cm Zehen circa 1cm Lippen 2 bis 5 mm laterale Inhibition: Mechanismus zur Kontrastverstärkung im somatosensorischen System benachbarte Zellen hemmen sich gegenseitig Input wird erst verstärkt bevor er die nachgeschaltete Zelle erreicht durch eine andere benachbarte Zelle gehemmt Übertragung taktiler Information: myelinisierte Neurone unmyelinisierte Neurone vorwiegend von schnellen myelinisierten Neuronen A Neuronen auch über langsame unmyelinisierte Neurone unmyelinisierte C Neurone Zielgebiet Insula Neuronentypen für taktile Informationsübertragung: Propiozeption A Gruppe I 80-120m/sec Mechanozeption A Gruppe II 35-75m/sec Schmerz A gramma Gruppe III 5-30m/sec Temperatur C unmyelinisiert Gruppe IV 0.5-2m/sec -3- Physiologische Psychologie Kapitel: 7.3 somatoviscerales sensorisches System Pfade der Weiterleitung: Berührung & Vibration dorsal column medial lemniscus pathway Hinterseitenstrangbahn Schmerz & Temperatur Spinothalamic pathway Vorderseitenstrangbahn Weiterleitung von Berührung & Vibration an den Cortex: A A und A- gamma Neurone dorsalen Kanal des Rückenmarks – ipsilateral dorsal column nuclei der Medulla – ipsilateral in medialen lemniscus VP Nucleus – Thalamus – contralateral Primärer somatosensorischer Cortex [S1] Weiterleitung von Temperatur & Schmerz zum Cortex A-gamma & C Neurone dorsaler Pfad contralateral lateraler spinothalamischer Trakt Rückenmark & Medulla Thalamus primären somatosensorischen Cortex primärer somatosensorischer Cortex: Brodmann Areale 1 2 und 3 [3a 3b] nach dem Sulcus centralis somatosensorische Information & Thalamus: Info von Thalamus meister Input in Areal 3a & 3b & in die rezeptive Schicht 4 des Cortex weiter projiziert in Areal 1 & 2 wieder zurück in 3a und 3b Unterscheidung der Areale für somatosensorischen Input: BA1 hauptsächlich für Oberflächenbeschaffenheit BA 2 Größe & Form BA3b Textur Größe & Form Somatosensorischer Homunkulus: somatotopische Repräsentation in Form eines Männleins die Körperteile sind in Relation zur Repräsentation der Cortexareale die sie einnehmen dargestellt große Lippen große Hände großer Füße kleine dünne Arme und Beine Columnare Repräsentation / Organisation: sprechen auf einen bestimmten Reiztyp aus einer bestimmten Region des Körpers an abwechselnde Säulen von schnell und langsam adaptierende Rezeptoren Muskellänge & Gelenke Vater-Pacini-Lamellenkörperchen -4- Physiologische Psychologie Kapitel: 7.3 somatoviscerales sensorisches System Patient G.L Vollständiger Verlust der myelinisierten Fasern im N. suralis keine Berührungssensibilität keine Wahrnehmung von Kitzeln etc. Intakt Temperatur Schmerz & Jucken unmyelinisierte Fasern reagieren auf diese Reize ihr Zielgebiet ist Insula [System für Streicheleinheiten ] somatosensorischer Cortex wird nicht aktiviert unbehaarte Handfläche [glatte Haut] wird nur von myelinisierten Axonen versorgt Patientin G.L nahm diese Berührung nicht wahr Adaption in Zusammenhang mit Sensorik: konstante Reize lösen nach einer längeren Darbietungsdauer keine weiteren Empfindungen mehr aus [Armbanduhr] fehlende Aktionspotentiale physikalische Konstruktion der Rezeptoren Desensibilisierung bei längerem Druck konstante harmlose Reize sind kaum von Belang also ist dieser Adaptionsmechanismus sehr nützlich Temperatur Wahrnehmung der Temperatur Thermosensation durch freie Nervenenden Natrium-Kalium-Pumpe vermutlich für sensorische Transduktion an den Kälterezeptoren zuständig [Spray 1986] Rezeptoren für Wärme & Kälte liegen unterschiedlich tief in der Haut Kälterezeptoren eher im oberen Teil Wärmerezeptoren in tiefen Gewebsschichten [Bazett et al 1932] Thermorezeptoren: Wärmerezeptoren reagieren bei Temperatur zwischen 30° - 45 ° Kälterezeptoren feuern bei 10° manche reagieren auch wieder bei Temp. über 45 ° Schmerz Schmerzrezeption: durch ein Netzwerk frier Nervenenden in der Haut wie bei Thermosensation Nociceptoren Dektoren Gewebeschädigender schädlicher Reize mindestens drei Arten von Nociceptoren reagieren auf starken Druck oder Dehnung Schläge oder Kneifen [Mechanorezeptoren] Reaktion auf hohe Temperatur oder Säure VR1 Rezeptor für Schärfe [Capsaicin Wirkstoff von Chili] Brennen der Haut oder Entzündungsschmerz ATP sensible Rezeptoren Tumorschmerz Angina Migräne -5- Physiologische Psychologie Kapitel: 7.3 somatoviscerales sensorisches System 7.3.4 Die somatosensorischen Bahnen: somatosensorische Axone: aus Haut Muskeln & inneren Organen über Spinalnerven ins ZNS Gesicht & Kopfbereich Teil des Nervus trigeminus [V. Hirnnerv] unipolare Neurone in dorsalen Ganglionwurzel & in Ganglien des Hirnnervs Pfad für genau lokalisierbare Information: feine Berührung Axone steigen über Hinterstrangbahnen in weiße Substanz des Rückenmarks zu Kernen der unteren Medulla oblongata auf kreuzen contralateral in Lemniscus medialis [mediale Schleifenbahn] zu ventralen posterioren Kernen des Thalamus Axone aus dem Thalamus projizieren zum primären somatosensorischen Cortex weiter zum sekundären somatosensorischen Cortex Hinterstrangbahnen übertragen: epikritische Sensibilität Berührung Vibration Gelenksempfindungen Pfad für schlecht lokalisierbare Information: Schmerz oder Temperatur grober Druck- Tastreiz Axone aus dorsalen Ganglionwurzel kreuzen zur Gegenseite des Rückenmarks steigen über die Vorderseitenstrangbahn Tractus spinothalamicus zu den ventral posterioren Thalamus-Kernen protopathische Sensibilität Schädigungen des somatosensorischen Cortex: apperzeptive taktile Agnosie assoziative taktile Agnosie taktile Apraxie apperzeptive taktile Agnosie: Schädigung des linken Parietallappens Unfähigkeit Objekte durch Tasten zu erkennen obwohl taktile & Thermo-Schmerz Sensibilität intakt assoziative taktile Agnosie: bilaterale Läsion des Gyrus angularis [Abschnitt des PL] kann Berührte Objekte zeichnen aber nicht identifizieren intaktes Dreidimensionales Erkennen aber Analyse des Assoziationscortex defekt keine Integration von Sprache & Bewusstsein taktile Apraxie: gestörte Kooperation zw. motorischem & somatosensorischem System Störung Absichtsgelenkter Bewegung [Abtasten] desorganisiertes Abtasten taktile Perzeption an sich intakt -6- Physiologische Psychologie Kapitel: 7.3 somatoviscerales sensorisches System 7.3.5 Schmerzwahrnehmung Schmerzrezeptor: VR1-Rezeptor ionotroper Rezeptor enthält nociceptive Fasern sensibel für Capsaicin [Chili] Hitze & Säure Entzündungsschmerzen ATP-sensible Rezeptoren Nerventypen zu Schmerzweiterleitung: Nociceptoren myelinisierte schnelle Schmerzweiterleitung unmyelinisierte C Fasern dumpfe Weiterleitung perzeptive Verhaltenskomponenten von Schmerz [nach Price] sensorische Komponente unmittelbare Empfindung der Stärke Schmerzsensation unmittelbar emotionale Komponente unmittelbares Unlustempfinden unmittelbare emotionale Folgen langzeitige emotionale Komponente chronische Schmerzen künftiges Wohlbefinden & Komfort perzeptive Schmerzkomponenten & Hirnmechanismen: rein sensorische Komponente über Tractus vom Rückenmark Thalamus ventral posteriore thalamische Kerne primär & sekundär somatosensorischen Cortex unmittelbar emotionale Komponente vordere Gyrus Cinguli Cortex der Insula langzeitige emotionale Komponente durch Bahnen des präfrontalen Cortex Schädigung des Frontallappens Uneinsichtigkeit über Konsequenzen chronischer Schmerzen od. Schmerz als Warnsignal Manipulation des Schmerzempfindens: Elektro-Stimulation der Insula brennende & stechende Schmerzsensation Schädigung der Insula Verringerung der emotionalen Reaktion Schmerz wird empfunden aber nicht als Schadenssignal erkannt kein Rückzugs- Vermeidungsverhalten Hypnose Schmerzempfinden wird bei gleich bleibender Intensität geringe unangenehme Empfindung wird geringer regionale Aktivierung des Gehirns bei Schmerzreizen – PET: primärer somatosensorischer Cortex & Gyrus Cinguli aktiv bei Hypnose vermindert sich die Aktivität des Gyrus Cinguli verantwortlich für das Unlustgefühl [ACC] Intensitätsempfinden primäre somatosensorische Cortex -7- Physiologische Psychologie Kapitel: 7.3 somatoviscerales sensorisches System Phantomglied Phantomschmerz: Sensation eines Gliedes das amputiert wurde bis zu 70% erleben das amputierte Glied als existent durch Bildung von Neurome an den Nervenenden Phantomschmerzen der Hände treten oft im Gesichtsbereich auf somatosensorische Stimuli dieser Körperteile sind im Cortex [S1] nebeneinander repräsentiert Amputation und corticale Repräsentation: benachbarte Repräsentationsbereiche können sich auf den „amputierten“ Bereich ausdehnen bei ausgiebigem Training dehnt sich die corticale Repräsentation ebenfalls aus Gate-theory of Pain nach Melzack & Wall: Projektionsneurone im dorsalen Horn die Axone in spinothalamischen Trakt weiterleiten werden sowohl von Berührungssensitive als auch Schmerzsensitiven Axonen erregt Berührungssensitive Neurone aktivieren Interneurone die Schmerz-Axone hemmen Schmerz kann so durch Druck/ Reibung neben der Schmerzstelle unterdrückt werden aufsteigende Schmerzregulation Modifikation der Schmerzwahrnehmung endogene Modifikation der Schmerzsensibilität neuronale Schaltkreise können Analgesie verursachen Freisetzung endogener Opioide Analgetische Hirnstimulation elektrische Stimulation des periaquaeductalen Höhlengraus im rostral-ventralen Teil der Medulla oblongata [PAG] dient auch der Verminderung von chronischen Schmerzen Analgesie kann auch durch Akupunktur ausgelöst werden allerdings durch Naloxon [Opiat-Rezeptor-Blocker] aufgehoben Placeboanwendung ebenfalls Wirkung endogener Opioide: Analgesie Opiate hemmen inhibitorische Neurone im PAG Disinhibition der Neurone die auf Nc. Raphe Magnus projizieren Raphe-Kern enthält Neurone die Serotonin freisetzen projiziert auf graue Substanz des dorsalen Rückenmarks Schmerzweiterleitung wird inhibiert Placebo Placebo-Effekt: reduzierte Aktivität der schmerzsensitiven Areale Ausschüttung endogener Opioide erhöhte Aktivität im präfrontalen Cortex & im medialen periaquaeductalen Hohlengrau Aufhebung des Placebo-Effekts: durch Injektion von Naloxon Blockade von Opiatrezeptoren bei Akupunktur möglich bei Hypnose nicht Frauen reagieren stärker auf blaue Placebos Männer auf orange Tranquilliser Placebos -8-