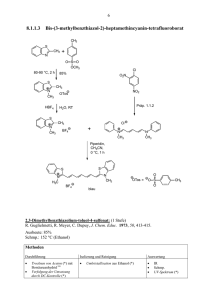
Kap4_1,4Diazine
Werbung

12 Kapitel 4 4 Ein Ausschnitt aus der vielfältigen Chemie der 1,4-Diazine Unter 1,4-Diazinen sollen Pyrazin und seine Derivate sowie Verbindungen mit einer Pyrazin-Teilstruktur verstanden werden.[27] Beispiele hierfür sind Phenazin, Chinoxalin und deren Derivate. Sie alle zeichnen sich durch ein niedrig liegendes LUMO und als Ligand durch die Fähigkeit zur Brücken-Koordination aus. Aufgrund der Ausrichtung der Elektronenpaare eignet sich Pyrazin als bifunktioneller, nicht chelatbildender Brücken-Koordinationspartner. Phenazin und Chinoxalin unterscheiden beieinanderliegende sich Grenzorbitale von Pyrazin und der durch enger erschwerten N-Koordination sterisch anspruchsvoller Gruppen aufgrund der peri-Wechselwirkungen. 1,4-Diazine verfügen über ein zweistufiges Redoxsystem, das mit einer mehrstufigen Protonierung kombiniert werden kann. Da Radikale vom Wurster- bzw. Weitz-Typ gebildet werden, eignen sie sich ausgezeichnet für Untersuchungen paramagnetische zum intermolekularen Elektronen-Transfer.[28] 7-Elektronen-Zwischenstufe der 1,4-Diazine Die ist thermodynamisch außerordentlich stabil.[27] Die 1,4-Dihydro-1,4-diazine mit 8Elektronen im sechsgliedrigen Ring sind dagegen, aufgrund der potentiellen Antiaromatizität bei Einbeziehung der freien Elektronenpaare der beiden Stickstoffatome und des daraus resultierenden hohen Elektronenüberschusses nicht stabil. So liegt z.B. das erste Ionisationspotential von 5,10-Dimethyl-5,10dihydrophenazin bei 6.57 eV.[29] Phenazin und Chinoxalin nehmen noch leichter Elektronen auf als Pyrazin und bilden die beständigeren Radikalionen sowie die stabileren Dihydroverbindungen. Die höhere Beständigkeit von 5,10Dimethyl-5,10-dihydrophenazin förderte seine Verwendung als ElektronenTransfer-Reagenz, z.B. bei der Reaktion mit Dioxetanonen (- Peroxylacetonen), bei der Chemilumineszenz auftritt (Abb. 4.1).[30] Das nach der Reduktion des Dioxetanons gebildete Radikalanion zerfällt unter Abspaltung von Kohlendioxid und Rückübertragung des Elektrons auf das Chemie der 1,4-Diazine 13 Radikalkation des 5,10-Dimethyl-5,10-dihydrophenazins, das unter Chemilumineszenz in den Grundzustand zurückkehrt. CH3 N + O O SET CH3 CH3 N N C N , N O CH3 - CO 2 O O O + C C N O CH3 CH3 SET CH3 * CH3 N O + O N Chemilumineszenz + C N N CH3 CH3 C Abb. 4.1: Mechanismus der Chemilumineszenz des Systems aus Dioxetanon und 5,10Dimethyl-5,10-dihyrophenazin. Aufgrund ihrer Neigung -Komplexe zu bilden, wurden unterschiedlich substituierte, zum Teil radikalische Verbindungen des Phenazins mit 7,7,8,8Tetracyanochinodimethan (TCNQ) umgesetzt. Es wurden Komplexe mit gemischten und getrennten Molekülstapeln erhalten. Das Interesse an solchen Donor-Akzeptor-Komplexen beruht auf deren potentiellen Leitfähigkeitseigenschaften.[31] So kristallisiert z.B. der Komplex des 5,10Dimethyl-5,10-dihydrophenazins und des Phenazins mit TCNQ in getrennten Kationen- und Anionenstapeln (Abb. 4.2). CH3 NC CN N CH3 , N CH3 CN N + n n NC N CN CN CH3 CN CN n Abb. 4.2: Komplex aus 5,10-Dimethyl-5,10-dihydrophenazin; Phenazin (n. abg.) und TCNQ. 14 Kapitel 4 Auch in der Biochemie findet man häufig die 1,4-Diazin-Struktur, wie z.B. im Riboflavin (Vitamin B2). CH2OH HO C H HO C H HO C H CH2 H3C N H3C N N O N H O 4.1 Die Photoreduktion des Phenazins in Lösung ersten Untersuchungen der Photoreduktion von Phenazin in verschiedenen Alkoholen wurden von Toromanoff et al. unternommen.[32] In konzentrierten Lösungen in Methanol fanden sie Komplexe aus Phenazin und 5,10-Dihydrophenazin. Im schwach sauren Methanol (Essigsäure/Acetat; 0.1 M) und im stark sauren Methanol (HCl; 0.1 M) wurde die Photoreduktion von Bailey et al. untersucht (Abb. 4.1.1.a+b). [33] Unter den dort gewählten Bedingungen ist 1n,* der niedrigste angeregte Zustand. Die Zugabe von Dibrommethan quencht die Reaktion nicht. Im schwach Sauren schlagen sie eine Protonierung dieses Zustandes vor, so daß ein monoprotoniertes angeregtes 1Phenazin entsteht (Abb. 4.1.1.a). Dies wird dann durch weitere Bestrahlung sofort zum Semichinonradikal reduziert, welches dann mit einem weiteren Semichinonradikal disproportioniert. zu Phenazin und 5,10-Dihydrophenazin Chemie der 1,4-Diazine 15 a) Photoreduktion in Methanol bzw. sc hwac h saurem Methanol: 1 N * N h 1 HA N N * N N H 1 N H * N N D Disproportionierung N N H H N H + N Komplexe N b) Photoreduktion in stark saurem Methanol: 1 N h H * 1 N N N H H H N * N HA H 1 N H H * N N N D N + -H N N N H H H H N N + 2 N H 2 N + H 2 N N H H 2 16 Kapitel 4 Abb. 4.1.1.a/b: Mechanismen der Photoreduktion von Phenazin in Lösung. Im stärker sauren Methanol (HCl; 0.1 M) schlägt Bailey vor, daß das monoprotonierte Phenazin direkt angeregt und ein zweites Mal protoniert wird (Abb. 4.1.1.b). Durch anschließenden Elektronentransfer von einem Donor (D) wird erneut 5,10-Dihydrophenazin gebildet, welches mit dem monoprotonierten Phenazin unter Protonenabgabe zwei Semichinonradikale bilden soll, die jeweils wieder zu diprotoniertem Phenazinradikalanion protoniert werden. Weitere Untersuchungen zur Photoreduktion von Phenazin wurden von Davis et al.[34] unternommen. Sie untersuchten das System in 2Propanol, Triethylamin und tri-n-Butylstannan und konnten zeigen, daß der niedrigste 3,*- und der 1,*-Zustand des Phenazins unter diesen Bedingungen nicht reagieren. Ihre Ergebnisse konnten am besten mit einem reaktiven 1n,*-Zustand mit einer Lebensdauer von ~10-9 s interpretiert werden. Zu den gleichen Ergebnissen kamen Kawata et al.,[35] die die Photoreduktion des monoprotonierten Phenazins bei kontinuierlicher Bestrahlung in wäßriger Schwefelsäure untersuchten. Die reaktive Spezies ist das im angeregten Singulett-Zustand vorliegende monoprotonierte Phenazin. Die Zugabe von 1,2-Dibrommethan konnte die Reaktion nicht quenchen. 1,2-Dibrommethan ist ein Quencher für 3,*-Zustände. Das erhaltene Photoprodukt ist das diprotonierte Phenazinradikalanion (5,10-Dihydrophenazinradikalkation).
![6.3.1 1-Oxa-spiro[2.5]octan - Institut für Organische Chemie](http://s1.studylibde.com/store/data/001356875_1-96e669e5c88ad586db9f9f199d424d05-300x300.png)