Synthese von Cyanacetamid aus Cyanessigester
Werbung
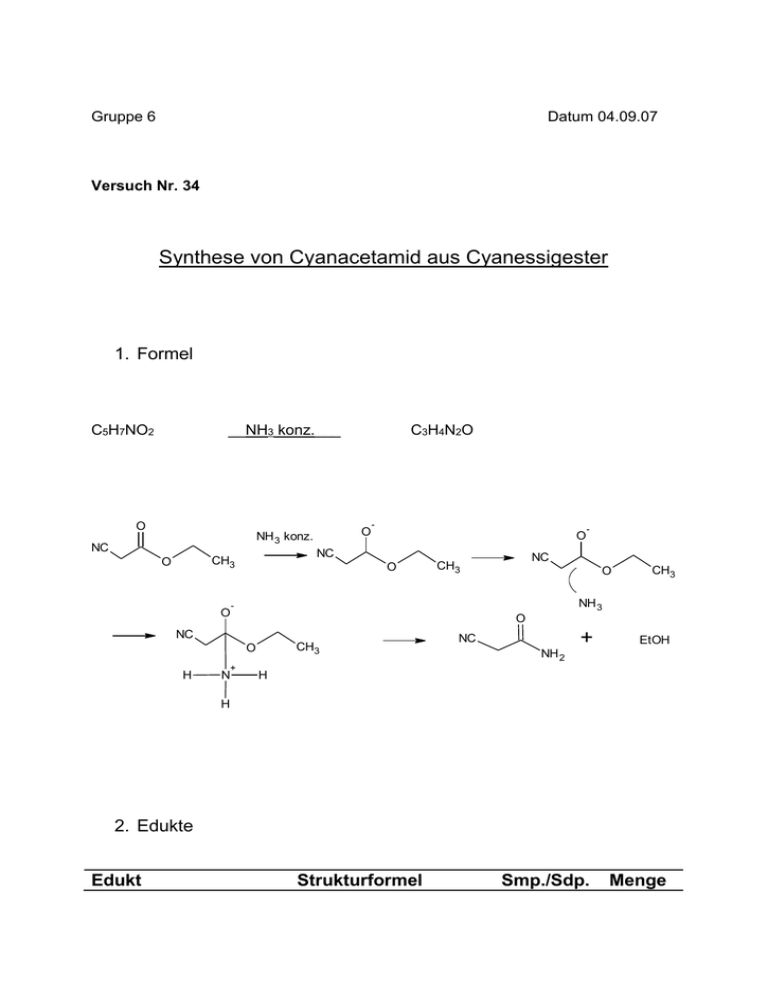
Gruppe 6 Datum 04.09.07 Versuch Nr. 34 Synthese von Cyanacetamid aus Cyanessigester 1. Formel C5H7NO2 __NH3 konz.___ O O NH 3 konz. NC O - O NC CH3 O C3H4N2O O O + CH3 NH 3 O CH3 O N NC CH3 - NC H - + EtOH Smp./Sdp. Menge NC NH 2 H H 2. Edukte Edukt Strukturformel Cyanessigsäureethylester konz. Ammoniak NH3 Ethanol -22°C/209°C 11,3g -77,74°C/33,41°C -114°C/78°C 30ml 3. Durchführung 11,3g Cyanessigsäureethylester werden unter Rühren langsam mit 30ml konz. Ammoniak versetzt. Dieses Reaktionsgemisch wird 40 Minuten bei Raumtemperatur gerührt und anschließend auf 0°C abgekühlt. Es scheidet sich Cyanacetamid ab, was abfiltriert und aus wenig Ethanol umkristallisiert wird. Vom entstandenen Produkt wird ein IR-Spektrum aufgenommen. 4. Beobachtung Der Versuch verlief genau wie in der Durchführung beschrieben. Das Endprodukt ist ein leicht gelbliches körniges Material. Das erstelle IR-Spektrum bestätigte das Produkt als Cyanacetamid (Siehe Anhang). 5. Ergebnis/Produkt Produktname: Cyanacetamid Menge: 2,5g Schmelzpunkt (bei Normaldruck): 120°C (Ethanol) Literaturwert Gefahrenbezeichnung: Xn R-/S-Sätze: R20/21/22, S28 Strukturformel: O NC NH 2 6. Reaktionsmechanismus Diese Art der Reaktion wird auch als Ammonolyse von Estern bezeichnet. Hierbei werden Ester mit Ammoniak zu Amiden umgesetzt. O O + R NH 3 OR' + R R'OH NH 2 Der Mechanismus ist eine nukleophile Acylsubstitution und beruht auf dem nukleophilen Angriff auf die Carbonylgruppe des Esters durch das freie Elektronenpaar am Ammoniakstickstoff. Die nukleophile Addition an die Carbonylgruppe ist der Schlüsselschritt, hierbei entsteht aus dem trigonalen Ausgangsprodukt eine tetraedrische Zwischenstufe. Im nächsten Schritt wird die Ester-Gruppe, also Sauerstoff zusammen mit einem Rest (hier CH2CH3), abgespalten und es entsteht das wieder trigonale Endprodukt, ein Amid.








![6.3.1 1-Oxa-spiro[2.5]octan - Institut für Organische Chemie](http://s1.studylibde.com/store/data/001356875_1-96e669e5c88ad586db9f9f199d424d05-300x300.png)

