CO2 kann als schwaches Oxidationsmittel jedoch mit stark
Werbung

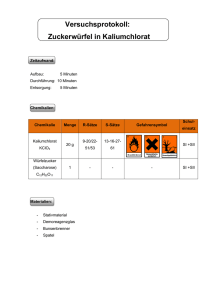
Kaliumchlorat O (brandfördernd) Xn (gesundheitsschädlich) weißes, kristallines Pulver KClO3 RSE-Sätze: R 9-20/22, S 13-16-27, E 1-6 MG: 122,55 g/mol Dichte: 2,34 g/cm3 Wasserlöslichkeit: 20°C 71g/l, 100°C 560g/l Schmelztemperatur: 370 °C Eigenschaften: Kaliumchlorat gibt oberhalb seiner Schmelztemperatur unter Bildung von Kaliumperchlorat Sauerstoff ab: 2 KClO3 ---> KCLO4 + KCl + O2. Über 550 °C zerfällt es vollständig in Kaliumchlorid (KCl) und Sauerstoff. Diese Zersetzung findet bei der Zugabe von Mangandioxid (Braunstein) als Katalysator schon bei 150-200 °C statt. Wird es mit leicht oxidierbaren Stoffen (Schwefel, Phosphor, Iod, Kohlenstoff) vermischt, kann es beim Erhitzen, bei Reibung, Stoß oder Schlag sehr heftig explodieren. Dies gilt auch für Mischungen mit organischen Stoffen, z.B. Holzmehl oder Petroleum. Aus diesem Grunde ist das Oxidationsmittel Kaliumchlorat mit allergrößter Vorsicht zu handhaben, da schon geringfügige Verunreinigungen und Berührungen die explosiven Reaktionen auslösen können. Es wird empfohlen, nur analysenreines und frisches, sehr sauberes Kaliumchlorat zu verwenden! (siehe auch: Hinweise zur Entsorgung von Kaliumchlorat) Herstellung: Die Gewinnung erfolgt durch Elektrolyse einer Natriumchloridlösung und der nachfolgenden Fällung des entstandenen Natriumchlorats mit Kaliumchlorid (KCl). Dabei werden die Elektroden (Kathode: Stahl; Anode: aktiviertes Titan) nicht wie bei der Herstellung von Natriumhydroxid durch eine Membran voneinander getrennt, sondern eng aneinander gelegt. Es entstehen Natriumchlorat und Salzsäure. Gibt man zu einer Natriumchloratlösung Kaliumchlorid fällt Kaliumchlorat aus. Bei der Elektrolyse einer Kaliumchloridlösung entsteht das Kaliumchlorat auf direktem Weg. Verwendung: Zur Herstellung von Zündhölzern (roter Phosphor an den Reibflächen entzündet das Gemisch aus Kaliumchlorat und Schwefel im Zündholzkopf), zur Produktion von Sprengstoffen ("Chloratit" enthält ca. 90% Kaliumchlorat, 10% organische Kohlenwasserstoffe und einen Zusatz von Holzmehl); Herstellung von Leuchtmunition und Feuerwerkskörpern; in der Medizin früher in Gurgelwasser; als Unkrautvernichtungsmittel (früher "Unkraut Ex").