Grundpraktikum
Werbung

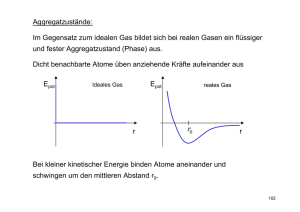
Versuchsprotokoll Versuch 2: Dampfdruckkurve Gruppe 43: Annika Kroning, Alexandra Erdt, Jakob Machon 1 – fach Bachelor Kolloquium: 23.06.06 Versuchstag: 29.06.06 1 1. Theoretische Grundlagen 1.1 Dampfdruck Evakuiert man einen Behälter und füllt dann eine Flüssigkeit ein, so entsteht ein dynamisches Gleichgewicht zwischen der flüssigen und der gasförmigen Phase. Der Dampfdruck stellt diejenige Kraft dar, die die Teilchen der gasförmigen Phase auf die Innenfläche des Behälters ausüben. Druck ist definiert als Kraft pro Fläche, demnach ist der Dampfdruck die Kraft der Teilchen, die auf die Innenwände ausgeübt wird dividiert durch die Oberfläche des Behälters. Der Dampfdruck ist temperaturabhängig: Bei einer bestimmten Temperatur weist er immer denselben Wert auf. Bei einer Volumenänderung stellt sich das Gleichgewicht neu ein: Bei Verkleinerung des Volumens gehen mehr Teilchen in die flüssige Phase über, bei Vergrößerung des Volumens gehen mehr in die Dampfphase über. Verbindungen oder Stoffe mit einem hohen Dampfdruck verdampfen schneller als solche mit einem niedrigeren Dampfdruck, also ist der Dampfdruck ein Maß für die Flüchitgkeit eines Stoffes. Am Siedepunkt ist der Dampfdruck gleich dem Atmosphärendruck. 1.2 Phasenübergänge Abb. 1: Phasendiagramm eines reinen Stoffes Ein Phasendiagramm eines Stoffes ist eine graphische Darstellung der Druck – und Temperaturbereiche, bei denen die einzelnen Phasen thermodynamisch stabil sind. Die drei Kurven stellen jeweils die Grenzen zwischen den Phasen dar. An diesen Grenzen stehen die beiden Phasen im Gleichgewicht. Ist der Umgebungsdruck gleich dem Dampfdruck, siedet eine Flüssigkeit (Siedepunkt). Es gibt zwei besondere Punkte im Phasendiagramm: 2 Tripelpunkt: An diesem Punkt treffen sich die drei Kurven. Hier liegen alle drei Phasen im Gleichgewicht vor. Er ist für jeden Stoff spezifisch festgelegt. Es ist der niedrigste Punkt, an dem der Stoff in der flüssigen Phase vorliegen kann. Kritischer Punkt: Es ist das höchste Temperatur/Druck – Paar, an dem eine Flüssigkeit existieren kann. Bei höherem Druck bzw. höherer Temperatur können Flüssigkeit und Gas nicht mehr unterschieden werden. 1.3 Gibb`sche Phasenregel Mit Hilfe der Gibb`schen Phasenregel lässt sich berechnen, wieviele Zustandsvariablen im System verändert werden können, ohne dass sich die Phasen ändern: F=K–P+2 F: Freiheiten (Anzahl der veränderbaren Zustandsvariablen) K: Anzahl der Komponenten P: Anzahl der Phasen Am Tripelpunkt ist F = 1 – 3 + 2 = 0 (invariant), da keine der Zustandsvariablen (T, p) geändert werden kann ohne eine Änderung des Phasengleichgewichts hervorzurufen. Auf den Kurven des Phasendiagramms ist F = 1 – 2 + 2 = 1 (univariant), demnach kann eine der Variablen (T, p) geändert werden. Die andere gleicht sich dann so der Änderung an, dass die Phasen wieder ins Gleichgewicht kommen. Liegt nur eine Phase vor, so ist F = 1 – 1 + 2 = 2 (divariant), es können also beide Variablen in gewissem Maße beliebig verändert werden, ohne dass sich die Phase ändert. 1.4 Beschreibung der Verdampfungsenthalpie über die Gleichung von Clausius-Clapeyron und Anwendung des Kirchhoff’schen Satzes Am Phasenübergang sind die chemischen Potentiale der beiden Phasen gleich, es gilt μgas=μflüssig und dμgas=dμflüssig Außerdem gilt für d S m dt Vm dp . Ersetzt man die dμ durch die totalen Differentiale und fasst zusammen, ergibt sich die Beziehung dp S m dT Vm (1) Da die beiden Phasen im Gleichgewicht stehen und somit der Vorgang reversibel ist, kann man die Entropie durch die dabei umgesetzte Wärmemenge (die bei isobaren Prozessen gleich der Änderung der molaren Enthalpie ist) und die zugehörige Temperatur ersetzen: v S also gilt dp v H dT T vV v H T (Clausius – Clapeyron`sche Gleichung) (2) 3 Mit ΔvV gleich der Differenz der Molvolumina (V(g) – V(l)). Die Clausius – Clapeyron`sche Gleichung beschreibt die Steigungen der im Phasendiagramm dargestellten Kurven, in diesem Fall die der Siedekurve. Betrachtet man jetzt Moleküle von Gasen, stellt man fest, dass diese sich frei im Raum bewegen können. Sie nehmen also den für sie frei zur Verfügung stehenden Raum komplett ein. In Flüssigkeiten spielen jedoch intermolekulare Kräfte eine Rolle, von den die Moleküle zusammengehalten werden. Wenn der Temperatur – Druck – Bereich weit unterhalb der kritischen Temperatur und dem kritischen Druck liegt, so ist VFlüss viel kleiner als VDampf und kann somit vernachlässigt werden. Die Clausius – Clapeyron`sche Gleichung kann zu folgender Gleichung vereinfacht werden: H v dp dT T VDampf Für niedrige Dampfdrücke gilt für die Gasphase annähernd das ideale Gasgesetz. Setzt man V RT aus der Zustandsgleichung idealer Gase für VDampf ein, so ergibt sich: p H v H v H v p dp RT dT T VDampf R T 2 T p durch Umformen kommt man auf H v dp dp mit d ln p . Die Gleichung lautet dann: 2 pdT RT p d ln p H v dT RT 2 Durch Trennung der Integrationsvariablen p und T ergibt sich: d ln p H v dT RT 2 Handelt es sich um einen kleinen Temperaturbereich, so ändert sich H v kaum und kann daher als konstant angesehen werden. Unter Berücksichtigung dieser Bedingung integriert man nun die oben aufgeführte Gleichung und zieht die Konstanten H v und R vor das Integral. Es ergibt sich somit: ln Da ln p2 H v H v ln p1 p1 R R T1 p2 ln p2 ln p1 kommt man durch erneutes Umformen der obigen Gleichung p1 auf die Geradengleichung: 4 ln p2 H v H v ln p1 R T2 R T1 Die Steigung dieser Gleichung lautet: m Wenn ln p gegen H v R T2 1 aufgetragen wird, kann man H v aus der Steigung berechnen. T Um die ermittelten Daten mit den Literaturwerten vergleichen zu können, müssen die Werte auf 25°C umgerechnet werden. Dazu muss der Kirchhoff’sche Satz angewendet werden. Kirchhoff’scher Satz: T2 H v ,T2 H v ,T1 C p dT T2 Für die Verdampfung ergibt sich dann: T2 H vT2 H vT1 c p ( Dampf ) c p ( Flüssigkeit ) dT T1 Innerhalb einer Phase verändert dich c p nur wenig. Somit kann man auch hier sagen, dass c p konstant ist. Dieses gilt, wenn sich die Temperatur nicht stark verändert. Letztendlich gilt also: H v ,T2 H v ,T1 c p (T2 T1 ) 1.5 Temperaturabhängigkeit der Verdampfungsenthalpie Die Verdampfungsenthalpie ist temperaturabhängig. Sie nimmt mit steigender Temperatur zu, bis der kritische Punkt erreicht ist. An diesem Punkt kann der Stoff nicht mehr flüssig vorliegen, somit kann auch nichts verdampfen. 1.6 Troutonsche Regel Die Verdampfungsentropie, die aus der Verdampfungsenthalpie der jeweiligen Flüssigkeit am Siedepnkt bestimmt wird, ist im Mittel gleich groß. Sie streut um den Durchschnittswert verd S verd H = 88JK-1mol-1 TS Bei Stoffen, die Wasserstoffbrückenbindungen ausbilden, liegt die Verdampfungsentropie über 88J/Kmol. Der Grund dafür ist ihre geringe Entropie in der flüssigen Phase, da die Moleküle durch die Wasserstoffbrücken geordneter vorliegen als bei Stoffen ohne Brückenbindungen. In der Gasphase tre- ten die Wasserstoffbrücken nicht mehr auf, die 5 Entropieerhöhung ist also größer. Verbindungen mit Werten unter 88 J/Kmol bilden sowohl in der flüssigen als auch in der Dampfphase intermolekulare Bindungen aus, sodass diese in beiden Phasen geordneter vorliegen. Für Stoffe, die dem Troutonschen Regelfall in etwa entsprechen, gelten folgende experimentelle Tatsachen: Schwingungsspektren von flüssiger und gasförmiger Phase unterscheiden sich kaum Gleiches gilt für die Rotationen → Moleküle schwingen und rotieren in diesen beiden Phasen sehr ähnlich, somit müssen wesentliche Änderungen der Energie und Entropie die Translation betreffen. Man geht jetzt also davon aus, dass den Flüssigkeitsmolekülen Raum für Bewegungen (insbesondere Translation) zur Verfügung steht. Demnach behandelt man eine Flüssigkeit wie ein Gas und die Verdampfung wie die Expansion eines Gases. Dieser Raum wird freies Volumen genannt und ist wesentlich kleiner als das Volumen der Gasbehälter. Wird also das Gasmodell auf Flüssigkeiten angewandt, so steht NA Flüssigkeitsmolekülen ein Raum von ca. 1cm3 für die Translation zur Verfügung. 1.7 Druckmessgeräte Manometer: Das Manometer wird zur Messung von Gasdrücken in geschlossenen Systemen verwendet. Es besteht aus einem am oberen Ende geschlossenen Glasrohr, welches mit Gas gefüllt ist und in einem mit Quecksilber gefüllten Behälter steht. Durch das Eigengewicht des Quecksilbers sinkt die Hg – Säule soweit, bis der von ihr ausgeübte Druck gleich dem Druck entspricht, der auf den Quecksilberbehälter ausgeübt wird. Die Skalierung ist im Allgemeinen so gewählt, dass die Hg – Säule an einem duchschnittlichen Tag auf Meereshöhe 760mm = 1Torr = 1atm hoch ist. Barometer: Das Barometer hat eine ähnliche Funktionsweise wie das Manometer. Es wird meist im Zusammenhang mit meteorologischen Messungen gebraucht. Dort hängt der Luftdruck neben der Höhe auch von der Wetterlage ab. 2. Versuch 3.1 Versuchsaufbau: 6 Abbildung 1 Dampfdruckmessapparaturi 3.2 Versuchsbeschreibung Mit der oben dargestellten Apparatur lassen sich statistische Dampfdruckmessungen durchführen. Die Temperatur lässt sich mit Hilfe eines Eisbades, das immer weiter erwärmt wird, einstellen und der zugehörige Druck wird am Druckmessgerät abgelesen. Die Pumpe ist in diesem Fall eine Drehschiebervakuumpumpe. Damit eine Verunreinigung Pumpe verhindert wird, wird zwischen die Pumpe und den Messkolben eine Kühlfalle geschlossen. Die Kühlfalle besteht aus einem Abscheidegefäß, das in flüssigen Stickstoff taucht, welcher sich in einem DEWAR- Gefäß befindet. Nun wird Hahn A geschlossen und die Vakuumpumpe auf Betriebtemperatur gebracht. Bevor die Kühlfalle aufgebaut werden kann, müssen alle Schliffe mit Aceton gereinigt und anschließend gefettet werden. Dann wird der Rückflusskühler mit dem 100-ml Zweihalskolben „blindgeflanscht“. Nun wird Hahn C geschlossen und Hahn B geöffnet und Hahn A wird so eingestellt, dass die Apparatur bis ca. 1,0 mbar evakuiert werden kann. Wenn Hahn B wieder geschlossen wird, darf sich das Vakuum nur geringfügig ändern. Ändert es sich doch erheblich, müssen die Schliffe erneut überprüft werden. Wenn alles dicht ist, wird Hahn C geöffnet und die Messung kann beginnen. 7 In den 2-Halkolben wird jetzt so viel Ethanol gefüllt, bis das Thermometer ca. 1 cm in die Flüssigkeit taucht. Die Flüssigkeit wird mit einem Rührer gerührt, damit sich die Kälte besser verteilen kann. Hahn C kann nun wieder geschlossen werden. In der Kunststoffschale kann nun Kältebad aus Eis und Wasser hergestellt werden. Der 2Halskolben wird nun bis zum Halsansatz in das Kältebad getaucht. Auch das Kältebad soll gerührt werden. Wenn eine konstante Temperatur erreicht ist, wird der Hahn B geöffnet und die Messapparatur wird bis zum Sieden Evakuiert. Hahn B muss nun schnell wieder geschlossen werden. Der nun entstehende Druck ist zu notieren. Für die nächsten Messungen wird die Temperatur im Kältebad durch Entnahme von Eis erhöht. Die Apparatur soll zwischendurch nicht erneut evakuiert werden. Messergebnisse: Messung 1: Temperatur [K] 1/T 273 275 277 279 281 283 285 287 289 291 293 Druck [mbar] 0,003663 0,00363636 0,00361011 0,00358423 0,00355872 0,00353357 0,00350877 0,00348432 0,00346021 0,00343643 0,00341297 ln(p) 19,9 23,1 26 28,7 32,3 34,9 38,8 44,5 47,8 50,6 53,3 2,99071973 3,13983262 3,25809654 3,35689712 3,47506723 3,55248683 3,65842025 3,79548919 3,86702564 3,92395158 3,97593633 Druck 1 [kPa]Druck 1,99 2,31 2,6 2,87 3,23 3,49 3,88 4,45 4,78 5,06 5,33 ln(p1) 0,68813464 0,83724752 0,95551145 1,05431203 1,17248214 1,24990174 1,35583515 1,4929041 1,56444055 1,62136648 1,67335124 Messung 2: Temperatur [K] 1/T 273 0,003663 275 0,00363636 277 0,00361011 Druck [mbar] ln(p) 17,1 2,83907846 20,3 3,01062089 23 3,13549422 Druck 2 [kPa ] ln(p2) 1,71 0,53649337 2,03 0,70803579 2,3 0,83290912 8 279 281 283 285 287 289 291 293 0,00358423 0,00355872 0,00353357 0,00350877 0,00348432 0,00346021 0,00343643 0,00341297 26,1 29,6 33,1 37,8 42,5 45,7 49,2 52 3,26193531 3,38777436 3,49953328 3,6323091 3,74950408 3,8220983 3,89589362 3,95124372 2,61 2,96 3,31 3,78 4,25 4,57 4,92 5,2 0,95935022 1,08518927 1,19694819 1,32972401 1,44691898 1,5195132 1,59330853 1,64865863 Graphische Auswertung: y(M1) = -3988,5x + 15,343 5 y(M2) = -4511,6x + 17,119 4,5 4 y(DDB1) = -5158,4x + 19,358 3,5 y(DDB2) = -4998,4x + 18,861 3 2,5 2 1,5 1 0,5 0 0,0029 0,00315 0,0034 0,00365 Messung 1 Messung 2 DDB1 DDB2 Linear (DDB2) Linear (DDB1) Linear (Messung 1) 0,0039 Linear (Messung 2) HV HV m R . Somit R folgt hier für die von uns bestimmten Werte und die Vergleichswerte aus der Dortmunder Datenbank: J kJ H V (3988,5K ) 8,314 33,16 mol K mol J kJ H V (4511,5K ) 8,314 37,51 mol K mol J kJ H V (5158,4 K ) 8,314 42,89 mol K mol J kJ H V (4998,4 K ) 8,314 41,56 mol K mol Für die Verdampfungsenthalpie von Ethanol gilt: m i Prof. Dr. K. Al-Shamery, Physikalische Chemie: Versuchsskript SS 06 9