docx
Werbung

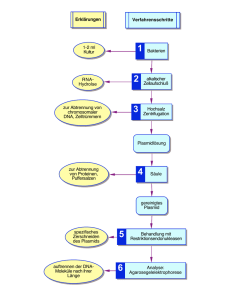
Ausarbeitung zum Seminarvortrag „Possibility of Application of Cytochrome P450 to bioremediation of dioxins“ Einleitung Dioxine sind eine Stoffgruppe verschiedener chemischer Strukturen, in denen zwei Phenylgruppen enthalten sind, welche unterschiedlich verbunden sein können. So sind polychlorierte Dibenzo-pDioxine (PCDD) durch eine Dioxingruppe, polychlorierte Dibenzo-p-Furane (PCDF) durch eine Furangruppe und polychlorierte Biphenyle (PCB) durch eine einfache kovalente Bindung miteinander verbunden. Der Substituierungsgrad mit Halogenen bestimmt dabei die Toxizität. So ist 2,3,7,8Dibenzo-p-Dioxin, auch das Seveso-Toxin genannt, das toxischste Dioxin und gleichzeitig eines der hartnäckigsten Stoffe bezogen auf seine Abbaubarkeit. Es ist bekannt als Einsatz im Vietnamkrieg als „Agent Orange“ zur Entlaubung der Wälder zur Zerstörung von Vietkongverstecken, vom „Sevesounglück“ in der ICMESA-Fabrik in der Region um Seveso und als Toxikum, welches Wladimir Juschtschenko 2004 verabreicht wurde. Es hat eine besonders hohe Halbwertszeit, ich äußerst hydrophob und bleibt deshalb nach Inkorporation überdauert lange Zeitspannen im Leber- und Fettgewebe von Tieren ohne nennenswert abgebaut zu werden. Es steht somit in besonderen Interesse, dass Systeme zum Abbau von PCDD/F und PCB auch zum Abbau von 2,3,7,8-TCDD befähigt sind. Dioxine entstehen natürlicherweise durch Verbrennungsprozesse unter Anwesenheit von Chlorsalzen wie NaCl oder KCl bei Temperaturen von 300 bis circa 600 °C. Waldbrände und vulkanische Aktivitäten sind natürliche Quellen von Dioxinen. Bestimmte industrielle Prozesse sowie Müllverbrennungsanlagen sind durch den Menschen bewirkte Dioxinquellen. Dioxine werden nach ihrer Entstehung durch die Luft verbreitet und lagern sich in lipophilen Milieus oder an Partikeln an. Somit sind nur wenig Dioxine in der freien Luft oder in Wasser enthalten, jedoch sedimentieren sie in den Boden und reichern sich dort an. Durch ihre Hydrophobizität können sie nach Aufnahme in einen tierischen Organismus im Fett- und Lebergewebe lange überdauern. So reichern sich Dioxine innerhalb der Nahrungskette an, besonders in fettreichen Tieren wie Lachs. Die genaue Pathogenese von Dioxinen im menschlichen Körper ist noch nicht verstanden, allerdings ist bekannt, dass Dioxine an den „aryl hydrocarbon receptor“ (ahr) binden, welcher in den Zellkern eindringt und dort auf die Transkription Einfluss nimmt. Ahr steuert zum Beispiel die Transkription von CYP1A1 und dient somit als Abwehrmechanismus gegen unerwünschte aromatische Verbindungen in Zellen. Außerdem nimmt ahr Einfluss auf die Ontogenese. Unter Dioxineinfluss entsteht als erstes sichtbares Symptom Chlorakne. Dabei kommt es zur Umwandlung von Hautdrüsen zu Keratinozyten und führt zu dem typischen, unangenehmen Erscheinungsbild. Neben Chlorakne entstehen oftmals Organschäden vor allem an der Leber. Diese können sich in Form von Übelkeit bemerkbar machen und können bis hin zum Organversagen führen. Es gibt Hinweise auf einen Zusammenhang zwischen dem vermehrten Auftreten von „soft tissue sarcomae“ (STS) in Gebieten um Müllverbrennungsanlagen. Ein weiterer oftmals beobachteter Effekt in Zusammenhang mit Dioxinexposition ist Teratogenität. Maßnahmen gegen Dioxine Die aktuell getroffenen Maßnahmen zur Reduzierung von Dioxinen ist einerseits die Vermeidung der Dioxinentstehung und die Verbrennung kontaminierter industrieller Abfälle bei Temperaturen von 850-1000 °C. Seit den 1980er Jahren werden bereits Maßnahmen zur Vermeidung getroffen und es bestehen einige Gremien zur Bekämpfung von Dioxinen, woraus auch einige wirkungsvolle Übereinkünfte getroffen wurden wie das Stockholmer Übereinkommen zur Vermeidung von POPs (persistent organic pollutants). Halogenatmer Es gibt zahlreiche Untersuchungen zum Abbau von Dioxinen, vor allem mit Cytochrom P450 (CYP). Es gibt aber auch andere Abbauweisen, wie zum Beispiel bei Dehalococcoides spec.. Dieser Genus kann unter anaeroben Bedingungen Dioxine (auch das besonders toxische 2,3,7,8-TCDD) als terminalen Elektronenakzeptor nutzen und somit Abbauen. Diese Organismen wären somit potenzielle Kandidaten zum Abbau von Dioxinen in kontaminierten Gewässern und Klärschlamm. Prokaryotische CYP Das Bakterium Bacillus megaterium synthetisiert CYP102A1, welches eine wasserlösliche Fusion von CYP und einer NADPH-Reduktase darstellt. Sulistyaningdyah et al. haben drei gezielte Mutationen an diesem CYP durchgeführt und konnten damit eine Steigerung der Aktivität bewirken. Diese Mutante war nicht zum Abbau von 2,3,7,8-TCDD in der Lage, dafür aber zu einem sehr effektiven Abbau von triCDD zu biCDD. BiCDD hat nur 5% der Toxizität von 2,3,7,8-TCDD. Eukaryotische CYP – P. chrysosporium P. chrysosporium ist bekannt für seine zahlreichen exkretierten Enzyme, welche bei Verrottungsprozessen unter anderem bei Bäumen eine große Rolle spielen. P. chrysosporium codiert darüber hinaus für 148 CYPs. Bei Verrottungsprozessen bewirken diese zahlreichen Enzyme eine Vielzahl von Dekontaminationsreaktionen. Bumpus et al. haben 2,3,7,8-TCDD-Aktivität dieser Cytochrome beschrieben, welche jedoch von den Autoren (Sakaki et al.) nicht bestätigt werden konnte. Eukaryotische CYP – Säugetier CYP1A1 (Mensch und Ratte) Sakaki et al. haben verschiedene CYPs von Ratten und Menschen auf ihre PCDD-Aktivität untersucht. CYP1A1 hat sich dabei als besonders effektiv herausgestellt und zeigte hohe Affinität zu mono-, biund triCDD. Es wurde keine Aktivität von 2,3,7,8-TCDD festgestellt. Deshalb wurden vier besonders große Residuen (Phenylalanin) in der Bindetasche der Ratten-CYP1A1 indentifiziert und durch kleinere Residuen ersetzt, mit dem Ergebnis, dass die mutierte CYP1A1 2,3,7,8-TCDD-Aktivität aufwies. Anwendung von CYP zur Degradation von Dioxinen Das einbringen von genetisch veränderten Mikroorganismen („genetic engineered microorganisms, GEM) ist auf Grund ethischer und ökologischer Bedenken unmöglich. Es wurden deshalb Anstrengungen bewirkt, verfolgbare Organismen zu erschaffen, jedoch ohne Erfolg. Heute hat man die Möglichkeit, selbst-tötende GEM zu schaffen, welche auf einem Toxin-Antigift-Plasmidsystem basieren. In diesem Plasmid ist ein gewünschtes Gen (z.B. für ein dioxinumsetzendes CYP) enthalten. Außerdem ist entweder genomisch oder auf dem Plasmid selbst ein Gen für ein Zellgift und ein kurzlebiges Gegengift enthalten. Das Plasmid enthält ein den abzulesenden Genen vorgeschalteten Promotor, welcher durch Dioxine induzierbar ist. So überlebt der GEM auf dioxinhaltigem Grund, stirbt aber ab, sobald kein Dioxin mehr vorhanden ist. Wenn man vermeiden möchte, dass das Plasmid weitergegeben wird, kann man das Toxin konstituiv auf dem Plasmid exprimieren und das Gegengift genomisch exprimieren lassen. Dieser Vorschlag wirkt vielversprechend, es gibt jedoch einige Bedenken für den Einsatz von sogenannten „suicidal GEMs“ (sGEMs). Rekombination und Mutation könnte zu einer Desensibilisierung des Organismus gegen das Toxin kommen, oder der Promotor könnte konstituiv exprimieren. Außerdem müsste der Promotor sehr sensibel gegenüber Dioxinen sein, da schwierig ist festzustellen, inwiefern die Kontamination dekontaminiert ist, wenn die Dioxinkonzentrationen nicht mehr ausreichen um den Promotor auf dem Plasmid zu induzieren und der Organismus abstirbt. Kris Hippler (25 55 587) 19.11.2015