Katalysator - Einführung
Werbung

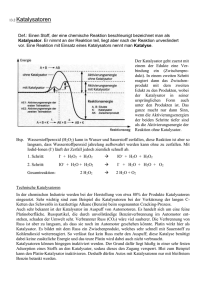
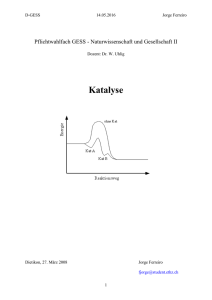
Der Firecat® Katalysator Was ist Katalyse? Katalyse ist ein Prozess bei der die Geschwindigkeit einer chemischen Reaktion durch eine bestimmte Substanz verändert wird. Diese Substanz wird Katalysator genannt. Im Gegensatz zu anderen Reagenzien, die an einer chemischen Reaktion teilnehmen, wird der Katalysator nicht von der Reaktion selbst aufgelöst. Doch obwohl Katalysatoren nicht direkt durch die Reaktion aufgelöst werden, können sie durch einen sekundären Prozess gebremst, deaktiviert oder zerstört werden. Bei der heterogenen Katalyse ist etwa Verkoken ein typischer sekundärer Prozess, bei welchem der Katalysator von polymeren Nebenprodukten bedeckt wird. Katalysatoren verändern nicht das Ausmaß einer Reaktion: sie haben keinen Effekt auf das chemische Gleichgewicht einer Reaktion, da sowohl die Geschwindigkeit der Reaktion als auch der Gegenreaktion verändert werden (siehe Thermodynamik). Die Tatsache, dass ein Katalysator nicht das Gleichgewicht verändert, ist eine Konsequenz des zweiten Hauptsatzes der Wärmelehre. Nehmen wir an, es gäbe einen Katalysator, der das Gleichgewicht veränderte. Der Einbau des Katalysators in das System würde bewirken, dass sich das Gleichgewicht in Richtung eines neuen verschieben; also Energie erzeugen würde. Die Erzeugung von Energie wäre zwangsläufig, da Reaktionen, wenn – und nur wenn – Gibbssche freie Energie produziert wird, spontan sind. Und wenn es keine Energiebarriere gibt, braucht man auch keinen Katalysator. Die Entfernung des Katalysators anschließend würde ebenfalls im Gewinn von Energie resultieren, das andauernde Ein- und Ausbauen des Katalysators würde also wie ein Kraftwerk wirken. Ein Katalysator, der das Gleichgewicht verändern könnte, wäre demnach ein Perpetuum Mobile erster Art, ein Widerspruch zu den Gesetzen der Wärmelehre. (http://de.wikipedia.org/wiki/Katalyse) Auch wenn Katalysatoren in unzähligen Gebieten in der Chemie, Nahrungsverarbeitung, Malerei, Beschichtung, Laminierung, Emissionsreduktion, etc. verwendet werden, interessieren wir uns an dieser Stelle nur für die kleine Gruppe der sogenannten „Oxidationskatalysatoren“. Oxidationskatalyse funktioniert wie folgt: Zunächst wird aus O2 2O, welches anschließend in der Grundierung instabile chemische Reagenzien mit Edelmetallpartikeln bildet. Konkret handelt es sich um Palladium (Pd), Platin (Pt) und Rhodium (Rh). Auf diese Weise wird verbleibender Sauerstoff, der andernfalls einfach durch den Kamin entweichen würde, zurückgehalten und bildet ein Umfeld mit zusätzlichem Sauerstoff; heiße, sehr reaktionsfreudige, freie Sauerstoffradikale. Da die molekularen Kräfte zwischen O und Edelmetallen sehr gering sind (was auch der Grund dafür ist, dass sie „Edel“ sind), kann sich O auch sehr leicht vom Metall trennen und stärker reagierende Verbindungen wie CO eingehen: Andererseits: Da die Oxidation von freien Sauerstoffradikalen eine Folge ihrer Effizienz ist, ist verständlich, warum Edelmetallkatalysatoren mehr oder weniger jede chemische “brennbare” Verbindung oxidieren können; wenn auch bei verschiedenen Geschwindigkeiten und Temperaturen… … wodurch CO2 und H2O (Dampf) als Abgase zurückbleiben. Nachdem wir jetzt das Thema Effizienz hinter uns gebracht haben, wollen wir uns ansehen, wie der Katalysator aufgebaut ist. Wir verwenden mit Edelmetallpartikeln überzogenes Cordierit als Substrat. Cordierit wird charakterisiert durch Hohe Porösität: wodurch es sich leicht überziehen und damit die Oberfläche so rau wie möglich gestalten lässt Geringe thermische Ausdehnung: Cordierit dehnt sich unter Hitze kaum aus, wodurch es sehr stabil ist und die Grundierung lange haftet Doch auch die Oberfläche des bestgeeignetsten keramischen Trägermaterials ist nicht sonderlich hoch. Eine Möglichkeit, diese zu erhöhen, ist die Form (Honeycombs), welche durch ein Kaltpressverfahren erlangt wird. Die Struktur gewöhnlicher Keramik lässt sich übrigens sehr gut mit der glatten Seite einer Duschkabinentür vergleichen. Spritzt man Wasser auf eine ebene, glatte Glasplatte, breitet sich das Wasser auf wenige große Lacken aus. Das liegt an der geringen Oberfläche. Wir wollen dagegen eine möglichst hohe Oberfläche, vergleichbar der rauen Seite der Duschkabine. Wird Wasser auf diese gespritzt, breitet es sich weit aus und bedeckt ein großes Gebiet. Wir erreichen diesen Effekt durch die Verwendung einer Grundierung. Das am häufigsten verwendete Material hierfür ist Gamma-Aluminium. Aluminium verfügt über viele Phasen, doch die höchste Oberfläche hat es in der Gammaphase. Einer der Gründe, warum man den Katalysator von direktem Flammkontakt fern und die Temperatur unter 815°C halten sollte, ist, dass sich Gamma-Aluminium ab dieser Temperatur in Alpha-Aluminium verwandelt. Damit würde es einen großen Teil seiner Oberfläche und katalytische Aktivität verlieren. Das Gamma-Aluminium wird als Schlicker angebracht und später durch große Hitze pulverisiert. Dieser Vorgang erhöht die Oberfläche enorm: ein so überzogenes Substrat verfügt über die 2000-fache Oberfläche eines unbehandelten Grundgerüsts und ist damit bereit für die Verwendung als Katalysator. Die meisten herkömmlichen Katalysatoren sind aus der Gruppe der Übergangsmetalle. Darin sind sowohl Edel- als auch gewöhnliche Metalle. Unsere Wahl war die Verwendung der Edelmetalle Platin und Palladium, da diese exzellente Katalysatoren zur Oxidation sowie äußerst robust und bei dieser Anwendung langlebig sind. Die Metalle werden einer Lösung beigefügt und finden anschließend auf verschiedene Weise in die Grundierung eingefügt, unter anderem mittels Sprüh- und Tauschbeschichtungsverfahren. Die Technik ist weniger wichtig als die Einschränkungen, um gewährleisten dass das Gewicht des Metalls weder zu hoch noch zu leicht und überall etwa gleich ist. Zu viel Metall ist Geldverschwendung , da der diffusions-kontrollierte Prozess der katalytischen Oxidation wie jede Verbrennung durch die relative Faktoren Zeit, Temperatur und Unregelmäßigkeit bestimmt wird. Wird dagegen die richtige Menge an Metall verwendet, beeinflusst zusätzliches Metall die Effizienz weniger als die Lebensdauer, speziell bei falscher Anwendung. Nach der Anwendung werden die mit Metall überzogenen Teile erneut kalziniert, um das Metall an der Oberfläche zu fixieren. Cordierit mit Grundierung und Edelmetallpartikeln. Rot-glühender Katalysator in Aktion