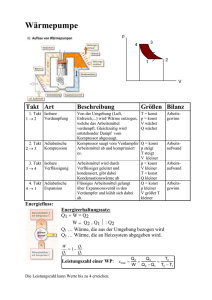
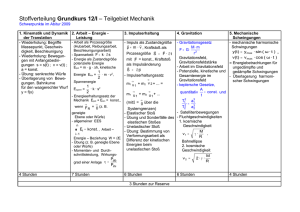
pV = konst.
Werbung

Physik für Mediziner, Zahnmediziner und Pharmazeuten SS2000 14.Vorlesung 26.5.2000 1 Prof. Dr. Alois Putzer Zurück zur ersten Seite Plan : Nächste Vorlesungen Heute Strömungen, Blutkreislauf Anschließend : Wärme Übungsblatt : (Lösungen werden in der Vorlesung besprochen +Internet) Folien ab jetzt auch als .pdf files (6 Folien / Seite) 2 Zurück zur ersten Seite Hagen-Poiseuille Das Hagen-Poiseuille Gesetz beschreibt die Strömung einer Flüssigkeit durch ein Rohr mit Radius R, Länge L und einer Druckdifferenz p Für den Volumenstrom (Volumen/Zeit) erhält man: 4 V R p IV t 8 L Anwendungsbeispiel : Blutkreislauf 3 Zurück zur ersten Seite Stokes Das Gesetz von Stokes beschreibt die Bewegung einer Kugel durch eine Flüssigkeit. Auf diese Kugel wirken die Gewichtskraft G, die Auftriebskraft FA und die Reibungskraft FS. F ma G FS FA FS 6 RvS (Stokessch e Formel) Wenn keine resultierende Kraft mehr auf die Kugel wirkt, nimmt die Kugel eine konstante Geschwindigkeit vS ein (Sedimentationsgeschwindigkeit). Aus der Sedimentationsgeschwindigkeit läßt sich die Zähigkeit der Flüssigkeit berechnen. 4 Zurück zur ersten Seite Anwendung: Blutsenkung Laminare und turbulente Strömung Reynoldsche-Zahl Re 2 R v Fl. Kapillaren : Re=0,01:lamina r Aorta: Re=5000:turbulent 5 Zurück zur ersten Seite Strömungsvorgänge Strömung von Flüssigkeiten(später auch von Wärme und Elektrizität) Im menschlichen Körper spielen Ströme eine wichtige Rolle Transport energiereicher Moleküle zu den Zellen Sauerstofftransport im Blut Transport von Medikamenten. 6 Zurück zur ersten Seite Strömungswiderstand Analog zum Ohmschen Gesetz : U = R I Δ p R V IV 8 L RV 4 R 7 Zurück zur ersten Seite Blutkreislauf 8 Zurück zur ersten Seite Wärme Temperatur, Wärmemenge, -kapazität Versuch: Wärmekapazität Ausdehnung Gasgesetze Osmose, Diffusion (Stoffaustausch) Tiefe Temperaturen Lokalanästhesie,Kältetherapie Wärmestrahlung, Wärmeleitung Grundumsatz, Wärmehaushalt 9 Zurück zur ersten Seite Temperaturabhängige Größen Aggregatzustand Länge (Volumen) Elektrische Leitfähigkeit Schallgeschwindigkeit Reaktionsgeschwindigkeit 10 Zurück zur ersten Seite Temperatur : Maß für die mittlere Energie der Moleküle Einheit der Temperatur T : [K] (Kelvin) Für Wasser bei Athmosphärendruck: Gefrierpunkt : 0 °C = 273,15 K Siedepunkt : 100 °C = 373,15 K Chemische Reaktionen im Körper sind stark temperaturabhängig => Kerntemperatur muß annäher nd konstant gehalten werden. 11 Zurück zur ersten Seite Wärmemenge und Wärmekapazität Wärmemenge (Wärmeenergie): Q [J] 1 J = 0,239 cal (Kalorie) 1 cal = 4,19 J = Wärmemenge, um 1g Wasser von 14,5 °C auf 15,5 °C zu erwärmen Zusammenhang zwischen Wärmemenge Temperaturänderung: ΔQ C ΔT c m ΔT C=Wärmekapazität des Körpers : [J/K] c=spezifischeWärmekapazität : [J/gK] 12 Zurück zur ersten Seite Längen- (Volumen-) Ausdehnung Längenänderung l(T) l0 (1 αΔ T) α linearer Ausdehnung skoeffizie nt Volumenänderung V(T) V0 (1 βΔ T) β 3α (für α klein) Bei thermischen Dehnungen treten sehr große Kräfte auf. Spannungen treten bei Temperaturänderung auf, wenn man Materialien mit verschiedenen Ausdehnungskoeffizienten fest miteinander verbindet. (Bi-Metall, Implantate) 13 Zurück zur ersten Seite Ruhende Gase 3 Zustandsgrößen : Volumen V, Druck p und Temperatur T Gasmoleküle bewegen sich statistisch (Brownsche Molekularbewegung) Gesetz von Boyle-Mariotte: p V = konst. (T = konst.) 14 Zurück zur ersten Seite Isotherme (gleiche Temperatur) pV = konst. (T=konst.) 15 Zurück zur ersten Seite Luftdruck Am Erdboden: Dichte : 1,2 kg/m³ Druck : 1013 hPa Luftdruck und Dichte nehmen exponentiell mit der Höhe ab. 16 Zurück zur ersten Seite Geschwindigkeitsverteilung der Gasmoleküle für verschiedene T. 17 Zurück zur ersten Seite Wärme als thermische Energie Ther mische Energie = kinetische und potentielle Energie der Moleküle. Bei Gasen tritt nur kinetische Energie auf. Die Gesamtenergie(Wkin) ist die Summe der kinetischen Energien aller Gasmoleküle. Bei jedem Stoß der Gasmoleküle an die Gefäßwand wird der Impuls p=2mv übertragen. pV = 2/3 Wkin Bei steigender Temperatur steigt die kinetische Energie der Gasmoleküle. 18 Zurück zur ersten Seite Ausdehnung von Gasen(1) Normzustand (V0) festgelegt bei: T = 273,15 K , p = 1013 hPa Gase haben nur Volumenänderung: Bei isobarer Erwärmung (p=konst.) 1 1 K 273,15 ΔT V(T) V0 (1 ) 273,15K Bei 0K (absoluter Nullpunkt) ist für ideale 19 Gase V(T) = 0. Zurück zur ersten Seite Ausdehnung von Gasen(2) Bei isochorer Erwärmung (V=konst.) Isotherme (T=konst.) ΔT p(T) p 0 (1 ) 273,15K pV Isochore (V=konst.) p proportional T Isobare (p=konst.) V = konst proportional T Für ideale Gase: .pV 20 = N k T = n R T (Erklärung später) Zurück zur ersten Seite Zustandsgleichung (Ideale Gase) Unter Normalbedingungen nimmt 1 mol eines idealen Gases das Molvolumen = 22,41 Liter ein. Zustandsgleichung für 1 mol pV = NA k T = R T k = 1,38 10-23 J/K (Boltzmann-Konst.) R = 8,31 J/(mol K)= molare Gaskonstante Für beliebige Gasmengen: p V=nRT n = Anzahl der Mole 21 Zurück zur ersten Seite