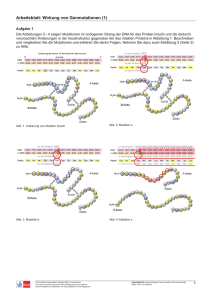
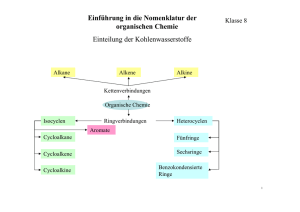
Ionisation
Werbung

Massenspektrometrie Seminar WiSe 2015/2016 PD Dr. Markus Nett Nachwuchsgruppenleiter L ib i I i für Leibniz‐Institut fü Naturstoff‐Forschung N ff F h und Infektionsbiologie d I f k i bi l i E‐mail: markus.nett@hki‐jena.de Grundvorgänge der Massenspektrometrie Ionisierung Fragmentierung MassenFokussierung Zerfall in geladene und ungeladene Bruchstücke Trennung der gebildeten Bruchstücke nach ihrer Masse -2- Wie werden organische Substanzen ionisiert? durch Beschuss der Probenmoleküle mit Elektronen, Ionen oder Photonen Elektronenstoß-Ionisation Elektronenstoß Ionisation (EI) Chemische Ionisation (CI) Fast-Atom-Bombardment (FAB) Matrix Matrix-unterstützte unterstützte Laserdesorptions Laserdesorptions-Ionisation Ionisation (MALDI) durch elektrische Felder Elektrospray-Ionisation (ESI) -3- Elektronenstoß-Ionisation (EI) Glühkathode Elektronenstrahl Hochvakuum 10-4 – 10-7 Torr Spalte, elektr. Linsensysteme + + Vakuumschleuse mit Probenheizung + + + + + positive Ionen → Massenanalysator y Elektronenauffänger Hochvakuumpumpe Beschuss mit energiereichen Elektronen (70 eV) “harte” Ionisierung (Ionisierungspotential: 7-15 eV) Spaltung chemischer Bindungen unter Bildung zahlreicher Fragmentionen -4- Chemische Ionisation (CI) Glühk th d Glühkathode 0,2 – 2 Torr Elektronenstrahl (150 eV) Probenmoleküle Ionenstrom zum Massenanalysator Elektronenauffänger Linsensystem der Ionenquelle Reaktandgas Reaktandgas wird durch Elektronenbeschuss ionisiert Protonenübertragung durch Zusammenstöße mit weiteren Reaktandgas-Molekülen Reaktion mit dem gasförmigen Analyt unter Bildung von [M+H]+-Ionen -5- Chemische Ionisation – theoretische Grundlagen Prinzip: Ionisation erfolgt durch Ionenmolekülreaktion mit einem im Überschuß zugesetzten Reaktandgas R, z.B. Methan, Isobutan, H2, NH3, ... Primärreaktion: Ionisation des Reaktandgases R mit hoher Energie (~150 eV) R + e– R+• + 2e– (Ionisation) R+• + R RH+ + R • (Protonierung) Sekundärreaktionen: zwischen RH+ und dem Molekül M RH+ + M MH+ + R (Protonierung) [M+1]-Ion RH+ + M M-H+ + R + H2 ((H-Abstraktion)) [M-1]-Ion RH+ + M MRH+ [M+RX]-Ion -6- (Anlagerung) Fast-Atom-Bombardment (FAB) Primärpartikel (Ar, Xe) Hochvakuum Sekundärpartikel Neutralteilchen, Ionen, Elektronen Selvedge Region Matrix Analyt Analyt in einer flüssigen, schwer flüchtigen Matrix Beschuß mit 5-30 keV-Partikeln Zerstäubung der Matrix, Stosskaskade, Bildung von Sekundärpartikeln -7- Matrix-unterstützte Laserdesorptions-Ionisation (MALDI) Laserstrahl Analyt-Ion zum Massenanalysator Matrix-Ion Matrix/Analyt Analyt in einer flüssigen Matrix Ionisation mit einem gepulsten Laserstrahl Beschleunigung der entstandenen Ionen in einem elektrischen Feld -8- Elektrospray-Ionisation (ESI) – Prinzip Auslaß Stickstoff: nebulizer-gas Atmosphärendruck Gegenelektrode – Spraybildung + – Kapillare gelöste Probe Transferoptik + – + + Spülgas ((bath-gas, g Stickstoff)) + Mikroöffnung (sample cone) + + – Ionen zum Hochvakuum und Massenanalysator + – Skimmer 2–6 kV Zerstäubung der Probenlösung in einem elektrischen Feld Verdampfung des Lösungsmittels => Coulomb-Explosion Detektion von Quasi-Molekülionen, v.a. [M+H]+ und [M+Na]+ bzw. [M-H]– -9- Massenspektrum Darstellung der Ionenhäufigkeit über das Masse-Ladungsverhältnis m/z, normiert auf den Peak mit der größten Häufigkeit (Basispeak: I = 100%) Basispeak Fragmentpeaks 75 eV-EI-MS von Myrcen 41 93 69 + Molpeak M • 136 - 10 - m/z rel. Intensität 41 69 93 136 100 % 78 % 94 % 6% Identifizierung des Molpeaks in EI-MS-Spektren meist die höchste auftretende Massenzahl Peak kann sehr geringe Intensität aufweisen (Fragmentierung) Abnahme der Intensität des Molpeaks - 11 - Identifizierung des Molpeaks in EI-MS-Spektren Plausible Massendifferenzen zu den nächsten Signalen? Δ4 - 14 sowie Δ21 - 25 zwischen Molpeak und erstem Fragmentpeak sind unwahrscheinlich. Der Molpeak ist immer ein Radikalkation M+• ungerade Elektronenzahl (OE+• , odd electron) I mitit einer Ion i geraden d Elektronenzahl El kt hl (EE+, even electron) l t ) C - Atome - F Fragmentpeak t k H - Atome N - Atome 1 2 2 ja OE+• nein EE+ Ergebnis gerade? - 12 - Identifizierung des Molpeaks – Übungsaufgabe Durch peak matching wurde die Elementarzusammensetzung der folgenden Ionen bestimmt. Welches Ion kommt als Molpeak in Betracht? I #1 Ion #1: C10H14O Ion #2: C6H8NO2 - 13 - Informationen aus dem Signal des Molpeaks Summenformel Stickstoffregel • Eine ungerade Massenzahl des Molekülions weist auf das Vorhandensein einer ungeraden Zahl von N-Atomen im Molekül hin. • Ist die Massenzahl dagegen geradzahlig, enthält das Molekül entweder gar keinen Stickstoff oder eine gerade Zahl von N-Atomen N Atomen. Isotopenmuster Hinweis auf das Vorkommen von Cl, Cl Br, Br Ni, Ni Cu Cu, Zn Zn, etc etc. - 14 - Hochauflösende Massenspektrometrie Mit Ausnahme des Kohlenstoffisotops 12C sind die Atommassen der Elemente nicht ganzzahlig. 1 14 16 => Massendefekt H hat eine Atommasse von 1.007825 u N hat eine Atommasse von 14.003074 14 003074 u O hat eine Atommasse von 15.994915 u Wenn die Massenzahl eines Ions auf mindestens vier Dezimalstellen genau bestimmt werden kann,, so läßt sich dessen monoisotopische g p elementare Zusammensetzung berechnen. Bestimmung der Summenformel - 15 - Peak-matching-Methode Die experimentell bestimmte Masse wird mit der exakten Masse einer Referenzsubstanz verglichen. In dem folgenden Beispiel wurde die Masse des Molekülions mit 566,2179 u bestimmt: - 16 - Abschätzen der Summenformel mit der „Rule of 13“ 1 Abstraktion: das Molekül besteht nur aus C- und H-Atomen; die Zahl 13 entspricht der Summe der Atommassen eines C- und eines H-Atoms M: Molekulargewicht M/13 = n + r/13 /13 n: ganzzahliger Anteil r: Summenformel: Rest CnHn+r Der Grad der Ungesättigtheit, d.h. die Anzahl der Doppelbindungen und/oder Ringe in dem potentiellen Molekül, berechnet sich nach der Formel: DBE = (n – r + 2)/2 J. Chem. Educ. 1983, 60, 557-558 - 17 - „Rule of 13“ – Übungsaufgabe 1 Bestimmen Sie die Summenformel und den Grad an Ungesättigtheit für ein Molekülion mit der Masse 78. Um was für eine Verbindung könnte es sich handeln? - 18 - Abschätzen der Summenformel mit der „Rule of 13“ 2 Für die Erweiterung der Summenformel CnHn+r um andere Elemente muss zunächst das CH-Massenäquivalent subtrahiert werden. Element CH-Äquivalent N CH2 O CH4 F CH7 P C2H7 S C2H8 35 Cl C2H11 79 Br C6H7 od. C5H19 I DBE = 2C + 2 – H + j Σ(B – 2) 2 C: Anzahl C-Atome in der erweiterten Summenformel H: Anzahl H-Atome in der erweiterten Summenformel j: Anzahl der eingeführten Atome B: Anzahl der Bindungen, die das eingeführte Atom eingeht C10H7 J. Chem. Educ. 1983, 60, 557-558 - 19 - „Rule of 13“ – Übungsaufgabe 2 Bestimmen Sie die Summenformel und den Grad an Ungesättigtheit für ein Molekülion mit der Masse 142, das entweder (i) ein Sauerstoffatom oder (ii) ein Chloratom enthält. - 20 - „Rule of 13“ – Übungsaufgabe 3 Sie erhalten EI-MS- und IR-Spektrum einer nicht identifizierten Verbindung. Machen Sie einen Vorschlag zu der Summenformel des betreffenden Moleküls nach Auswertung der Spektren. Um was für eine Verbindung könnte es sich handeln? 4000 3000 - 21 - 2000 1500 1000 500 Doppelbindungsäquivalente (DBE) Berechnung Doppelbindungsäquivalente 1. O- und S-Atome in der Summenformel ersatzlos streichen 2. jedes Halogen durch ein H-Atom ersetzen 3. für jedes N- und/oder P-Atom die Anzahl der H-Atome um 1 reduzieren (2 x n + 2) – m DBE = 2 jede Doppelbindung = 1 DBE jeder Ring = 1 DBE jede Dreifachbindung = 2 DBE z.B. C=C, C=O, C=N, C=S, N=O, N=N, S=O z.B. C≡C, C≡N - 22 - n: Anzahl der C-Atome m: Anzahl der H-Atome Doppelbindungsäquivalente (DBE) – Anwendungsbeispiele Im Falle eines gesättigten, acyclischen Kohlenwasserstoffs gilt: m = 2 x n +2 (2 x n +2) – (2 x n + 2) DBE = =0 2 Verbindung Summenformel Anzahl Doppelbindungen Anzahl Ringe C6H6 3 1 (2 x 6 +2) 2) – 6 2 =4 Essigsäure C2H4O2 1 0 (2 x 2 +2) – 4 2 =1 Ethanol C2H6O 0 0 (2 x 2 +2) – 6 2 =0 C2H5NO2 1 0 (2 x 2 +2) – 4 2 =1 C8H10O2N4 4 (2 x 8 +2) – 6 2 =6 Benzen Glycin Coffein - 23 - 2 DBE Übungsaufgabe 4 Berechnen Sie die Doppelbindungsäquivalente für die folgenden Summenformeln und machen Sie Vorschläge zu den Strukturen der jeweiligen Verbindungen! 1) C5H5N 2)) C10H8 3) C3H4O4 4) C3H5NO - 24 - Isotopenmuster Die natürlich vorkommenden Elemente sind häufig Mischungen aus mehreren Isotopen des gleichen Elements, z.B. 12C/13C (98.90/1.10); 35Cl/37Cl (75.43/24.57); 79Br/81Br (50.44/49.56) In der Massenspektrometrie werden die einzelnen Isotope eines Moleküls getrennt registriert. Isotopenpeaks Die durch Kombination mit den schwereren Isotopen gebildeten Molekülionen liegen bei entsprechend höheren MZ und werden bezeichnet: M+1, M+2, ... Beispiel: CH3Cl MZ 12 C1H335Cl 50 M+• 13 C1H335Cl 51 M+1 (12C2H1H235Cl) 51 M+1 12 52 M+2 52 M+2 C1H337Cl (13C2H1H235Cl) - 25 - sehr geringe Wahrscheinlichkeit sehr geringe Wahrscheinlichkeit Isotopenmuster + Molpeak M • 75 eV-EI-MS von m-Dichlorbenzen m/z rel. Intensität 146 147 148 149 150 100 % 7% 63 % 4% 10 % 146 148 Fragmentpeaks 111 75 50 150 - 26 - Isotopenpeaks Fragmentierungsreaktionen in der EI EI--MS Spaltung einer chem. Bindung Spaltung zweier Bindungen Folgespaltungen • Alkylspaltung • Retro-Diels-Alder-Reaktion • Olefinspaltung • Abspaltung von CO • Allylspaltung • Benzyl-/Tropyliumspaltung • α-Spaltung Umlagerungen • McLafferty-Umlagerung - 27 - • Onium-Umlagerung Fragmentierung bei der EI-MS –e• –e• –e• –e• –e• Molekül Ionisierung + • Molekülion + • NeutralN t l molekül RadikalR dik l Kation + • Neutralmolekül • RadikalKation Radikal • Radikal + Kation + Kation + Neutralmolekül Kation Stephenson-Audier-Regel Die Ladung wird von dem Bruchstück mit dem kleineren Ionisierungspotential übernommen, d.h. von jenem Fragment, das am leichtesten ein Elektron abgeben könnte. Heteroaromaten, Aromaten und konjugierte Polyene besitzen relativ niedrige Ionisierungspotentiale. - 29 - Fragmentierungsreaktionen – allgemeine Prinzipien Fragmentierungs-Reaktionen in der EI-MS sind monomolekular endotherm kinetisch kontrolliert Welche Bindung gespalten wird, hängt ab von der Bindungsenergie der Stabilität der gebildeten Fragmente ? Neutralmoleküle ? durch induktive Effekte, Mesomerie oder Umlagerung stabilisierbare Kationen - 30 - Alkylspaltung (σ-Spaltung) • Spaltung erfolgt an verzweigten C-Atomen • Präferenz für den Verlust des größten Alkylradikals Stabilisierung des CarboCarbo-Kations durch induktive Effekte + + + + CH3 < RCH2 < R2CH < R3C CH3 + • CH3 – CH2 – CH•2 – CH2 – CH2 – C – + +C – CH3 CH3 - 31 - Alkylspaltung (σ-Spaltung) CH3 H3C – CH – CH2 – CH2 – CH2 – CH3 43 43 85 + Molpeak M • 100 Übungsaufgabe 5 Ordnen Sie die den nachfolgenden 43 Stellungsisomeren (C8H18) die zugehörigen MS-Spektren zu: 85 29 57 3-Ethylhexan 114 71 57 2,2-Dimethylhexan 29 99 - 33 - Allylspaltung Spaltung erfolgt in Allylstellung Stabilisierung g des CarboCarbo-Kations durch mesomere Effekte – CH = CH – CH2 – CH2 – – CH = CH – CH2+ + • –+CH – CH = CH2 - 34 - + • CH – 2 Allylspaltung CH3 H3C – C = CH – CH2 – CH2 – CH3 69 69 + Molpeak M • 98 Benzyl- oder Tropyliumspaltung Spaltung erfolgt in der Benzylstellung Stabilisierung g durch Umlagerung g g zum TropyliumTropylium py -Kation + • X• – CH2 – X + – CH2+ Umlagerung + - 36 - Benzyl- oder Tropyliumspaltung BenzylSpaltung + + + C3H7• + H2C = CH – CH3 m/z 91 C6H5 – C4H9 • m/z 134 C6H5 – CH2 + McLaffertyUmlagerung C6H5 – CH3 • m/z 92 91 92 + Molpeak M • 134 α-Spaltung Bei einfach gebundenen Heteroatomen (O, S, N) wird bevorzugt die α-Bindung gespalten, weil das entstehende Kation durch Mesomerie stabilisiert wird. Der schwerere Substituent wird bevorzugt eliminiert. R – X – CH2 – R´ – R – X – CH2+ + + • R – X = CH2 - 38 - + • R´ α-Spaltung H 58 H3C – CH2 – N – CH2 – CH2 – CH3 72 58 + Molpeak M • 87 72 α-Spaltung • Spaltung erfolgt an der zur Carbonylfunktion benachbarten Bindung Stabilisierung des CarboCarbo-Kations durch mesomere Effekte • bevorzugte Eliminierung des größeren Radikals • Säure < Ester < Keton = R – CH2 – C – R´ + • O + + O - 40 - C – R´ ≡ C – R´ = R – CH2• +O α-Spaltung 57 H3C – CH2 – C – CH2 – CH2 – CH2 – CH2 – CH3 = O 99 57 99 + Molpeak M • 128 Retro-Diels-Alder-Reaktion (RDA-Reaktion) • Sechsgliedrige cyclische Systeme, die eine Doppelbindung enthalten, zerfallen in eine Dien- und eine En-Komponente. • Ladung verbleibt i.d.R. am Dien • alternative Ladungsverteilung? Detektion der En-Komponente im MS + • + • + - 42 - Retro-Diels-Alder-Reaktion (RDA-Reaktion) + • + • + m/z 68 m/z 136 68 + Molpeak M • 136 McLafferty-Umlagerung • Übertragung des γ-ständigen H-Atoms auf ein doppelt gebundenes Atom X • X ist meistens ein Heteroatom • Verschiebung der Doppelbindung • Eliminierung eines Neutralteilchens mit den β- und γ-ständigen Atomen +• +• H X α γ β H γ X + α - 44 - β McLafferty-Umlagerung γ β α + H2C = C (OH)2• = H3C – CH2 – CH2 – CH2 – C – OH H3C – CH = CH2 + • m/z 102 O m/z 60 60 Folgespaltungen Die bei der Alkylspaltung entstandenen Kationen können durch Eliminierung von Olefinen weiter fragmentieren (Olefinspaltung): + R – CH2+ R – CH2 – CH2 – C + H2C = C Aus den durch α-Spaltung gebildeten Kationen wird leicht CO eliminiert (CO-Verlust): + C–R CO O - 46 - + R+ CO-Verlust + • OH m/z 94 + • O m/z 66 + CO + Molpeak M • 94 66 Folgespaltungen Die bei der α-Spaltung gebildeten Onium-Ionen können einer Umlagerung unterliegen (Onium-Umlagerung): R – CH2 – CH2 – CH2 – X = C + R – CH2 – CH = CH2 + H–X=C + - 48 - Übungsaufgabe 6 Erläutern Sie die Fragmentierung der abgebildeten Verbindung bei der EI-MS. 205 220 57 - 49 - Übungsaufgabe 7 Erläutern Sie die Fragmentierung der abgebildeten Verbindung bei der EI-MS. - 50 - Übungsaufgabe 8 Erläutern Sie die Fragmentierung der abgebildeten Verbindung bei der EI-MS. 41 93 69 + M• 136 - 51 - Übungsaufgabe 9 Erläutern Sie die Fragmentierung der abgebildeten Verbindung bei der EI-MS. m/z - 52 - Übungsaufgabe 10 Interpretieren Sie das dargestellte MS-Spektrum im Hinblick auf • charakteristische (M – X)-Signale • Schlüsselbruchstücke und Serien • stattgefundene Fragmentierungen Arecolin 140 96 155 53 124