2 - Friedrich-Schiller
Werbung

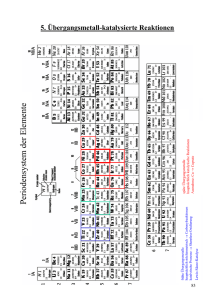
Vanadium(IV)verbindung mit Oxotransferaseaktivität Susanne Kaiser und Winfried Plass Institut für Anorganische und Analytische Chemie, Friedrich-Schiller-Universität Jena Einleitung Eine wesentliche biologische Funktion Molybdän-abhängiger Enzyme besteht in der Katalyse von Sauerstoffatomtransferreaktionen mit gleichzeitigen Zweielektronenübergängen zwischen einem Substrat und räumlich getrennten Einelektronenüberträgern wie Cytochromen, Eisen-Schwefel-Zentren und Flavinen. Diese Oxotransferaseaktivität zeichnet sich durch eine formale Sauerstoffatomübertragung zwischen dem Metallzentrum des Enzyms und dem Substrat aus. Dabei dient im allgemeinen Katalysezyklus dieser sogenannten Oxotransferasen bzw. Hydroxylasen Wasser als Sauerstoffquelle. LMoIVO + XO VI LMo O2 + X Neben diesen Molybdän-abhängigen Enzymen wurde auch eine molybdänfreie Nitrat-Reduktase isoliert, die anstatt des üblichen Molybdopterincofaktors eine Häm c-Gruppe [1] und ein Vanadiumatom enthält. Synthese O Die N-(2-Mercaptoacetophenonen)-hydrazide bilden eine neue Klasse dreizähniger ONS-chelatisierender Liganden und sind in guten Ausbeuten aus einer Hydrazidkomponente und Bildung der Schiffschen Base mit o-Mercaptoacetophenon in Methanol bzw. Ethanol zugänglich. Der Umsatz von H2tsalhyph mit Vanadylacetylacetonat führt zum Vanadium(IV)komplex [V(tsalhyph)2]. + H2N N H SH SH SH O MeLi OH (THF) N N H O O H2tsalhyph VO(acac)2 Struktur Eine strukturelle Besonderheit ist, dass in dieser Vanadium(IV)verbindung, anders als erwartet, zwei der doppelt deprotonierten Ligandmoleküle koordinieren und keine Oxo-Gruppe mehr zu finden ist. Die Koordinationsumgebung des Vanadiumatoms lässt sich als trigonal-prismatisch beschreiben, wie sie bereits für sechsfach koordinierte reaktive Zwischenstufen und Übergangszustände anderer [2] Modellkomplexe theoretisch berechnet wurde. Im Gegensatz zur erwarteten planaren Struktur des Liganden wird in der Kristallstruktur eine Torsion des schwefelsubstituierten Aromatfragments um die Bindung zum Iminkohlenstoffatom C16-C17 bzw. C26-C27 um einen Winkel von 35,5° bzw. 29,2° gegenüber der Ebene des Hydrazidrests deutlich. [V(tsalhyph)2 Katalytische Aktivität Erstmals konnte ausgehend von einer Vanadium(IV)verbindung Oxotransferaseaktivität am Beispiel der Reduktion von DMSO zu Dimethylsulfid mit Triphenylphosphan als Sauerstoffakzeptor nachgewiesen werden. PPh3 + O=SMe2 O=PPh3 + SMe2 Der Komplex [V(tsalhyph)2)] wird dafür in sauerstofffreiem, getrocknetem DMSO-d6 gelöst und mit der 10fachen 31 molaren Menge an PPh3 versetzt. Der Reaktionsverlauf wird mit Hilfe der P-NMR-Spektroskopie verfolgt. Bei einer Reaktionstemperatur von 100°C reagieren nach 10,5 Stunden ca. 82 % des eingesetzten PPh3 zu OPPh3 (Abb. 1). PPh3 OPPh3 Von [V(tsalhyph)2] wurde weiterhin ein zeitabhängiges UV/Vis-Spektrum in DMSO bei 100°C aufgenommen (Abb. -1 -1 3 2) und die Extinktionskoeffizienten bei den Absorptionsmaxima bestimmt: e (lmax= 266 nm) = 25,8·10 l·mol ·cm ; 3 -1 -1 e (lmax= 359 nm) = 17,6·10 l·mol ·cm Ein Versuch, die Katalyse UV/Vis-spektroskopisch zu verfolgen, ist in Abb. 3 dargestellt. PPh3 [V(tsalhyph)2] Abb. 2: Zeitabhängiges UV/Vis-Spektrum (60min-Zyklen) von [V(tsalhyph)2] in DMSO bei 100°C Abb. 3: Zeitabhängiges UV/Vis-Spektrum (60min-Zyklen) von [V(tsalhyph)2] mit dem Substrat PPh3 in DMSO bei 100°C [1] A. N. Antipov, D. J. Sorokin, N. P. L Vov, J. G. Kuenen, Biochem. J. 369, 185-189, 2003. [2] M. Kaupp, Angew. Chem. 116, 554-558, 2004. Abb. 1: 31P-NMR (81MHz) von [V(tsalhyph)2] mit PPh3 in DMSO-d6 bei 100°C; oben: nach 3,5 h Reaktionszeit; unten: nach 10,5 h Reaktionszeit

![[Mo(CO)6], [Ru(CO)5] und [RhCl(CO)(PPh3)2]](http://s1.studylibde.com/store/data/005606366_1-015cff068bd8932129b59ee7ad5cb2c5-300x300.png)