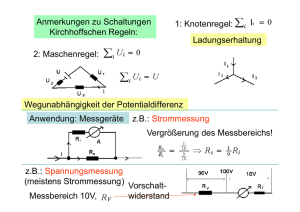
Fachinfo von Ferinject
Werbung

Fachinformation Ferinject 50 mg Eisen/ml 1. BEZEICHNUNG DES ARZNEIMITTELS Verdünnungsschema für Ferinject bei intravenöser Tropfinfusion Ferinject Ferinject 50 mg Eisen/ml, Injektions- und Infusionslösung. 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Ein ml Lösung enthält 50 mg elementares, dreiwertiges Eisen als Eisencarboxymaltose. Jede 2-ml-Durchstechflasche enthält 100 mg elementares, dreiwertiges Eisen als Eisencarboxymaltose. Jede 10-ml-Durchstechflasche enthält 500 mg elementares, dreiwertiges Eisen als Eisencarboxymaltose. Ein ml Lösung enthält bis zu 5,5 mg (0,24 mmol) Natrium, siehe Abschnitt 4.4. Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1. 3. DARREICHUNGSFORM Injektions- und Infusionslösung. Dunkelbraune, nicht durchsichtige, wässrige Lösung. 4 ml 100 bis 200 mg ≥4 bis 10 ml ≥ 200 bis 500 mg 100 ml 6 Minuten ≥ 10 bis 20 ml ≥ 500 bis 1.000 mg 250 ml 15 Minuten Verträgliche maximale Einzeldosis Eine Einzeldosis Ferinject sollte 1.000 mg Eisen (20 ml) pro Tag bzw. 15 mg Eisen (0,3 ml) pro kg Körpergewicht nicht überschreiten. Die maximale wöchentliche Gesamtdosis beträgt 1.000 mg (20 ml). Intravenöse Injektion: Ferinject kann unter Verwendung der unverdünnten Lösung in einer Dosis von bis zu 1.000 mg Eisen durch intravenöse Injektion verabreicht werden. Bei Dosen über 200 und bis zu 500 mg Eisen sollte Ferinject mit einer Geschwindigkeit von 100 mg/min verabreicht werden. Bei Dosen über 500 und bis zu 1.000 mg Eisen sollte Ferinject über 15 Minuten verabreicht werden. Intravenöse Tropfinfusion: 4.1 Anwendungsgebiete Ferinject kann als intravenöse Infusion bis zu einer Einzeldosis von maximal 1.000 mg Eisen (20 ml) verabreicht werden. 4.2 Dosierung, Art und Dauer der Anwendung Ermittlung der kumulativen Eisendosis Die kumulative Dosis zur Wiederauffüllung der Eisenspeicher mit Hilfe von Ferinject wird anhand des Körpergewichts und Hämoglobinspiegels des Patienten ermittelt und darf nicht überschritten werden. Zur Bestimmung der kumulativen Eisendosis sollte folgende Tabelle herangezogen werden: Hb (g/dl) Patienten mit Patienten mit einem Körper- einem Körpergewicht von gewicht ≥ 70 kg 35 kg bis <70 kg <10 1.500 mg 2.000 mg ≥ 10 1.000 mg 1.500 mg Hinweis: Eine kumulative Eisendosis von 500 mg sollte bei Patienten mit einem Körpergewicht von <35 kg nicht überschritten werden. Bei übergewichtigen Patienten sollte für die Ermittlung des Eisenbedarfs ein normales Verhältnis zwischen Körpergewicht und Blutvolumen zugrunde gelegt werden. Bei Patienten mit einem Hb-Wert ≥ 14 g/dl sollte eine Initialdosis von 500 mg Eisen gegeben werden, und die Eisenparameter sollten vor erneuter Gabe überprüft werden. Nach Wiederauffüllung der Eisenspeicher sollte anhand regelmäßiger Kontrollen sichergestellt werden, dass die Eisenspiegel korrigiert und aufrechterhalten werden. 010495-D901 – FERINJECT – n Höchstmenge Mindestdauer der sterile 0,9%ige Verabreichung (m/V) Kochsalzlösung bis 4. KLINISCHE ANGABEN Ferinject ist indiziert zur Behandlung von Eisenmangelzuständen, wenn orale Eisenpräparate unwirksam sind oder nicht angewendet werden können. Die Diagnose muss durch geeignete Laboruntersuchungen bestätigt sein. September 2011 2 Eisen Hinweise zur Anwendung Ferinject darf nur intravenös entweder unverdünnt als Bolusinjektion oder während einer Hämodialysesitzung unverdünnt direkt in den venösen Teil des Dialysegeräts oder als Tropfinfusion verabreicht werden. Für eine Tropfinfusion darf Ferinject nur mit steriler 0,9%iger (m/V) Kochsalzlösung wie folgt verdünnt werden: Siehe Tabelle Hinweis: Aus Stabilitätsgründen sind Verdünnungen auf Konzentrationen unter 2 mg Eisen/ml nicht zulässig. Ferinject darf nicht subkutan oder intramuskulär verabreicht werden. Hämodialysepflichtige chronische Nierenkrankheit Bei Patienten mit hämodialysepflichtiger chronischer Nierenkrankheit darf eine einmal täglich injizierte Höchstdosis von 200 mg Eisen nicht überschritten werden (siehe auch Abschnitt 4.4). Kinder und Jugendliche Die Anwendung von Ferinject wurde bei Kindern nicht untersucht und wird daher bei Kindern unter 14 Jahren nicht empfohlen. 4.3 Gegenanzeigen Die Anwendung von Ferinject ist kontraindiziert bei: • bekannter Überempfindlichkeit gegen Ferinject oder einen der sonstigen Bestandteile • nicht durch Eisenmangel bedingter Anämie, z. B. bei sonstigen Formen der mikrozytären Anämie • Anhaltspunkten für eine Eisenüberladung oder Eisenverwertungsstörungen • erstes Schwangerschaftstrimester 50 ml – 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung Parenteral verabreichte Eisenpräparate können Überempfindlichkeitsreaktionen einschließlich anaphylaktoider Reaktionen mit möglicher Todesfolge verursachen (siehe Abschnitt 4.8). Deshalb müssen Vorrichtungen für eine kardiopulmonale Reanimation verfügbar sein. Wenn während der Verabreichung allergische Reaktionen oder Anzeichen einer Unverträglichkeit auftreten, muss die Behandlung sofort beendet werden. Patienten mit Leberfunktionsstörungen darf parenterales Eisen nur nach sorgfältiger Abwägung von Nutzen und Risiken verabreicht werden. Die Verabreichung von parenteralem Eisen bei Patienten mit Leberfunktionsstörungen, bei denen Eisenüberladung ein auslösender Faktor ist, und speziell bei Porphyria cutanea tarda (PCT), sollte vermieden werden. Zur Verhinderung einer Eisenüberladung wird eine sorgfältige Überwachung des Eisenstatus empfohlen. Für hämodialysepflichtige Patienten mit chronischer Nierenkrankheit liegen keine Informationen zur Sicherheit von Einzeldosen von über 200 mg vor. Bei akuten oder chronischen Infektionen, Asthma, Ekzem oder atopischen Allergien darf parenterales Eisen nur mit Vorsicht angewendet werden. Es wird empfohlen, die Verabreichung von Ferinject bei fortbestehender Bakteriämie abzubrechen. Bei Patienten mit chronischen Infektionen müssen Nutzen und Risiken der Anwendung unter Berücksichtigung der Suppression der Erythropoese sorgfältig abgewogen werden. Bei der Verabreichung von Ferinject ist Vorsicht geboten, um eine paravenöse Injektion zu vermeiden. Bei paravenöser Injektion von Ferinject kann es an der Injektionsstelle zu einer Braunfärbung und Irritation der Haut kommen. In einem solchen Fall muss die Verabreichung von Ferinject sofort beendet werden. Ein ml unverdünntes Ferinject enthält bis zu 0,24 mmol (5,5 mg) Natrium. Dies ist zu berücksichtigen bei Personen unter Natrium kontrollierter (natriumarmer/kochsalzarmer) Diät. Ein ml unverdünntes Ferinject enthält maximal 75 μg Aluminium. Dies ist bei der Behandlung von Dialyse-Patienten zu berücksichtigen. Die Anwendung von Ferinject bei Kindern wurde bisher nicht untersucht. Eine Dosis von 20 ml (1.000 mg Eisen) als Injektion oder Infusion darf nicht häufiger als einmal wöchentlich verabreicht werden. 1 Fachinformation Ferinject 50 mg Eisen/ml 4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen Wie bei allen parenteralen Eisenpräparaten ist die Resorption von oralen Eisenpräparaten vermindert, wenn diese gleichzeitig verabreicht werden. 4.8 Nebenwirkungen Die am häufigsten berichteten Nebenwirkungen sind Kopfschmerzen, die bei 3,3 % der Patienten auftraten. Siehe Tabelle 4.9 Überdosierung Die Verabreichung von Ferinject in Dosen, welche die zur Korrektur des Eisenmangels zum Zeitpunkt der Verabreichung benötigte Menge übersteigen, kann zur Kumulation von Eisen in den Eisenspeichern und damit schließlich zu Hämosiderose führen. Die Überwachung von Eisenparametern wie Serumferritin und Transferrinsättigung kann beim Erkennen einer Eisenanreicherung helfen. Wenn es zur Eisenkumulation gekommen ist, kann die Anwendung eines Eisenkomplexbildners in Erwägung gezogen werden. Gegebenenfalls sollte daher vor Beginn einer oralen Eisentherapie ein Mindestabstand von 5 Tagen nach der letzten Gabe von Ferinject eingehalten werden. 4.6 Schwangerschaft und Stillzeit Klinische Daten für Schwangere stehen nicht zur Verfügung. Vor einer Anwendung in der Schwangerschaft müssen Nutzen und Risiken der Behandlung sorgfältig abgewogen werden. Tierexperimentelle Studien lassen darauf schließen, dass das aus Ferinject freigesetzte Eisen die Plazentaschranke überschreiten kann und die Anwendung dieses Arzneimittels während der Schwangerschaft Auswirkungen auf die Skelettentwicklung des Feten haben kann. 5. PHARMAKOLOGISCHE EIGENSCHAFTEN 5.1 Pharmakodynamische Eigenschaften Klinische Studien haben nur einen vernachlässigbar geringen (≤ 1%) Übertritt von Eisen von Ferinject in die Muttermilch ergeben. Die begrenzten Daten über stillende Mütter deuten darauf hin, dass ein Risiko durch Ferinject für das gestillte Kind unwahrscheinlich ist. 4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen Es ist unwahrscheinlich, dass Ferinject einen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen hat. Systemorganklasse Erkrankungen des Immunsystems Erkrankungen des Nervensystems Gefäßerkrankungen Erkrankungen der Atemwege, des Brustraums und Mediastinums Erkrankungen des Gastrointestinaltrakts Erkrankungen der Haut und des Unterhautzellgewebes Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Untersuchungen Sehr häufig (≥ 1/10) Pharmakotherapeutische Gruppe: Dreiwertiges Eisen, Parenteralia. ATC-Code: B03A C01 In der Ferinject Injektions- und Infusionslösung liegt Eisen als stabiles dreiwertiges Eisen in Form eines Komplexes mit einem polynukleären Eisenhydroxid-Kern und einem Kohlenhydrat-Liganden vor. Der Komplex ist so beschaffen, dass den Eisentransport- und -speicherproteinen im Körper (Transferrin bzw. Ferritin) verwertbares Eisen in steuerbarer Form zur Verfügung gestellt wird. Klinische Studien haben gezeigt, dass das hämatologische Ansprechen und das Auffüllen der Eisenspeicher nach intravenöser Verabreichung von Ferinject rascher Häufig (≥ 1/100, <1/10) erfolgen als nach oraler Verabreichung von Vergleichspräparaten. Mithilfe der Positronenemissionstomographie (PET) wurde nachgewiesen, dass die Verwertung von 59Fe und 52Fe aus radioaktiv markiertem Ferinject durch die Erythrozyten zwischen 61 % und 99 % betrug. Nach 24 Tagen zeigte sich, dass radioaktiv markiertes Eisen von Patienten mit Eisenmangel zu 91 % bis 99 % und von Patienten mit renaler Anämie zu 61 % bis 84 % verwertet wurde. 5.2 Pharmakokinetische Eigenschaften Mithilfe der Positronenemissionstomographie (PET) wurde nachgewiesen, dass 59 Fe und 52Fe aus Ferinject rasch aus dem Blut eliminiert, in das Knochenmark transportiert und in Leber und Milz gespeichert wurden. Nach Verabreichung einer Einzeldosis Ferinject von 100 bis 1.000 mg Eisen werden bei Patienten mit Eisenmangel maximale Gesamteisenspiegel im Serum von 37 μg/ ml bis zu 333 μg/ml nach 15 Minuten bzw. 1,21 Stunden erreicht. Das Volumen des zentralen Kompartiments entspricht im Wesentlichen dem Plasmavolumen (ungefähr 3 Liter). Das injizierte oder infundierte Eisen wurde rasch aus dem Plasma eliminiert. Die terminale Halbwertszeit reichte von 7 bis 12 Stunden und die mittlere Verweildauer von 11 bis 18 Stunden. Die renale Elimination des Eisens war vernachlässigbar gering. 5.3 Präklinische Daten zur Sicherheit Basierend auf den konventionellen Studien zur Sicherheitspharmakologie, Toxizität bei wiederholter Gabe und Genotoxizität lassen die präklinischen Daten keine besonderen Gefahren für den Menschen erkennen. Tierexperimentelle Untersuchungen deuten da- Gelegentlich (≥ 1/1.000, <1/100) Selten (≥ 1/10.000, <1/1.000) Überempfindlichkeit einschließlich anaphylaktoider Reaktionen Kopfschmerzen, Schwindel Parästhesie Hypotonie, Hypertonie, Flush Dyspnoe Übelkeit, Bauchschmerzen, Obstipation, Diarrhoe Dysgeusie, Erbrechen, Dyspepsie, Flatulenz Hautausschlag Pruritus, Urtikaria Myalgie, Rückenschmerzen, Arthralgie Reaktionen an der Injektionsstelle Fieber, Müdigkeit, Schmerzen im Brustkorb, Schüttelfrost, Unwohlsein, peripheres Ödem Vorübergehender Abfall der Serum- Anstieg der Aspartataminotransfephosphatspiegel, Anstieg der Ala- rase, Anstieg der Gamma-Glutnin-Aminotransferase amyltransferase, Anstieg der Lactatdehydrogenase im Blut Es gibt keine Nebenwirkungen mit unbekannter Häufigkeit. 2 010495-D901 – FERINJECT – n Fachinformation Ferinject 50 mg Eisen/ml rauf hin, dass das aus Ferinject freigesetzte Eisen die Plazentaschranke überschreitet und in die Muttermilch ausgeschieden wird. In Studien zur Fortpflanzungstoxizität an Tieren war FERINJECT mit geringfügigen Skelettanomalien beim Feten assoziiert. Zur Beurteilung des karzinogenen Potentials von Ferinject wurden keine Langzeitstudien an Tieren durchgeführt. Es gibt keine Anhaltspunkte für ein allergenes oder immunotoxisches Potenzial. Ein kontrollierter in-vivo Test zeigte keine Kreuzreaktivität von Ferinject mit Anti-Dextran-Antikörpern. Nach intravenöser Verabreichung wurden keine lokalen Reizerscheinungen oder Unverträglichkeiten beobachtet. 6. PHARMAZEUTISCHE ANGABEN 6.1 Liste der sonstigen Bestandteile Natriumhydroxid (zur Einstellung des pHWerts) Salzsäure (zur Einstellung des pH-Werts) Wasser für Injektionszwecke 6.2 Inkompatibilitäten Das Arzneimittel darf, außer mit den unter Abschnitt 6.6 aufgeführten, nicht mit anderen Arzneimitteln gemischt werden. Die Kompatibilität mit Behältnissen aus anderen Materialien als Polyethylen und Glas ist nicht bekannt. 6.3 Dauer der Haltbarkeit Haltbarkeit des Arzneimittels im unversehrten Behältnis: 3 Jahre. Haltbarkeit nach Anbruch der Durchstechflaschen: Vom mikrobiologischen Standpunkt aus sollen Präparate für die parenterale Verabreichung sofort verwendet werden. Haltbarkeit nach Verdünnung mit steriler 0,9%iger (m/V) Natriumchloridlösung: Jede Durchstechflasche Ferinject ist nur für den einmaligen Gebrauch vorgesehen. Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu entsorgen. Ferinject darf nur mit steriler 0,9%iger (m/V) Natriumchloridlösung gemischt werden. Andere intravenöse Verdünnungslösungen und Arzneimittel dürfen nicht verwendet werden, weil eine Gefahr für Sedimentbildung und/oder Wechselwirkungen besteht. Hinweise für die Verdünnung siehe Abschnitt 4.2. 7. INHABER DER ZULASSUNG Vifor France SA 7 – 13, Boulevard Paul-Emile Victor 92200 Neuilly-sur-Seine Frankreich Mitvertreiber Vifor Pharma Deutschland GmbH Baierbrunner Straße 29 D-81379 München Tel. 089 324918 600 Fax 089 324918 601 e-mail: [email protected] 8. ZULASSUNGSNUMMER 66227.00.00 9. DATUM DER ERTEILUNG DER ZULASSUNG/VERLÄNGERUNG DER ZULASSUNG 20. August 2007 10. STAND DER INFORMATION September 2011 11. VERKAUFSABGRENZUNG Verschreibungspflichtig Vom mikrobiologischen Standpunkt aus sollen Präparate für die parenterale Verabreichung nach Verdünnung mit steriler 0,9%iger (m/V) Natriumchloridlösung sofort verwendet werden. 6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung In der Originalverpackung aufbewahren. Nicht über 30 °C lagern. Nicht einfrieren. 6.5 Art und Inhalt des Behältnisses 2 ml Lösung in einer Durchstechflasche (Typ-I-Glas) mit Bromobutyl-Gummistopfen und Aluminiumbördelkappe in Packungsgrößen zu 1 und 5 Durchstechflaschen. 10 ml Lösung in einer Durchstechflasche (Typ-I-Glas) mit Bromobutyl-Gummistopfen und Aluminiumbördelkappe in Packungsgrößen zu 1 und 5 Durchstechflaschen. September 2011 Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht. 6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung und sonstige Hinweise zur Handhabung Die Durchstechflaschen sind vor Gebrauch visuell auf Sedimente und Beschädigungen zu prüfen. Nur homogene, sedimentfreie Lösungen sind zu verabreichen. 010495-D901 – FERINJECT – n Zentrale Anforderung an: Rote Liste Service GmbH | FachInfo-Service | Postfach 11 01 71 10831 Berlin 3