Thieme: Endspurt Vorklinik – Physiologie 1
Werbung

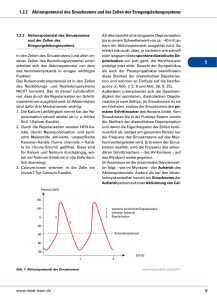
34 3 Herz Corel Stock Lernpaket 2 3 Herz 3.1 Die elektrische Erregung des Herzens Das Herz pumpt sauerstoffarmes Blut in die Lunge und sauerstoffreiches Blut in den Körperkreislauf. Die Pumpwirkung beruht auf einem Wechsel von Kontraktion und Erschlaffung der Herzmuskelzellen. Grundlage für die Kontraktion einer Herzmuskelzelle sind ein elektrischer Impuls und Ionenströme in die Zelle. Dabei steigt die Ca2+-Konzentration in der Muskelzelle an und bewirkt eine Kontraktion. Die Aktionspotenziale sind in den verschiedenen Zellen des Herzens (Schrittmacherzellen, Zellen des Erregungsleitungssystems und Herzmuskelzellen) unterschiedlich; je nach Zelltyp fließen auch unterschiedliche Ionenströme. 3.1.1 Erregungsentstehung und -ausbreitung am Herzen Der Herzmuskel weist elektrophysiologisch gesehen gegenüber der Skelettmuskulatur zwei Besonderheiten auf: ▪▪Schrittmacherzellen, ▪▪Weiterleitung der Erregung von Zelle zu Zelle. Das Herz besitzt einen Eigenrhythmus, d. h., auch wenn man alle zum Herzen führenden Nerven durchtrennt, schlägt es in einem regelmäßigen Rhythmus von ca. 70 Schlägen/min weiter. Dieser Rhythmus entsteht in den Schrittmacherzellen. Schrittmacherzellen sind spezialisierte Herzmuskelzellen, die spontan depolarisieren und so selbst eine Erregung auslösen. Zu den verschiedenen Schrittmacherzellen s.u. Für die Weiterleitung einer Erregung am Herzen ist von großer Bedeutung, dass Herzmuskelzellen über Gap Junctions an den Glanzstreifen miteinander in Verbindung stehen. Die Durchlässigkeit der Gap Junctions wird durch die zytosolische Ca2+- und H+-Konzentration kontrolliert. Nehmen die intrazelluläre H+ - oder die Ca2+-Konzentration zu, nimmt die Durchlässigkeit der Gap Junctions ab. Durch die Verbindung sind letztlich alle Herzzellen elektrisch gekoppelt, d. h., wird eine Zelle erregt, breitet sich diese Erregung auf alle Herzmuskelzellen aus. Man spricht daher von einem funktionellen Synzytium. Die unterschiedliche Dichte der Gap Junctions ist u.a. dafür verantwortlich, dass sich die Erregung regional verschieden schnell über das Myokard ausbreitet. Während die Zellen des Vorhofs und der Kammern jeweils miteinander verbunden sind, sind die Vorhöfe und Kammern durch die bindegewebige Ventilebene voneinander getrennt. Daher kann die Erregung nur am sog. AV-Knoten von den Vorhöfen auf die Kammern übergeleitet werden. ▶▶Ablauf eines normalen Erregungszyklus. Normalerweise be- ginnt ein Erregungszyklus, indem die Schrittmacherzellen des Sinusknotens spontan depolarisieren und sich die Erregung zunächst über das Vorhofmyokard ausbreitet. Die nächste Station ist der Atrioventrikular-(AV-)Knoten. Er ist die einzige leitende Verbindung zwischen Vorhof und Ventrikel. Im AV-Knoten selbst erfolgt die Weiterleitung sehr langsam. Dadurch wird die Kammererregung um ca. 90 ms verzögert, sodass sich die Vorhöfe zeitlich vor den Kammern kontrahieren. Vom AV-Knoten aus sorgt das sog. Erregungsleitungssystem dafür, dass das gesamte Arbeitsmyokard schnell und gleichmäßig erregt wird. Das Erregungsleitungssystem besteht aus spezialisierten, besonders schnell leitenden Muskelfasern, dem sog. His-Bündel, den Kammer-(Tawara-)Schenkeln und den Purkinje-Fasern. Die Leitungsgeschwindigkeit nimmt im Erregungsleitungssystem wieder deutlich zu. ▶▶Hierarchie der Erregungsausbreitung. Die Schrittmacherzel- len des Sinusknotens, die bei einem normalen Erregungszyklus am Herzen eine Frequenz von ca. 70 Schlägen/min erzielen, sind die primären Schrittmacherzellen. Doch nicht nur die Zellen des Sinusknotens haben einen Eigenrhythmus, sondern auch die Zellen des AV-Knotens und des Erregungsleitungssystems (His-Bündel, Tawara-Schenkel, Purkinje-Fasern) können über Spontandepolarisation rhythmische Erregungen auslösen. Diese Schrittmacherzellen nennt man sekundäre bzw. tertiäre Schrittmacherzellen. Ihre Eigenfrequenz ist jedoch geringer als die der Schrittmacherzellen des Sinusknotens. Normalerweise wird ihre Spontanaktivität durch die schnellere Spontanaktivität des Sinusknotens überdeckt, d. h., während die sekundären Schrittmacher noch langsam depolarisieren, erreicht sie schon das aus dem Sinusknoten stammende Aktionspotenzial. Apropos Nur bei einem Ausfall des Sinusknotens macht sich der Eigenrhythmus der nachgeschalteten Schrittmacherzellen bemerkbar. Dann schlägt das Herz mit einer geringeren Frequenz, die vom Ort der Erregungsentstehung abhängt. Die Frequenz des Sinusknotens beträgt normalerweise in Ruhe 60–80 Schläge/min, der AV-Rhythmus beträgt 40–55 Schläge/min, tertiäre (= ventrikuläre) Schrittmacher liegen bei 25–40 Schlägen/min. aus: Endspurt Vorklinik – Physiologie 1 (ISBN 9783131534422) © 2013 Georg Thieme Verlag KG Fazit – Das müssen Sie wissen –– ! Die Zellen des Arbeitsmyokards sind über Gap Junctions miteinander verbunden. –– ! Die Durchlässigkeit der Gap Junctions sinkt, wenn die intra- zellulären H+- und Ca2+-Konzentrationen steigen. –– ! Die Gap Junctions liegen in regional unterschiedlicher Dichte vor, was einer der Gründe für die uneinheitliche Ausbreitungsgeschwindigkeit der Erregung ist. –– ! Die Erregungsleitung ist im AV-Knoten am langsamsten. 3.1.2 Aktionspotenziale im Herzen Den unterschiedlichen Abschnitten des Herzens lassen sich verschiedene Aktionspotenziale zuordnen (Abb. 3.1). Das Aktionspotenzial ist im Sinusknoten und bei Zellen des Vorhofmykards und des AV-Knotens relativ kurz. Im Erregungsleitungssystem hinter dem AV-Knoten ist die Dauer des Aktionspotenzials relativ lang (ähnlich wie im Arbeitsmyokard). Von den Abschnitten des Erregungsleitungs- und -bildungssystems dauert das Aktionspotenzial in den Purkinje-Fasern mit am längsten. Lerntipp Hinter dem AV-Knoten ist die Dauer des Aktionspotenzials in den unterschiedlichen Abschnitten ähnlich lang, in den PurkinjeFasern aber offenbar am längsten. Die Abstufung müssen Sie sich merken. Sie wird häufig nicht genau dargestellt, kann aber prüfungsrelevant sein. ▶▶Aktionspotenzial der Schrittmacherzellen. Schrittmacherzel- len besitzen im Gegensatz zu den meisten anderen Zellen kein stabiles Ruhepotenzial (Abb. 3.2). Nach einer Erregung repolarisieren sie zwar auch, erreichen dabei aber maximal ca. –60 mV (maximales diastolisches Potenzial). Durch einen unselektiven Einstrom von Kationen beginnen sie dann direkt, erneut zu depolarisieren. Wenn diese langsame diastolische Spontandepolarisation das Schwellenpotenzial von ca. –40 mV erreicht, werden spannungsabhängige Ca2+-Kanäle geöffnet. Dieser Anstieg der Ca2+ -Leitfähigkeit führt zu einem Aktionspotenzial. Nach neueren Erkenntnissen erfolgt die langsame diastolische Depolarisation hauptsächlich über unspezifische Kationenkanäle (überwiegend Na+, auch K+), die durch Hyperpolarisation aktiviert werden (HCN-Kanäle, hyperpolarisation-activated cyclic nucleotide-gated channels). Der einwärtsgerichtete Kationenstrom wird auch als If-Strom (f: funny current) oder Ih-Strom (h: hyperpolarisation-activated) bezeichnet. Sinus-Knoten Vorhofmyokard His-Bündel AV-Knoten Tawara-Schenkel Purkinje-Fasern Ventrikelmyokard 100 ms Abb. 3.1 Erregungsbildung und Form der Aktionspotenziale in den verschiedenen Abschnitten des Herzens. Da aufgrund der langsamen Depolarisation keine Na+-Kanäle, sondern Ca2+-Kanäle aktiviert werden und das Ca2+-System langsamer als das Na+-System ist, ist der Aufstrich flacher als bei den Aktionspotenzialen des Arbeitsmyokards (S. 35). Um die Zelle wieder zu repolarisieren, werden K+-Kanäle aktiviert (K+ strömt aus der Zelle). Wenn das maximale diastolische Potenzial erreicht ist, sinkt die K+-Leitfähigkeit wieder ab und Kationen strömen in die Zelle ein. Die Zelle beginnt erneut langsam zu depolarisieren bis sie wieder den Schwellenwert erreicht und das nächste Aktionspotenzial ausgelöst wird. Die Frequenz der Autorhythmie hängt von 4 Faktoren ab: ▪▪Steilheit der diastolischen Spontandepolarisation: Je flacher die diastolische Spontandepolarisation verläuft, desto länger dauert es, bis das Schwellenpotenzial erreicht wird, und desto später wird ein Aktionspotenzial ausgelöst. ▪▪Dauer der Repolarisation: Je länger die Repolarisation dauert, desto später beginnt die nächste diastolische Depolarisation. ▪▪Höhe des Schwellenpotenzials: Je weniger negativ das Schwellenpotenzial ist, desto länger dauert es, bis es erreicht wird und dadurch ein neues Aktionspotenzial ausgelöst wird. ▪▪Höhe des maximalen diastolischen Potenzials: Je niedriger das maximale diastolische Potenzial ist, desto weiter ist der Weg zum Schwellenpotenzial. ▶▶Aktionspotenzial des Arbeitsmyokards. Wie Nervenzellen besitzen auch die Zellen des Arbeitsmyokards in der Diastole ein Ruhepotenzial von ca. –85 mV. Für das Ruhepotenzial der Herzmuskelzelle gelten die allgemeinen Gesetzmäßigkeiten für erregbare Zellen. Je höher die K+-Permeabilität der Zellmembran ist, desto mehr nähert sich das Membranpotenzial dem Gleichgewichtspotenzial der K+-Ionen von ca. –90 mV. Wird die Leitfähigkeit der Membran für K+-Ionen verringert, strömen weniger K+-Ionen in die Zelle und das Ruhepotenzial der Zelle verschiebt sich Richtung Depolarisation. Werden Herzmuskelzellen durch einen Reiz, der normalerweise aus dem Sinusknoten stammt, bis auf das Schwellenpotenzial von –65 mV depolarisiert, entsteht ein Aktionspotenzial. Das Besondere dieses Aktionspotenzials sind seine lange Dauer von ca. 300 ms und seine charakteristische Form, die es in unterschiedliche Phasen unterteilt. Diese Phasen sind: ▪▪eine schnelle Depolarisation mit einem Überschießen des Potenzials zu positiven Werten, ▪▪Plateauphase, ▪▪Repolarisation. Die schnelle Depolarisation beruht auf der vorübergehenden Öffnung spannungsabhängiger Na+-Kanäle, durch die in kurzer Zeit Na+-Ionen in die Zelle einströmen. Die erhöhte Na+Leitfähigkeit führt zu einem steilen Aufstrich (Abb. 3.3). In der Plateauphase werden durch die Depolarisation spannungsgesteuerte L-Typ-Ca2+-Kanäle geöffnet, Ca2+-Ionen strömen aus dem Extrazellulärraum ein und bilden in dieser Phase die hauptsächliche Stromkomponente. Gleichzeitig werden K+-Kanäle geschlossen, sodass die Zelle zunächst depolarisiert bleibt, obwohl das schnelle Na+-System bereits wieder inaktiviert ist. Dieses System bleibt während der Plateauphase inaktiviert (= absolute Refraktärphase, s.u.). Einströmende Ca2+-Ionen aktivieren ryanodinsensitive Ca2+-Kanäle im sarkoplasmatischen Retikulum, dem intrazellulären Ca2+-Speicher, durch die weitere Ca2+-Ionen ins Zytosol strömen und eine Kontraktion auslö- aus: Endspurt Vorklinik – Physiologie 1 (ISBN 9783131534422) © 2013 Georg Thieme Verlag KG 35 L er n pa k e t 2 3.1 Die elektrische Erregung des Herzens 3 Herz Membranpotenzial (mV) Membranpotenzial (mV) 40 0 Kontraktion Schwellenpotenzial 0 200 –400 ms – 40 – 80 ms Leitfähigkeit – 80 Leitfähigkeit Ca2+ Na+ nichtselektive Leitfähigkeit für Kationen Ca2+ 0 IKation ICa2+ Abb. 3.2 Aktionspotenzial und Ionenströme in Schrittmacherzellen. Oben: rote Linie = rasche diastolische Spontandepolarisation (z. B. im Sinusknoten) mit hoher AP-Frequenz, orange Linie = flachere diastolische Spontandepolarisation (z. B. im AV-Knoten) erzeugt eine geringere AP-Frequenz. sen. Es folgt die Repolarisation, in der die Ca2+-Kanäle gehemmt und stattdessen K+ -Kanäle geöffnet werden. Gegen Ende der Repolarisation werden die Ca2+-Ionen durch einen Na+-Ca2+Austauscher (auch Na+-Ca2+-Antiporter genannt) gegen ihren elektrochemischen Gradienten aus der Zelle transportiert oder über Ca2+-ATPasen wieder in das sarkoplasmatische Retikulum gepumpt. Die Kontraktion ist beendet. Substanzen, die die Ca2+-Leitfähigkeit der Myokardzellmembran erhöhen (wie Adrenalin und Noradrenalin), führen zu einer erhöhten Konzentration von Ca2+-Ionen im Zytosol, wodurch die Kontraktionskraft des Herzens gesteigert wird. Lerntipp Schauen Sie sich die Phasen des Aktionspotenzials der Arbeitsmyokardzellen und auch die Leitfähigkeit der Zellmembran für die jeweiligen Ionen gut an. In der Prüfung wird Ihnen möglicherweise der Verlauf des Aktionspotenzials präsentiert und Sie müssen erkennen, welcher Ionenstrom gerade für die jeweilige Phase ausschlaggebend ist. ▶▶Refraktärzeit der Herzmuskelzelle. Während die Herzmus- kelzelle vollständig depolarisiert ist, ist es unmöglich, ein weiteres Aktionspotenzial auszulösen. Diese Phase wird als die absolute Refraktärzeit bezeichnet. Grund für die Unerregbarkeit ist die Inaktivierung des schnellen Na+-Systems, die bis zum Auswärtsstrom IK+ Einwärtsstrom Auswärtsstrom K+ Einwärtsstrom 36 K+ IK+ 0 ICa2+ INa+ Abb. 3.3 Aktionspotenzial in Zellen des Arbeitsmyokards und die zugehörigen Ionenströme. Ende der Plateauphase andauert. Wenn das Na+-System mit zunehmender Repolarisation langsam wieder in den aktivierbaren Zustand übergeht, beginnt die relative Refraktärzeit: Entsprechend starke Reize können ab einem Membranpotenzial von ca. –40 mV zwar wieder Aktionspotenziale auslösen, die Erregungsschwelle ist aber erhöht und die auslösbaren Potenziale sind deutlich kleiner als außerhalb der Refraktärperiode. Die Refraktärzeit endet, wenn das schnelle Na+-System wieder vollständig aktivierbar ist. Das refraktäre Verhalten hat den Sinn, eine vorzeitige Wiedererregung der Zellen zu verhindern und so den für die Pumpfunktion zwingend notwendigen regelmäßigen Wechsel von Erschlaffung und Kontraktion sicherzustellen. ▶▶Dauer eines Aktionspotenzials. Das Aktionspotenzial des Ar- beitsmyokards dauert in Abhängigkeit von der Herzfrequenz und der Lage der Herzmuskelzelle ca. 200–400 ms. Durch die relativ lange Dauer sind die zuerst erregten Myokardteile noch refraktär, wenn die letzten Teile erregt werden. Dadurch wird eine Tetanisierung des Herzmuskels und die Entstehung kreisender Erregungen verhindert. Da die Dauer der Plateauphase in der Regel länger ist als die Dauer der Einzelzuckung, ist der Herzmuskel nicht tetanisierbar. Die Aktionspotenzialdauer passt sich der Herzfrequenz an, ein Schutzmechanismus, der auch bei sehr niedrigen oder sehr hohen Frequenzen wirksam ist. So wird das Aktionspotenzial mit zunehmender Herzfre- aus: Endspurt Vorklinik – Physiologie 1 (ISBN 9783131534422) © 2013 Georg Thieme Verlag KG 3.1 Die elektrische Erregung des Herzens Apropos Bei einem Elektrounfall gehören Störungen der Herzfunktion zu den häufigsten Komplikationen. Besonders gefährlich ist Wechselstrom, weil durch die ständige Umpolung die Gefahr sehr groß ist, dass ein Stromschlag in die sensible Phase (wenn das Herz teils noch erregt, teils schon wieder unerregt ist) trifft. Die Erregungsbildung und -leitung kann dadurch massiv gestört werden. Dies äußert sich in Rhythmusstörungen bis hin zum Kammerflimmern (S. 44) und/oder Herzstillstand. Fazit – Das müssen Sie wissen –– !! Von den Abschnitten des Erregungsleit- und -bildungssys- tems sind die Purkinje-Fasern jene, in denen das Aktionspotenzial mit am längsten dauert. –– !! Die Depolarisation von Schrittmacherzellen wird, nachdem das Schwellenpotenzial überschritten ist, hauptsächlich durch den Einstrom von Ca2+-Ionen erzeugt. Nach neueren Erkenntnissen sind unspezifische Kationenkanäle für den If-Strom (funny current) verantwortlich. –– ! Wenn das maximale diastolische Potenzial erreicht ist, sinkt die K+-Leitfähigkeit wieder ab und die Sinusknotenzelle beginnt erneut zu depolarisieren. –– !! Die schnelle Depolarisation beruht auf der vorübergehenden Öffnung spannungsabhängiger Na+-Kanäle, durch die in kurzer Zeit Na+-Ionen in die Zelle einströmen. Die erhöhte Na+-Leitfähigkeit führt zu einem steilen Aufstrich. –– ! Die Plateauphase wird hauptsächlich vom Strom der ­Ca2+-Ionen durch spannungsabhängige Ca2+-Kanäle getragen. –– ! Gegen Ende der Repolarisation werden die Ca2+-Ionen durch einen Na+-Ca2+-Antiporter gegen ihren elektrochemischen Gradienten aus der Zelle transportiert. –– ! Eine Erhöhung der Ca2+-Leitfähigkeit der Myokardzellmembran führt zu einer erhöhten Konzentration von ­Ca2+-Ionen im Zytosol. 3.1.3 Elektromechanische Kopplung Im Herzen wird eine elektrische Information (Aktionspotenzial) in eine mechanische Aktion (Kontraktion) umgesetzt, man spricht von elektromechanischer Kopplung. ▶▶Kontraktion und Entspannung des Herzmuskels. Das Akti- onspotenzial läuft (ähnlich wie beim Skelettmuskel) über die Zellmembran bis zu den T-Tubuli, Ca2+-Ionen strömen aus dem Extrazellulärraum bzw. den T-Tubuli in die Zelle und induzieren die Ca2+-Freisetzung aus dem sarkoplasmatischen Retikulum. Während des Aktionspotenzials steigt so die intrazelluläre Ca2+-Konzentration von 10 –7 auf 10 –5 mol/l. Die aus dem Extrazellulärraum stammenden Ca2+-Ionen reichen jedoch bei Weitem nicht zur Auslösung einer Kontraktion, sondern sie vermitteln hauptsächlich das Signal für die Freisetzung. Durch Absättigung der Troponin-C-Bindungsstellen heben die Ca2+-Ionen den troponinvermittelten Hemmeffekt des Tropomyosins auf. Die Interaktion von Aktin und Myosin führt schließlich zur Kontraktion. In der Diastole werden die Ca2+-Ionen mithilfe einer Ca2+ATPase wieder in die intrazellulären Speicher und mithilfe eines Na+-Ca2+-Antiporters in den Extrazellulärraum befördert. Bei Letzterem handelt es sich um einen sekundär aktiven Trans- port, dessen treibende Kraft der von der Na+-K+-ATPase erzeugte elektrochemische Na+-Gradient ist. ▶▶Steuerung der Kontraktionskraft (Inotropie). Anders als beim Skelettmuskel betrifft jede Erregung alle Muskelfasern (funktionelles Synzytium, s.o.), eine Erhöhung der Kontraktionskraft kann also nicht über eine Rekrutierung zusätzlicher motorischer Einheiten erfolgen. Gleichzeitig ist der Herzmuskel nicht tetanisierbar, sodass die Kontraktionskraft nur über Beeinflussung nachgeschalteter Prozesse in den Zellen selbst gesteigert werden kann. Eine prinzipielle Möglichkeit, die Herzkraft zu beeinflussen, besteht in der ummittelbaren Erhöhung oder Senkung des transmembranären Ca2+-Einstroms während des Aktionspotenzials. Unabhängig von der Vordehnung des Herzmuskels infolge der diastolischen Ventrikelfüllung (S. 46) hängt die Kontraktionskraft (Inotropie) wesentlich von der Höhe der zytosolischen Ca2+-Konzentration ab. Die positiv inotrope Wirkung des Sympathikus beruht auf der β1-Rezeptor-vermittelten Erhöhung des transmembranären Ca2+-Einstroms aus dem Extrazellulärraum. Auch ein verlängertes Aktionspotenzial (mit entsprechend verlängertem Ca2+-Einstrom) oder eine Hemmung der Na+-K+ATPase (mit konsekutiver Hemmung des ­Na+-Ca2+-Antiporters) führen zu einer Zunahme der Kontraktilität. 3.1.4 Auswirkungen eines gestörten Elektrolyt­ haushalts der K+-Konzentration. Die K+-Leitfähigkeit der hängt v. a. von der K+-Konzentration im Kanal ab, die wiederum aus den K+-Konzentrationen auf beiden Seiten der Membran resultiert. ▪▪Hypokaliämie: Bei K+-Mangel ist die Leitfähigkeit der K+-Kanäle herabgesetzt, die Plateauphase ist dadurch verlängert während gleichzeitig die diastolische Spontandepolarisation in den Schrittmacherzellen beschleunigt wird. Eine (mäßige) Hypokaliämie wirkt daher positiv inotrop (Steigerung der Herzkraft) und positiv chronotrop (Steigerung der Herzfrequenz). Mit weiterer Abnahme der K+-Konzentration nehmen aber die Automatieprozesse zu, was zu Herzrhythmusstörungen (v. a. ektope Erregungsbildung) führen kann. Im EKG zeigt sich eine Senkung der ST-Strecke, eine abgeflachte T-Welle und eine hohe U-Welle. ▪▪Hyperkaliämie: Bei K+-Überschuss ist infolge des geringer ausgeprägten Gradienten zwischen intra- und extrazellulärer K+-Konzentration das Ruhepotenzial weniger negativ (Depolarisation). Die Depolarisation führt zu einer Erhöhung der K+-Leitfähigkeit der Membran. Das Ruhepotenzial wird wieder negativer (Hyperpolarisation), doch die depolarisierende Wirkung wird besonders bei extrazellulären K+-Konzentrationen von über 6 mmol/l nicht vollkommen ausgeglichen. Eine Verschiebung des Ruhepotenzials durch eine Hyperkaliämie in Richtung weniger negativer Werte reduziert Erregbarkeit, Leitungsgeschwindigkeit und Kontraktionskraft des Herzens. Grund hierfür ist eine gewisse Inaktivierung von Na+-Kanälen durch die leichte Depolarisation des Ruhepotenzials, sodass die anfängliche, durch den Einstrom von Na+-Ionen vermittelte Depolarisation beim Aktionspotenzial etwas langsamer abläuft; ebenso verlangsamt ist die Erregungsausbreitung auf die Nachbarzellen. Durch den Anstieg der K+ -Leitfähigkeit der Membran wird ▶▶Einfluss ­K+-Kanäle aus: Endspurt Vorklinik – Physiologie 1 (ISBN 9783131534422) © 2013 Georg Thieme Verlag KG L er n pa k e t 2 quenz insgesamt kürzer. Dies beruht in erster Linie auf der stark erhöhten K+ -Leitfähigkeit der Zellmembran am Ende eines Aktionspotenzials. 37 38 3 Herz außerdem die Repolarisation gefördert und die Dauer des Aktionspotenzials verkürzt . Typische Veränderungen im EKG sind hohe T-Wellen, Abflachung oder Verlust der P-Welle und eine Verbreiterung des QRS-Komplexes, der mit der T-Welle zu einer sinusförmigen Kurve verschmelzen kann. Auch AV-Blockierungen bis zum AV-Block III. Grades können auftreten. Die Auswirkungen einer Hyperkaliämie am Herzen werden durch eine gleichzeitig vorliegende Azidose, Hypokalzämie oder Hyponatriämie noch verstärkt. Apropos In der Herzchirurgie kann man künstlich einen Herzstillstand herbeiführen. Wenn man das Herz mit einer hochkonzentrierten K+-haltigen Lösung perfundiert, kommt es zur Kardioplegie. ▶▶Einfluss der Ca2+-Konzentration. ▪▪Hyperkalzämie: Bei Ca2+-Überschuss ist der Ca2+-Einstrom in die Zelle gesteigert, der schnelle Anstieg der intrazellulären Ca2+-Konzentration bedingt eine Verkürzung der Plateauphase, die zu Rhythmusstörungen führen kann. Im EKG findet man die QT-Zeit auf Kosten der ST-Strecke verkürzt. ▪▪Hypokalzämie: Ca2+-Mangel verlängert das Aktionspotenzial in den Zellen des Arbeitsmyokards und führt so zu einer Verlängerung der Plateauphase mit einem verlängerten QT-Intervall im EKG. Fazit – Das müssen Sie wissen –– ! In der Diastole werden die Ca2+-Ionen mithilfe einer ­Ca2+-ATPase wieder in die intrazellulären Speicher befördert. –– ! Hypokalzämie verlängert das Aktionspotenzial in den Zellen des Arbeitsmyokards und führt so im EKG zu einem verlängerten QT-Intervall. 3.2 Grundlagen der Elektrokardiografie Durch die Depolarisation der Herzmuskelzellen entstehen kleine elektrische Dipole. In der Summe sind diese Potenzialänderungen stark genug, um an der Körperoberfläche registriert werden zu können. Die Erregung des gesamten Herzens führt so zu auf der Hautoberfläche messbaren Potenzialdifferenzen. Das Elektrokardiogramm (EKG) ist eine grafische Aufzeichnung der elektrischen Vorgänge, die Rückschlüsse auf die Erregungsbildung, die Erregungsausbreitung und -rückbildung, den Lagetyp des Herzens und den Rhythmus zulässt. Zum Verständnis der Entstehung der EKG-Kurve dient die Vektortheorie. 3.2.1 Vektortheorie Das Membranpotenzial jeder einzelnen Herzmuskelzelle wird bei Erregung umgepolt. Während der Depolarisation wirken die Herzmuskelzellen wie kleine elektrische Dipole und erzeugen je nach Richtung der Erregungsausbreitung einen kleinen elektrischen Vektor. Da das Herz ein funktionelles Synzytium ist, kann es in seiner Gesamtheit als Dipol betrachtet werden. Die Richtung des integralen Summationsvektors (= Integralvektors) des Gesamtherzens kommt durch die Summation der einzelnen Vektoren aller Myokardzellen zustande. Die Stärke des Gesamtvektors ist von der Muskelmasse abhängig und spiegelt daher v. a. die Abläufe im linken Ventrikel wider. Ist eine Zelle (bzw. das gesamte Herz) gleichmäßig erregt (also überall unerregt oder überall erregt), findet man mit ex- P QRS T R Abb. 3.4 Vektorkardiogramm. Messanordnung zur Darstellung der Vektorschleifen während eines Herzzyklus. Eingezeichnet ist die Lage des Vektors zum Zeitpunkt der R-Zacke im EKG. trazellulären Elektroden keine Potenzialdifferenz. Ein elektrischer Vektor entsteht nur, wenn sich die Erregung verändert (also ausbreitet oder rückbildet) und die Oberflächenladung an den beiden „Enden“ unterschiedlich ist. ▶▶Richtung und Verlauf des Summationsvektors. Die Richtung des Summationsvektors wird durch die Richtung bestimmt, in die sich die Erregung ausbreitet. Während der Herzerregung ändert der Summationsvektor also sowohl seine Länge (Ausdruck der Potenzialgröße) als auch seine Richtung (Pfeilspitze: +). Stark vereinfacht kann man sagen, dass die Erregung des Herzens „von oben nach unten“ (von der Herzbasis in Richtung Herzspitze) und die Rückbildung in die entgegengesetzte Richtung (von der Herzspitze in Richtung Herzbasis) verlaufen. Zieht man den Weg der Vektorspitze in den einzelnen Phasen der Herzerregung nach, erhält man eine dreidimensionale Figur, die sog. Vektorschleife. ▶▶Vektorschleifen der verschiedenen Herzabschnitte. Die Vek- torschleife (Abb. 3.4) ist dreiteilig. Die Erregung der Vorhöfe erzeugt die Vorhofschleife (= P-Welle im EKG). Nach der Vorhoferregung werden die Kammern erregt (Ventrikelschleife). Da sie eine wesentlich größere Muskelmasse besitzen, ist auch die Vektorschleife deutlich größer (= QRS-Komplex im EKG). Die Erregungsrückbildung in den Ventrikeln (= T-Welle im EKG) verläuft entgegengesetzt zur Depolarisation (Repolarisationsschleife). Während der Repolarisation sind also kurzzeitig (ähnlich wie bei der Depolarisation) die herzbasisnahen Teile (noch) erregt und die herzspitzennahen Teile (schon wieder) unerregt, deshalb zeigt die T-Welle ebenfalls einen positiven Ausschlag. 3.2.2 EKG-Kurve Lerntipp Schauen Sie sich genau an, welche Phase des Herzzyklus die einzelnen Abschnitte eines EKG beschreiben. In der Prüfung werden Sie möglicherweise mit Abweichungen vom normalen Verlauf konfrontiert, die Sie richtig interpretieren müssen. Das Bild eines normalen Herzzyklus im EKG besteht aus P-, Q-, R-, S-, T- (und evtl. U-) Wellen oder -Zacken, die sich den einzelnen Phasen des Herzzyklus zuordnen lassen (Abb. 3.5). Wie die Erregungen zustande kommen, zeigt Abb. 3.6. Das EKG bildet nur die Phasen der Vorhof- und Ventrikelerregung ab; das Erregungsleitungssystem des Ventrikels hat eine so geringe Muskelmasse, dass sich seine elektrische Erregung mit den Standard­ ableitungen des EKG nicht erfassen lässt. Bei intrazellulärer Ableitung sind beim Aktionspotenzial des Herzmuskels Potenzialdifferenzen von rund 100 mV messbar. aus: Endspurt Vorklinik – Physiologie 1 (ISBN 9783131534422) © 2013 Georg Thieme Verlag KG P-Welle (< 0,1 Sek. < 0,25 mV) QRSKomplex T-Welle U-Welle QRS-Dauer (0,06 – 0,1 Sek.) QT-Intervall PQ-Intervall (0,12 – 0,2 Sek.) R PQStrecke Q STStrecke S Abb. 3.5 Normales EKG. Sinusknoten erregt AV-Knoten unerregt P + (mV) 0 – PQ EKG (Ableitung II) QRS QRS QRS achse. Sie stimmt weitgehend mit der anatomischen Herzachse überein und kann daher Auskunft über den Lagetyp des Herzens (S. 41) geben. Als Letztes werden die subepikardialen Anteile an der Basis des linken Ventrikels depolarisiert (S-Zacke). Während der Depolarisation der Ventrikel erfolgt die Repolarisation der Vorhöfe. Diese Repolarisation ist im EKG aber nicht zu erkennen, weil die durch die Ventrikeldepolarisation hervorgerufenen zeitgleichen Potenzialänderungen wesentlich stärker sind. Während der ST-Strecke sind die Ventrikel vollständig erregt, sie verläuft daher isoelektrisch. Die T-Welle ist Ausdruck der Erregungsrückbildung in den Ventrikeln. Dabei verläuft die Repolarisation in umgekehrter Reihenfolge wie die Depolarisation, also von außen nach innen und von der Herzspitze in Richtung Herzbasis. Zu Beginn der T-Welle ist bereits der größte Teil des Herzschlagvolumens ausgeworfen. Der Zeitraum vom Beginn der Erregungsausbreitung in den Kammern (Q) bis zum Ende der Rückbildung (T) wird als Q ­ T-Zeit bezeichnet. Sie verkürzt sich bei hoher Herzfrequenz. Das QT-Intervall (Beginn Q bis Ende T) ist von der Herzfrequenz abhängig und dauert ca. 300–400 ms. Die Dauer stimmt nahezu mit der Dauer des Aktionspotenzials im Kammermyokard überein. Ist die Dauer des QT-Intervalls verlängert , weist das auf eine verzögerte Repolarisation (bspw. durch defekte K+-Kanäle) hin. Gelegentlich kann nach der T-Welle noch eine U-Welle beobachtet werden, deren Bedeutung allerdings noch unklar ist. Hohe U-Wellen finden sich bspw. bei Hypokaliämie oder Antiarrhythmikagabe. Fazit – Das müssen Sie wissen –– ! Die Potenzialdifferenzen beim EKG, die auf der Körperober- ST T QRS Abb. 3.6 Vorhof- und Ventrikelerregung und die Entsprechung im EKG. Einzelheiten siehe im Text. Die Potenzialdifferenzen beim EKG, das auf Körperoberfläche gemessen wird, liegen in der Größenordnung von rund 1 mV. Die P-Welle ist Ausdruck der Erregungsausbreitung in den Vorhöfen. Da die Muskelmasse der Vorhöfe nur relativ gering ist, ist auch die P-Welle nur relativ klein. Nachdem die Vorhöfe komplett erregt sind, muss sich die Erregung über den AV-Knoten in die Kammern ausbreiten. Da sich zu diesem Zeitpunkt der Erregungszustand nicht verändert (die Vorhöfe sind vollständig erregt, die Kammern vollständig unerregt), zeigt sich während der PQ-Strecke im EKG eine isoelektrische Linie. Das PQ-Intervall (PQ-Zeit, Beginn P bis Beginn Q) dauert normalerweise < 200 ms. Der QRS-Komplex bildet die Erregungsausbreitung in den Kammern ab. Er dauert normalerweise etwa 80 ms. Zunächst verläuft die Depolarisation der Ventrikel kurz in Richtung der Ventrikelbasis (Q-Zacke). Dann setzt die Depolarisation entlang der Herzachse ein (R-Zacke). Die bei normaler Herzlage erzeugte R-Zacke spiegelt eine Erregungsausbreitung ventrikulär von der Herzbasis zur Herzspitze wider. Die Richtung des größten Summationsvektors entspricht dabei der elektrischen Herz- fläche gemessen werden, liegen in der Größenordnung von rund 1 mV. –– ! Die P-Welle im EKG ist Ausdruck der Erregungsausbreitung in den Vorhöfen. –– ! Die PQ-Strecke spiegelt die atrioventrikuläre Überleitung wider. –– !! Die bei normaler Herzlage erzeugte R-Zacke spiegelt eine Erregungsausbreitung ventrikulär von der Herzbasis zur Herzspitze wider. –– ! Bei hoher Herzfrequenz verkürzt sich die QT-Zeit. –– ! Eine Verlängerung des QT-Intervalls weist auf eine verzögerte Repolarisation hin. 3.2.3 EKG-Extremitätenableitungen Mithilfe der Extremitäten- und Brustwandableitungen lässt sich der zeitliche Verlauf des Summationsvektors, projiziert auf die jeweilige Ableitungsebene, sichtbar machen. Die Messelektroden werden jeweils am rechten und linken Unterarm sowie am linken Unterschenkel angebracht. Am rechten Unterschenkel befindet sich eine Erdungselektrode, um externe Störeinflüsse auszuschalten. Die Extremitätenableitungen registrieren v. a. Ströme in der Frontalebene. Mithilfe dieser Elektroden kann man uni- oder bipolar ableiten. ▶▶Ableitungen nach Goldberger (aVR, aVL, aVF). Diese Ablei- tungen sind unipolar, d. h., man schaltet jeweils 2 Elektroden zu einer indifferenten Elektrode zusammen und misst gegen die aus: Endspurt Vorklinik – Physiologie 1 (ISBN 9783131534422) © 2013 Georg Thieme Verlag KG 39 L er n pa k e t 2 3.2 Grundlagen der Elektrokardiografie