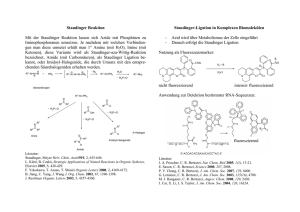
Die Kristallstruktur von p-Tolylbis
Werbung

Z. anorg. allg. Chem. 486, 217 - 224 (1982)
J. A. Barth, Leipzig
Die Kristallstruktur von p-Tolylbis(diethyldithiocarbamato)thallium{ 111) und Phenylbis(methylxanthogenato)bismut( 111)
Von CH. BURSCHKA
Würzburg, Institut für Anorganische Chemie der Universität
Inhaltsübersicht. Die Kristallstruktur von 4.CHs(CeH,)-TI(SaCN(CaHs)2)a (P21 /c, a =
11,973(3) A, b = 10,692(3) A, c = 19,232(4) A, ß = 114,02(2)°, Z = 4) und C8Hs-Bi(SaCOCHs)2
(P21/c, a = 6,395(2) A, b = 24,684(8) A, c = 9,732(3) A, ß = 101,38(3)°, Z = 4) konnte aus Rönt·
gendiffraktometerdaten von Einkristallen ermittelt werden. Die interatomaren Abstände zeigen daß,
die Koordination von Dithiocarbamat und Xanthogenat an die Metallatome wie schon vermutet
stark asymmetrisch zweizähnig und ausschließlich über Schwefel erfolgt. Die Koordinationsunter·
schiede zwischen Bismut und Thallium ergeben ein deutliches Indiz für die "stereochemische Aktivi.
tät" des freien Elektronenpaares am Bismutatom.
erystal Strueture 01 p-Tolylbis(dietbylditbioearbamato)tballium(III) and Phenylbis(metbylxantbogenato) bismut(ID)
Abstract. The crystal structure of 4.CH3(CaH,)-TI(SaCN(C2H5)2)a (P21/c, a = 11.973(3),
b = 10.692(3), c = 19.232(4) A, P = 114.02(2)°, Z = 4) and CeH5-Bi(SaCOCH3)2 (P21 /c, a =
6.395(2), b = 24.684(8), c = 9.732(3) A, ß = 101.38(3)°, Z = 4) was solved from X·ray diffraction
data of single crystals. FlOm the interatomic distances follows that the dithiocarbamate and xantho·
genate ligands coordinate asymmetrically bidentate to the metal as presumed and exclusively through
the sulfur atoms. Differences in the coordination sphere of bismut and thallium give evidence for a
"stereochemically active lone pair" on the bismut atom.
1. Einleitung
Liganden wie Carboxylat, Xanthogenat und Dithiocarbamat sind potentielle
Chelatbildner. Sie treten auch in Verbindung mit schweren Hauptgruppenele"menten als solche auf, jedoch ist die Tendenz zur symmetrisch-zweizähnigen
Bindung vom Zentralatom und offenbar auch von anderen schon vorhandenen
Substituenten daran abhängig. In der Mehrzahl der Fälle kommt es zu stark
asymmetrischer Koordination, obwohl man auch - besonders bei den schweren
IIla·Elementen - Beispiele symmetrischer Bindung findet, die einen weit·
gehenden Ladungsausgleich innerhalb des Chelatringes signalisiert [2-9J.
Die Zentralatome erreichen durch die mehrfache Koordination dieser Gruppe
höhere Koordinationszahlen als es ihrem "normalen" Valenzzustand in kovalenten
218
CH. BURscHKA
Verbindungen entspricht. Bei mehreren derartigen Verbindungen mit solchen
Liganden (COUCOUVANIS [1] gibt eine übersicht über die bis 1977 bekannten
Thiolatkomplexe) wurde zunächst auf Grund spektroskopischer Daten [10-12]
oder wegen ihrer besonderen Stabilität [13] auf eine gewisse Chelatisierung geschlossen. Eine Sicherung dieser Befunde über Röntgenstrukturanalysen ist bei
Organothallium- und -bismutverbindungen bisher jedoch nur in wenigen Fällen
erfolgt.·
In diesem Zusammenhang schien die Kristallstruktur der im Titel genannten
Verbindungen interessant, vor allem auch deshalb, weil sich die Zentralatome
durch ein freies Elektronenpaar bzw. eine Elektronenlücke in der Valenzschale
unterscheiden. über die Synthese und Charakterisierung der Substanzen wurde
bereits berichtet [12, 13].
2. Struktnraufklärung mit Röntgenbeugung
a) Phenylbis(methylxanthogenato)bismut(III). Tab.1 gibt eine
Übersicht über Daten, die bei der Untersuchung eines ausgewählten Einkristalls
der Verbindung erhalten wurden.
Polaroid-Aufnahmen zur Orientierung und eine kleinste-Quadrate-Rechnung mit 20 zentrierten
Reflexen (26° < 26 < 27°) führten zu den angegebenen Zellkonstanten. Auf Grund der regelmäßigen
Auslöschung von Reflexen hOl mit 1= 2n + ] und OkO mit k = 2n + 1 ergab sich die Raumgruppe
P21 /c (Nr. 14). Da 1p-Abtastungen mehrerer Reflexe erhebliche Absorptionseffekte erkennen ließen,
wurden die gemessenen Intensitäten auf der Basis von 11 1p-Kurven korrigiert. Reflexe mit 10 ;;:: 30'(10 )
wurden als beobachtet klassifiziert.
Nachdem die Lageparameter des Bismutatoms einer Pattersonsynthese zu entnehmen waren,
konnten die Positionen der übrigen Atome über Fourier- und Differenzfouriersynthesen festgelegt
Tabelle 1 Daten der Strukturbestimmung
Summenformel
Kristallabmessungen [mm]
Raumgruppe
11
[A]
b
[Al
c
rA]
fJ
Röntgen. Dichte [mg/mm3 ]
Absorptionskoeffizient liMo [mm- I ]
Vermessener Bereich 26
Anzahl gemessener Reflexe
davon symmetrieunabhängig
davon beobachtet (10 ;::;; 30'(10
R-Wert für alle bE'Ob. Reflexe
R-Wert für alle Reflexe
Anzahl der Variablen
»
TlS,N2C17H 27
Kugel 00,4
P21/c (Z = 4)
11,973(3)
10,692(3)
19,232(4)
114,02(2)°
1,75
7,59
5-40°
2391
2101
1869
0,037 (Rw = 0,042)
0,048 (Rw = 0,049)
122
BiS,OzC1oHu
0,15' 0,25 . 0,30
P21/c (Z = 4)
6,395(2)
24,684(8)
9,732(3)r
101,38(3)°
2,21
11,65
5-45°
2310
1969
1811
0,038 (Rw = 0,042)
0,046 (Rw = 0,046)
94
DiffraktometeJ:: Syntex-P211 MoKtX-Strahlung, Graphit-Monochromator, J.. = 0,71069 A, w-Abtastung, Aw = 1°, T = etwa 295 K
p-Tolylbis(diethyldithiocarbamato)thallium(III) u_ Phenylbis(methylxanthogenato)bismut(III)
219
werden. Wasserstoffatome blieben im Modell unberücksichtigt. Als Ergebnis einer Verfeinerung nach
der kleinsten-Quadrate-Methode wurden die in Tab. 2 angegebenen Strukturparameter erhalten. Tab. 4
enthält eine Auswahl der resultierenden interatomaren Abstände und Bindungswinkel. Mit Ausnahme zweier Maxima in Höhe von 1,7 bzw_ 1,3 elAs in enger Nachbarschaft zum Bismutatom, die
wahrscheinlich auf Mängel der Absorptionskorrektur zurückzuführen sind, enthielt eine Karte der
Restelektronendichte nur Konturen< 1,0 e/As.
b) p-Tolylbis(diethyldithiocarbamato )thalli um (lU). Die Strukturaufklärung dieser Verbindung erfolgte ähnlich wie vorstehend beschrieben, mit
dem Unterschied, daß ein kugelförmig geschliffener Einkristall von etwa 0,4 mm
o vermessen wurde, um Absorptionsfehler gering zu halten_
Die in Tab. 1 angegebenen Gitterkonstanten sind das Ergebnis einer auf 14 zentrierten Reflexen
(25° < 20< 28°) basierenden kleinste-Quadrate-Rechnung. Die systematische Auslöschung von
Reflexen führte ebenfalls zu der Raumgruppe P2 1/c. Auch hier wurde das über Patterson-, Fourierund Differenzfouriersynthesen erarbeitete Strukturmodell anschließend nach dem kleinste-QuadrateVerfahren verfeinert. Tab. 3 enthält die berechneten Strukturparameter, und eine Auswahl der resultierenden Abstände und Winkel ist in Tab. 4 aufgeführt. Die abschließend berechnete Restelektronendichte enthielt keine Hinweise auf Unstimmigkeiten und nur Maxima < 0,6 e/A3.
Alle Rechnungen wurden mit Hilfe des Programmsystems Syntex-XTL auf einem Kleincomputer NOVA 1200 erstellt unter Verwendung analytisch approximierter Strukturfaktoren für ungeIadene Atome.
Tabelle 2
Atom
Bi
SIA
S2A
81B
S2B
01A
01B
ClA
C2A
C1B
C2B
Cl
C2
C3
C4
C5
C6
Atomkoordinaten . 10' (für Bi' 10') und Temperaturfaktoren
x
01989(5)
-1012(4)
3476(3)
-3963(4)
-1640(5)
1712(9)
-5766(10)
1542(13)
3704(16)
-3862(15)
-6040(27)
-0~1(12)
1054'(16)
0843(17)
-0701(15)
-1990(17)
-1814(7)
y
z
B
42763(1)
3535(1)
3478(1)
4491(1)
5203(1)
2891(3)
5207(3)
S276(4)
2590(6)
4991(4)
5648(7)
3747(4)
3830(5)
S500(5)
3084(5)
3013(5)
3332(5)
41169(4)
5767(3)
5380(3)
3781(4)
2123(3)
7109(8)
2165(8)
6147(10)
7530(13)
2616(11)
1233(20)
2204(9)
1274(12)
0076(18)
0162(12)
0772(13)
1979(13)
4,8(1)
5,5(2)
S,7(2)
5,8(3)
4,4(2)
8,3(4)
8,2(2)
4,9(2)
5,8(3)
4,6(2)
5,7(3)
5,5(3)
Bu
Atom
Bu
Bu
Bu
Bi
SlA
S2A
SlB
4,42(2)
3,2(9)
3,1(1)
5,0(1)
6,5(1)
3,37(2)
4,9(2)
6,3(2)
3,9(1)
4,!(2)
3,91(2)
4,7(1)
5,5(2)
6,4(2)
4,9(2)
S2B
[A 'J für
-0,29(1)
O,4(9)
-0,4(1)
O,5(1)
-0,8(1)
C.H.Bi(S.COCH.).
Bu
O,66(1)
1,5(9)
1,4(1)
2,0(1)
1,0(1)
Bu
-O,47(2)
0,8(1)
0,7(1)
0,7(1)
0,8(1)
220
Tabelle 3
CH.
BURSOHKA
Atomkoordinaten '10' (filr Tl '10') und Temperaturfaktoren [A'] für 4-CH,C,B.Tl(8.CN(C.B.).).
x
Atom
TI
SlA
S2A
SIB
S2B
NIA
NIB
CIA
C2A
C3A
C4A
C5A
C1B
C2B
C3B
cm
C5B
Cl
02
C3
C4
C5
C6
C7
y
-00683(3)
-1981(2)
-2299(2)
0518(3)
1349(3)
-4148(8)
1869(8)
-2903(9)
-4661(11)
-5008(10)
-5020(9)
-5822(13)
1299(9)
1812(12)
2973(15)
2562(12)
1710(13)
2902(14)
2188(12)
2615(11)
1946(10)
0911(9)
0516(11)
1172(12)
26945(4)
1633(3)
3525(3)
4704(3)
2348(3)
2102(8)
4511(8)
2433(8)
1050(11)
1413(13)
2720(1l)
371\1(12)
38\18(9)
5907(12)
6426(14)
388\1(11)
3648(13)
-0333(13)
041\1(11)
0331(10)
0979(10)
1708(9)
1752(11)
1087(12)
z
B
37910(2)
2936(1)
4502(2)
3717(2)
2498(2)
3647(5)
2508(5)
3704(5)
2999(7)
2347(8)
4289(7)
4137(7)
2876(5)
2837(7)
3341(8)
1792(6)
1083(8)
53110(8)
5019(6)
4321(6)
3958(6)
4341(5)
5038(7)
5362(7)
4,5(2)
5,7(2)
4,3(2)
6,2(3)
6,\1(3)
6,0(3)
7,5(3)
4,3(2)
7,4(3)
9,5(4)
6,4(3)
8,7(4)
8,6(4)
6,0(3)
5,7(3)
5,2(2)
4,4(2)
6,1(3)
7,2(3)
Atom
Bl l
B ..
B ..
TI
SlA·
S2A
SlB
82B
6,04(3)
7,0(2)
5,4(2)
5,0(2)
5,7(2)
3,58(3)
3,4(1)
3,7(1)
4,6(1)
5,4(2)
6,01(3)
4,4(1)
5,1(2)
6,5(2)
5,\1(2)
B ..
BOI
B"
-0,23(2)
0,2(1)
-0,0(1)
0,0(1)
0,5(1)
3,52(2)
1,8(1)
1,7(1)
2,9(1)
3,2(1)
-0,52(2)
-0,0(1)
0,1(1)
0,1(1)
1,0(1)
Tabelle 4 Interatomare AbstAnde [A] und Winkel [0] in der Kristallstruktur von 4-CB.(C,B.)TI(S.CN(C.B,).). und
C,H.BI(S.COCB,),
Zentralatom M
Ligand
Atome
Tl
A
B
M-S1
M-S2
Cl-SI
C1-S2
Cl-N bzw. CI-0
N -C2 bzw. O-G
N-C3
C2-C3
C4-C5
M-C
2,5111(2)
2,728(3)
1,72(1)
1,69(1)
1,38(1)
1,47(2)
1,48(1)
1,53(2)
1,511(2)
2,546(4)
2,795(3)
1,72(1)
1,70(1)
1,35(1)
1,47(1)
1,53(2)
1,54(2)
1,57(2)
Zentralatom
B
2,649(3)
2,961(2)
1,73(1)
1,64(1)
1,32(1)
1,46(1)
2,670(3)
3,079(3)
1,69(1)
1,67(1)
1,32(1)
1,41(2)
2,15(1)
Abweichung von einer "besten Ebene":
S,CNO,
Ebene
Ligand
A
Atome
SI
S2
Cl
N bzw_ 0
C2
C4
Bi
A
2,25(1)
B
S,COO
A
B
-0,001(8)
0,001(3)
-0,005(11)
0,001(9)
-0,01(1)
0,02(1)
0,001(3)
-0,006(4)
0,04(1)
0,04(1)
-0,10(1)
0,03(1)
0,002(3)
0,000(3)
-0,02(1)
-0,019(8)
0,05(1)
-0,001(3)
0,000(2)
0,02(1)
0,007(8)
-0,04(2)
0,006(1)
-0,443(1)
0,000(3)
-0,248(1)
p-Tolylbis(diethyldithiocarbamato)thallium(III) u. Phenylbis(methylxanthogenato)bismut{III) 221
Tabelle 4 (Fortsebung)
Zentralatom M
Literatur
Atome
Tl
SlA-M-S2A
S1B-M-S2B
S1A-M-S1B
S2A-M-S2B
C-M-SIA
C-M-S2A
C-M-SIB
C-M-S2B
67,6(1)
67,6(1)
112,8(1)
144,3(1)
117,8(3)
109,9(3)
128,9
105,2(3)
BI
zum Vergleich:
BI
[15]
BI
[19]
As
[18]
78,1
147,9+)
89,7
87,8+)
98,1
91,3+)
69,1
67,8
84,6
137,8
97,9
89,3
98,5
90,9
.)
63,7(1)
61,8(1)
78,9(1)
155,1(1)
95,5(2)
85,5(2)
93,0(2)
86,5(2)
63,4
62,9
77,9
154,9
91,0
88,4
94,6
82,5
") Mittelwerte
+) Sauerstoff als Ligand
[15]: CH,Bi(S.CN(C,H.),),
[18]: C,H,As(S,CN(C,H,),),
[19J: C,H,Bi(opt),
(opt = 1-oxopyrldln-2-thiolat)
3. Beschreibung der Struktur und Diskussion
Auf Grund von Strukturvergleichen ähnlicher Verbindungen mit Dithioliganden [5-8, 15-18] war zu vermuten, daß auch im vorliegenden Fall Dithiocarbamat und Xanthogenat zweifach an die Zentralatome koordinieren. Zusätzliche Hinweise dafür waren einerseits dem 1.H-NMR-Spektrum der Bismutverbindung entnommen worden [12], andererseits lag auch im Falle der Thalliumverbindung mit deren besonderer Stabilität [13] ein entsprechendes Indiz vor. Die
röntgenographisch ermittelten interatomaren Abstände (vgl. Tab. 4) bestätigen
die Vermutung. Intramolekulare Metall-Schwefel-Bindungen erhöhen die Koordinationszahl für Thallium auf 5 und für Bismut auf 6, sofern man ein freies stereochemisch aktives Elektronenpaar mitberücksichtigt. Zusätzliche intermolekulare
Wechselwirkungen lassen sich im Gegensatz zu den bei CHaBi(S2CN(C2H5)2)2
[15] gefundenen Verhältnissen nicht feststellen, und es bestehen auch keine Anzeichen dafür, daß andere potentielle Koordinationsstellen der Liganden (außer
Schwefel) an der Koordination beteiligt werden, wie es z. B. von (CHa)2TIS2COCHa
[8] mitgeteilt wurde.
Thallium ist gestört trigonal-bipyramidal umgeben, wobei die Atome S1A,
SlB und C5 die Pyramidenbasis ergeben. Sie bilden die kürzesten Bindungen zum
Zentralatom, das mit guter Näherung in der Dreiecksebene liegt (Abweichung
von der Ebene SlA, SlB, C5: 0,095 A), während die Atome S2A und S2B deutlich
weiter entfernt sind und die apikalen Positionen einnehmen. Zwischen letzteren
tritt der mit 144,3(1)° größte S-TI-S-Winkel auf. Die Verzerrung in Richtung
auf eine tetragonal-pyramidale Anordnung kann nicht überraschen, da die
Bißwinkel der Liganden keine Werte um 90° annehmen können. Abb. 1 veranschaulicht die Struktur des Moleküls.
Wie in anderen Dithiocarbamatkomplexen [1], findet man auch in der untersuchten Thalliumverbindung planare S2CNC2-Fragmente mit Abständen Cl-Ni
von 1,35 A bzw. 1,38 A, die für partielle Doppelbindungen sprechen. Eine Komplanarität des Zentralatoms mit der Ligandenebene ist in 1,mterschiedlichem Maß
222
CR. BURSCHKA
gegeben. Während sie bezüglich des Liganden A, der etwas symmetrischer gebunden ist als B, fast exakt ist (wie auch in der Verbindung Tl(S2CN(C2Hö)2)a [6]),
besteht bezüglich B eine Abweichung von 0,44 A. Ahnliche Versetzungen gegenüber der Ligandenebene sind bei Bi(dtcla (dtc = S2CN(C2Hö)2) [16] mit 0,40 A,
0,55 A und 0,68 A, bei Pb(dtc)2 [17] mit 0,32 A und 0,80 A, bei Sb(dtcla [16] mit
0,13 A, 0,70 A und 0,49 A und bei C6HI)As(dtc)2 [18] mit 0,44 A und 0,55 A beobachtet worden. Da entsprechende Strukturdaten fehlen, ist ein Vergleich mit
anderen Monoorganothallium-Verbindungen bisher leider nicht möglich. Offenbar
scheint aber das Vorhandensein gerade einer Thallium-Kohlenstoff-Bindung eine
symmetrische Koordination zu erschweren, wie sie einerseits von Diorganothallium- und -indiumverbindungen [2-5], andererseits aber auch von Komplexen
ohne Metall-C-Bindung [6-9] bekannt ist.
C38
Die Struktur von C6H5-Bi(S2COCHa)2 (vgl. Abb. 2) enthält insgesamt ähnliche,
nur geringfügig längere Metall-Schwefel-Abstände. Während jedoch bei
4-CHaC6 H 4Tl(dtc)2 die Substituenten am Metallatom etwa gleich große Raumwinkel beanspruchen können, ist die U mge bung des Bismutatoms deutlich anders:
p. Tolylbis( diethyldithiocarbarna to )thalliurn(III) u. Phenylbis(methylxanthogenato) bismut(III) 223
Mit einem Winkel von 6,540 stehen die gleichfalls ebenen S2CDC-Fragmente zueinander nahezu koplanar. Diese Anordnun;5 legt die Annahme eines "stereochemisch aktiven" freien Elektronenpaares Iiahe, das die Halbsphäre gegenüber
der Bi-C-Bindung von weiterer nukleophiler Koordination abschirmt. Da diese
Ligandenkonstellation auch von CH3Bi(dtc)2 [15], CsH sAs(dtc)2 [1.8] und CoHsBi(opth (opt = 1-oxopyridin-2-thiolat) [19] her bekannt und die Anordnung
der 5 an das Metall koordinierenden Atome auffallend ähnlich ist (vgl. Tab. 4),
muß man vermuten, daß sie nicht allein durch Packungseffekte zustande kommt.
C4
Abb. 2 Molekülstruktur von CaH 6Bi(S,COCHah
Bemerkenswert erscheint, daß auch in (CoHs)2Bi(S2COC3H7) [14] eine ähnlich
große Koordinationslücke am Zentralatom gegenüber den Bi-C-Bindungen auftritt. Die Komplexe M(dtc)3 (M = Bi, Sb, As) [16] zeigen demgegenüber keine annähernd so große Lücke.
Von den im Kristallverband auftretenden intermolekularen Kontakten bleibt
der hier ermittelte Bi··· Bi-Abstand zu erwähnen, der mit 3,994(1) Aetwas kleiner
ist als der bei Bi(dtc)3 [16] gefundene Wert von 4,135(2) A und ggf. für die Abschätzung des van-der-Waals-Radius von Bismut einen Anhaltspunkt geben kann.
Herrn Prof. Dr. M. WIEBEß danke ich für die Anregung zu diesen Untersuohungen, Herrn Dr.
U. BAUDIS und Frau Dipl.-Chem. A. BASEL für die freundliche überlassung der Kristalle und dem
Rechenzentrum der Universität Würzburg für die Möglichkeit zur Anfertigung der ORTE'P·Plots.
Literatur
[1]
[2]
[3]
[4]
[5]
D. CoUVOUVANIS, Progr. Inorg. Chem. 26, 301-469, 308ff. (1979).
Y. M. CROW U. B. BRrrTON, Acta Crystallogr. B 31,1929 (1975).
W. B. EINSTEIN, M. M.. Gn.BERT U. D. G. TUOK, J. Chern. Soc., Dalton Trans. 1973, 248.
H. D. HAUSEN U. H. U. SORWERlNG, Z. anorg. allg. Chern. 398.119 (1973).
W. SORWARZ, G. MANN U. J. WEmLEIN, J. Organomet. Chern. 122, 303 (1976).
224
[6]
[7]
[8]
[9]
[10]
[11]
[12]
[13]
[14]
[15]
[16]
[17]
[18)
rI9]
CH. BURSCHKA
H. ABRAlIAMSON, J. R. HEIMAN U. L. H. PIGNOLET, lnorg. Chem. U, 2070 (1975).
S. ESPERAS U. S. HUSEBYE, Acta Che~ Scand. A 28, 1015 (1974).
P. J. HAUSER, J. BORDNER U. A. F. SCBBEINER, Inorg. Chem. 12,1347 (1973).
R. FAGGIANl U. 1. D. BROWN, Acta Crystallogr. B S4, 2845 (1978).
H. KUROSOWA U. R. OKAWARA, J. Organomet. Chem. 10, 211 (1967).
R. OKAWARA, J. Organom6t. Chem. 14,225 (1968).
M. WIEBER U. A. BASEL, Z. anorg. allg. Chem. 448, 89 (1979).
U. BAUDIS U. M. WIEBER, Z. anorg. allg. Chem. 448, 79 (1979).
M. WIEBER, H. G. RÜDLING U. CH. BURSomu, Z. anorg. allg. Chem. 470, 171 (1980).
CH. BtmsClIXA u. M. WIEBER, Z. Naturforseh. Mb, 1037 (1979).
C. L. RASTON U. A. H. WmTE, J. Chem. 8oc., Dalton Trans. 1976, 791.
H. IWASAKI U. H.lIAGJHARA, Acta Crystallogr. B 28,507 (1972).
R. BALLY, Acta. Crystallogr. 23, 295 (1967).
J. D. CURRY U. R. J. JANDACEK, J. Chem. 800., Dalton Trans. 1972, 1120.
Bei der Redaktion eingegangen am 4. März 1981.
Anseht. d. Verf.: Dr. CH. BURSCHKA, !nst. f. Anorg. Chemie d. Univ., Am Hubland,
D·8700 Würz burg