- Vetstudy
Werbung

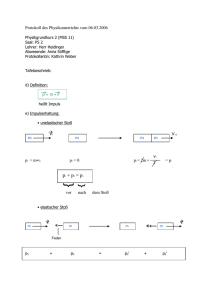
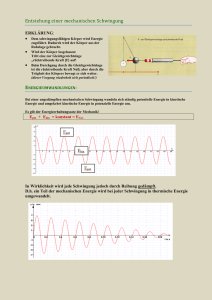
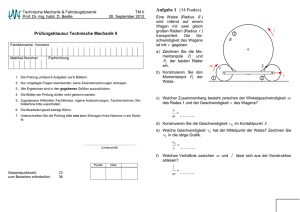
Kinetische Energie: Die an einem freien Körper von einer Kraft geleistete Arbeit ist gleich der Änderung seiner kinetischen Energie Potentielle Energie: Wird ein Körper von der Masse m gegen die Gewichtskraft auf die Höhe h angehoben, dann nimmt seine potentielle Energie zu => diese Kraft wird konservativ genannt Dissipative Kräfte: Arbeitsleistung gegen dissipative (d.h. mechanische Energie verbrauchende) Kräfte führt nicht zur Steigerung der potentiellen Energie des Systems. Es erfolgt Umwandlung in Wärmeenergie, die sich nicht vollständig in mechanische Energie zurückverwandeln lässt Energieerhaltungssatz: In einem abgeschlossenen System bleibt die Summe aus potentieller und kinetischer Energie konstant. Nimmt eine Energieform ab, so muss die andere zwangsläufig um den gleichen Betrag zunehmen 1.Newtonsches Axiom: Ein Körper, auf den keine Kraft wirkt, verharrt in Ruhe oder bewegt sich gleichförmig 2.Newtonsches Axiom: F=m*a 3.Newtonsches Axiom: actio = reactio Zu jeder Kraft gibt es eine Gegenkraft gleichen Betrages und entgegengesetzter Richtung Boyle-Mariottesches Gesetz: P * V = const. (bei T = const.) Elastischer/unelastischer Stoß: Ist die kinetische Energie nach dem Stoß gleich derjenigen vor dem Stoß, dann nennt man den Stoß elastisch. Ändert sie sich auf Grund anderer Energieformen (Deformations- oder Wärmeenergie), dann spricht man vom unelastischen Stoß Ungedämpfte Schwingung: (Bsp. Ball) Der Ball erreicht stets seine Ausgangshöhe wieder => existiert nicht in der Realität - Ungedämpfte harmonische Schwingung: Ort-Zeit-Abhängigkeit kann durch eine Sinuskurve beschrieben werden Gedämpfte Schwingung: Sprunghöhe nimmt stetig ab auf Grund der bei jeder Bewegung auftretenden Reibungsverluste. Mechanische Energie wird stetig in Wärme umgewandelt Erzwungene Schwingung: Man kann eine Bewegung des Balles mit konstanter Sprunghöhe erreichen, indem man dem Ball periodisch den in Wärme umgewandelten Energiebetrag von außen wieder zuführt => kleiner Schlag mit der Hand 1.Hauptsatz der Wärmelehre: Die Zunahme der inneren Energie ΔU eines Systems ist gleich der zugeführten Wärmeenergie Q und der am System verrichteten Arbeit W ΔU = Q + W Isothermer Prozess: Wird dafür gesorgt, dass die Temperatur eines Systems während eines Prozesses konstant bleibt, spricht man von einem isothermen Prozess => Q = -W oder W = -Q, wenn ΔU = 0 Adiabatischer Prozess: Verlaufen ohne Wärmeaustausch mit der Umgebung => Q=0 => ΔU=W