Anti-MERS-CoV-IIFT Kamel (IgG)
Werbung

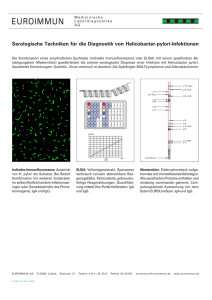
Anti-MERS-CoV-IIFT Kamel (IgG) MERS-CoV positiv Erster kommerziell erhältlicher IIFT zum Nachweis von anti-MERS-CoV Antikörpern bei Kamelen Effiziente Automatisierungslösungen Technische Daten Antigensubstrat Probenverdünnung MERS-Coronavirus-infizierte und nicht-infizierte Zellen (Spezies EU 14) Camelides Serum oder Plasma Qualitative Auswertung: 1:100 Semiquantitative Auswertung: 1:10 / 100 / 1000 etc. Bezüglich des Messbereiches gibt es keine Obergrenze Reagenzien Gebrauchsfertig, mit Ausnahme des PBS-Tween-Puffers Testablauf 30 min (Probe) / 30 min (Konjugat), Raumtemperatur Mikroskopie Objektiv 20 x Lichtquelle: EUROIMMUN-LED oder Quecksilberdampflampe, 100 W Anregungsfilter: 488 nm, Farbteiler: 510 nm, Sperrfilter: 520 nm Stabilität Alle Bestandteile des Testsatzes sind ab dem Tag der Herstellung mindestens 18 Monate haltbar Packungsformat 10 Objektträger, jeder mit 10 Testfeldern, der Testsatz enthält alle notwendigen Reagenzien Bestell-Nr. FI 2604-1010 GK Klinische Bedeutung Das beim Menschen 2012 erstmals aufgetretene „Middle East Respiratory Syndrome“ (MERS) wird durch ein neuartiges Coronavirus (MERS-CoV) verursacht. Alle humanen MERS-CoV-Infektionen haben ihren Ursprung im Nahen Osten mit Schwerpunkt in Saudi-Arabien. Von den bisher aufgetretenen Erkrankungsfällen endeten ca. 40 % tödlich. Die Symptome beim Menschen sind ähnlich denen des „Severe Acute Respiratory Syndrome“ (SARS) mit akuter Lungenentzündung, oft zusätzlichem Nierenversagen mit nachfolgender Sepsis und schließlich Multiorganversagen. Die Inkubationszeit beträgt meist weniger als eine Woche, in Einzelfällen bis zu zwölf Tage. Die Viren werden von Mensch zu Mensch durch Tröpfchen- und Schmierinfektion übertragen. Von besonderer Bedeutung hierbei sind respiratorische Sekrete aus den oberen Atemwegen infizierter Personen, da sie durch Niesen, Husten und damit kontaminierte Hände weitergegeben werden können. Bislang existiert keine erprobte und sichere antivirale Therapie. Die Behandlung der Erkrankten beschränkt sich daher auf die Linderung der Symptome. Auch steht bislang kein wirksamer Impfstoff gegen MERS-CoV zur Verfügung. Bestätigte Wirtsorganismen des MERS-CoV sind neben Fledermäusen Dromedare, die derzeit als potentielle Quelle sporadischer Infektionen beim Menschen diskutiert werden. Antikörper gegen das MERS-CoV sind in Kamelseren gefunden worden, die schon 1983 gewonnen wurden, so dass das Virus bereits seit langer Zeit in der Kamelpopulation zu zirkulieren scheint. Die Antikörperprävalenz beträgt bei adulten Kamelen in endemischen Gebieten bis zu 100 % und unterscheidet sich damit von der bei jungen Kamelen unter 2 Jahren (bis 72 %). Neugeborene Kamele stehen im Verdacht, das Virus zu vermehren und zu übertragen. Die Kamelkälber müssen zunächst neutralisierende Antikörper bilden und stellen bis dahin eine potentielle Infektionsquelle für den Menschen dar. Klinische Symptome sind bei Kamelen jedoch selten und generell mild. Einen zugelassenen Impfstoff gibt es bisher nicht. EUROIMMUN AG · Seekamp 31 · 23560 Lübeck · Telefon: 0451 5855 0 · E-Mail: [email protected] · www.vet.euroimmun.de Stellenwert Zur Bestätigung von Verdachtsfällen einer MERS-CoV-Infektion sind der Direktnachweis von MERS-CoV mittels Polymerasekettenreaktion (PCR) und der Nachweis von Antikörpern gegen MERS-CoV mittels indirekter Immunfluoreszenz (IIFT), ELISA oder Neutralisationstest die sichersten labordiagnostischen Verfahren. IgG-Antikörper treten ungefähr 3 Wochen nach Infektion auf und persistieren über Jahre. Der Anti-MERS-CoV-IIFT Kamel (IgG) basiert auf MERS-CoV-infizierten Zellen und erlaubt eine effiziente Bestimmung von anti-MERS-CoV Antikörpern bei Kamelen. Bei der serologischen Diagnostik sind Kreuzreaktionen mit anderen Coronaviren, insbesondere den bovinen Coronaviren, zu beachten. Positive Ergebnisse sollten mit einer weiteren Methode, im Idealfall einem Neutralisationstest, bestätigt werden. Testprinzip und Testdurchführung Das vorliegende Testsystem dient ausschließlich der In-vitro-Bestimmung von Antikörpern in camelidem Serum oder Plasma. Die Bestimmung kann qualitativ oder semiquantitativ erfolgen. BIOCHIPs, die mit MERS-CoV-infizierten Zellen beschichtet sind, werden mit verdünnten Proben inkubiert. Bei positiven Reaktionen binden sich spezifische Antikörper der Klasse IgG, IgA und IgM an die Virusantigene. Gebundene Antikörper werden in einem zweiten Inkubationsschritt mit Fluorescein-markierten Anti-Kamel-IgG-Antikörpern angefärbt und im Fluoreszenzmikroskop sichtbar gemacht. Inkubation mit der TITERPLANE®-Technik Reagenzträger Mit BIOCHIPs bestückter Objektträger Objektträger mit EUROIMMUN-BIOCHIPs werden mit Hilfe der TITERPLANE®-Technik inkubiert, bei der mehrere Proben gleichzeitig und direkt nebeneinander unter identischen Bedingungen bearbeitet werden. Die Inkubation der Substrate mit den Positiv- und Negativ-Kontrollen (in jedem Testsatz enthalten) zeigt an, ob der Test korrekt durchgeführt wurde, und hilft bei der Auswertung. ;;; ;; ;; ;; ;; ;;; ;; ;; ;; ;; ; ;; ;; ;; ;;; ;; ;; ;; ;; ; ;; ;; ;; ;;; ;; ;; ;; ;; Referenzbereich Titer < 1 : 100. In einem Kontrollkollektiv, bestehend aus Kamelproben aus Deutschland mit negativem Vorhersagewert für MERSCoV (n = 33), wurde eine MERS-CoV-Prävalenz von 0 % ermittelt. Sensitivität und Spezifität 33 serologisch vorcharakterisierte Kamelproben mit negativem Erwartungswert (Herkuft: Deutschland und VAE), sowie 163 Kamelproben mit positivem Erwartungswert (Herkunft: Dubai, Teneriffa, Gran Canaria, VAE) wurden mit dem AntiMERS-CoV-IIFT Kamel (IgG) untersucht. Die Spezifität des Testsystems betrug 100 % bei einer Sensitivität von 99,4 %. Erwartungswerte der Proben n = 196 EUROIMMUN Anti-MERS-CoV-IIFT Kamel (IgG) positiv negativ positiv 162 0 negativ 1 33 Literatur 1. 2. 3. 4. 5. Corman VM, Jores J, Meyer B, Younan M, Liljander A, Said MY, Gluecks I, Lattwein E, Bosch BJ, Drexler JF, Bornstein S, Drosten C, Müller MA. Antibodies against MERS Coronavirus in Dromedary Camels, Kenya, 1992-2013. Emerg Infect Dis 2014; 20(8):1319-22 Meyer B, Müller MA, Corman VM, Reusken CB, Ritz D, Godeke GJ, Lattwein E, Kallies S, Siemens A, van Beek J, Drexler JF, Muth D, Bosch BJ, Wernery U, Koopmans MP, Wernery R, Drosten C. Antibodies against MERS coronavirus in dromedary camels, United Arab Emirates, 2003 and 2013. Emerg Infect Dis. 2014; 20(4):552–9 Müller MA, Corman VM, Jores J, Meyer B, Younan M, Liljander A, Bosch BJ, Lattwein E, Hilali M, Musa BE, Bornstein S, Drosten C. MERS coronavirus neutralizing antibodies in camels, eastern Africa, 1983–1997. Emerg Infect Dis 2014; 20(12):2093-95 Gutiérrez C, Tejedor-Junco Mía T, González M, Lattwein E, Renneker S. Presence of antibodies but no evidence for circu-lation of MERS-CoV in dromedaries on the Canary Islands, 2015. Euro Surveill. 2015; 20(37) Meyer B, Drosten C, Müller MA. Serological assays for emerging coronaviruses: Challenges and pitfalls. Virus research 2014 EUROIMMUN AG · Seekamp 31 · 23560 Lübeck · Telefon: 0451 5855 0 · E-Mail: [email protected] · www.vet.euroimmun.de FI_2604K_D_DE_A01, 12/2015