- KIT
Werbung

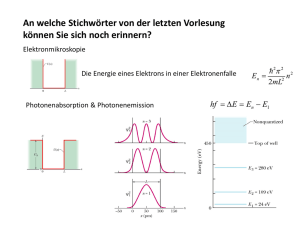
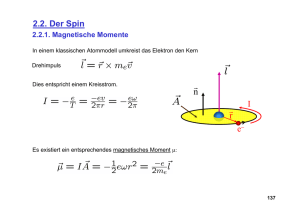
3. Vom Wasserstoffatom zum Periodensystem der Elemente Im vorangegangenen Kapitel haben wir uns mit den grundlegenden Konzepten der Quantenmechanik auseinandergesetzt. Ein weiteres Ziel dieser Vorlesung ist es, mit Hilfe der Theorie aus den Kapiteln 1 und 2 ein Grundverständnis vom Aufbau der Materie und vor allem die den Ingenieur interessierenden Eigenschaften verschiedener Stoffe wie Leitfähigkeit oder optische Eigenschaften zu gewinnen. Die in diesem Kapitel am Beispiel des Wasserstoffatoms gewonnenen Einsichten führen uns zur Systematik des Periodensystems der Elemente (PSE). 3.1. Quantenmechanische Probleme in drei Dimensionen 3.1.1. Schrödingergleichung in drei Dimensionen Die einführenden Kapitel haben sich der Einfachheit halber meistens auf eine Dimension beschränkt. Für relevante physikalische Situationen muss man dagegen oft dreidimensional rechnen. Es ergeben sich dadurch keine prinzipiell neuen Phänomene, die mathematische Beschreibung wird aber deutlich aufwändiger. Die Schrödingergleichung ändert sich von 3.1-1 =2 ∂ 2 ψ ( x ) + V ( x )ψ ( x ) = Wψ ( x ) − 2m ∂x 2 im Eindimensionalen zu − G G ∂2 ∂2 G =2 ∂ 2 + + ψ (r ) + V (r )ψ (r ) = Wψ (r ) 2 2 2 ∂y ∂z 2m ∂x 2 =∇ =∆ 3.1-2 in drei Dimensionen. Normalerweise erschwert die Dreidimensionalität die Lösung der Schrödingergleichung erheblich, in einigen Fällen kann man aber die dreidimensionalen Probleme wieder geschickt aufspalten. Wir betrachten hierzu ein Potential der Form G 3.1-3 V (r ) = f ( x ) + g ( y ) + h( z ) , es besteht also aus einer additiven Überlagerung von drei Komponenten, die nur von einer kartesischen Koordinate abhängen (in der Folge farblich gekennzeichnet). Wenn man nun den Ansatz für die Wellenfunktion G ψ (r ) = u( x )v ( y )w ( z ) 3.1-4 - 56 - in die dreidimensionale Schrödingergleichung 3.1-2 einsetzt, erhält man folgenden Ausdruck: − =2 ∂ 2 ∂2 ∂2 + + + f ( x ) + g ( y ) + h( z ) u( x )v ( y )w ( z ) = W u( x )v ( y )w ( z ) 2 2 2 ∂y ∂z 2m ∂x 3.1-5 Löst man die Klammer auf und teilt durch u( x )v ( y )w ( z ) erhält man C A B 2 2 2 2 2 2 = 1 ∂ u( x ) = 1 ∂ v (y ) 1 ∂ w (z) = − + f (x) − + g(y ) − + h( z ) 2m u( x ) ∂x 2 2m v ( y ) ∂y 2 2m w ( z ) ∂z 2 3.1-6 = W ( = W x + W y + Wz ) . Wir sehen, dass die Terme auf der linken Seite alle nur von einer Variable abhängen, Die rechte Seite ist sogar konstant. Nun verändern wir den x-Wert. Nur die von x abhängigen Terme (A) werden davon beeinflusst. Wenn sich der gesamte Ausdruck (A) aber mit x ändert, müsste diese Änderung von den Termen (B) oder (C) kompensiert werden, damit die rechte Seite der Gleichung konstant bleibt. Da (B) und (C) jedoch gar nicht von x abhängen, ist das unmöglich. Als Folgerung bleibt, dass die einzelnen Teile (A) zwar in sehr komplizierter Weise von x abhängig sein können, in der Summe aber immer konstant sind. Gleiches gilt für die anderen beiden Koordinaten. Damit kann man Gleichung 3.1-6 in drei unabhängige Gleichungen zerlegen: =2 ∂ 2 u( x ) + f ( x )u( x ) = Wx u( x ) 2m ∂x 2 =2 ∂ 2 − v ( y ) + g ( y )v ( y ) = Wy v ( y ) 2m ∂y 2 3.1-7 =2 ∂ 2 w ( z ) + h( z )w ( z ) = Wzw ( z ) 2m ∂z 2 3.1-9 − − 3.1-8 Diese drei Gleichungen beschreiben wieder jeweils ein eindimensionales quantenmechanisches System, können somit mit unserem vorhandenen Handwerkszeug gelöst werden. Die Energieeigenwerte des Gesamtsystems erhält man dann durch Addition der Lösungen der eindimensionalen Probleme ( WGesamt = Wx + Wy + Wz ), die Wellenfunktionen in drei Dimensionen durch Multiplikation der Einzelwellenfunktionen (Gleichung 3.1-4). - 57 - 3.1.2. Beispiel Quantenpunkt Das Vorgehen im letzten Unterabschnitt soll anhand eines Beispiels verdeutlicht werden, das erstens analytisch zu lösen ist und zudem eine zentrale Rolle in der Opto- und Nanoelektronik-Forschung spielt. Als Quantenpunkte bezeichnet man Systeme, die in allen drei Raumdimensionen sehr kleine Ausdehnungen (einige Nanometer) haben. Die reproduzierbare Herstellung von nanometergroßen Quantenpunkten stellt hierbei eine anspruchsvolle technologische Aufgabe dar (Abbildung 3.1-1) (siehe z.B. auf der Homepage des Dortmunder StartupUnternehmens Nanosemiconductor http://www.nanosemiconductor.com/). Abbildung 3.1-1: Elektronenmikroskopische Aufnahme sogenannter Quantenpunkte (Quelle: Infineon). Abbildung 3.1-2: Herstellung von Quantenpunkten (Quelle: J. Reithmaier, Uni Würzburg) Was haben nun diese winzigen Objekte mit unserem Problem zu tun? In erster Näherung kann sich ein Elektron im Quantenpunkt frei bewegen, ihn aber nicht verlassen. Diese Situation entspricht einem Potentialkasten in drei Dimensionen mit unendlich hohen Wänden. In Kapitel 2 erhielten wir die Wellenfunktionen für den Fall des eindimensionalen unendlichen Potentialtopfs: 3.1-10 nxπ x ,mit nx = 1,2,3,.. L ψ nx = An sin Als Energieeigenwerte haben wir Wnx = 3.1-11 =2π 2 2 nx 2mL2 berechnet. Damit erhält man für das dreidimensionale Problem: - 58 - ψn n x π x n y π y nz π z = ( , , ) sin x y z A sin nx ,ny ,nz sin x ,ny ,nz L L L 3.1-12 Und Wnx ,ny ,nz = Wnx + Wny + Wnz 3.1-13 Abbildung 3.1-3 zeigt das Schema der untersten Energieniveaus für einen solch idealisierten Quantenpunkt mit unendlich hohen Wänden. Die Niveaus werden durch die drei Quantenzahlen nx , ny und nz bezeichnet. Man erkennt, dass für viele Energieniveaus mehrere verschiedene Wellenfunktionen existieren. Einen solchen Energieeigenzustand, für den es mehr als eine Realisierungsmöglichkeit gibt, nennt man entartet. W (W0) ( 2 +2 +2 )W 2 2 2 0 12 11 9 6 3 (nx =ny =nz =2) = 12W0 (nicht entartet) ( 3 +1 +1 )W = (1 +3 +1 )W = (1 +1 +3 )W 0 = 11W0 (dreifach entartet) (nx =3;ny =nz =1);(nx =1; ny =3; nz =1);(nx =1; ny =1; nz =3) 2 2 2 2 2 2 0 2 2 2 0 ( 2 +2 +1 )W = ( 2 +1 +2 )W = (1 +2 +2 )W 0 = 9W0 (dreifach entartet) (nx =ny =2;nz =1);(nx =2; ny =1; nz =2);(nx =1; ny =2; nz =2) 2 2 2 2 2 2 0 2 2 2 0 ( 2 +1 +1 )W = (1 +2 +1 ) = (1 +1 +2 ) = 6W 2 2 2 2 2 2 2 2 2 0 (dreifach entartet) (nx =2; ny =nz =1);(nx =1; ny =2; nz =1);(nx =1; ny =1; nz =2) 0 (1 +1 +1 ) W 2 2 2 0 = 3W0 (nx =ny =nz =1) (nicht entartet) 0 Abbildung 3.1-3: Schema der niedrigsten Energieniveaus eines dreidimensionalen Quantenpunkts. Die meisten Zustände sind entartet, das heißt durch mehr als eine Kombination von Quantenzahlen erreichbar. Da jede Kombination von Quantenzahlen eine Eigenfunktion des Problems repräsentiert, ist das gleichbedeutend mit mehreren Eigenfunktionen zu einem Energieeigenwert. 3.1.3. Die Sache mit dem Spin Im Jahr 1922 zeigten Stern und Gerlach mit genialem experimentellen Geschick, dass die bisherige Beschreibung des Elektrons nicht komplett war. Sie ließen Silberatome durch ein inhomogenes Magnetfeld fliegen (siehe Abbildung 3.1-5). Nach dem Durchgang durch dieses spaltete sich der Atomstrahl in zwei Teilstrahlen auf. Erklärbar ist dies durch die im inhomogenen magnetischen Feld auftretenden Kräfte der Form - 59 - G G G 3.1-14 F = − pm ⋅ ∇B , wobei pm das magnetische Dipolmoment bezeichnet. Das magnetische Dipolmoment kann mit dem Drehmoment eines geladenen Teilchens auf einer Kreisbahn oder der Eigendrehung eines ausgedehnten, geladenen Objekts in Verbindung gebracht werden (siehe Abbildung 3.1-4). Auf dem Schirm hinter dem inhomogenen Magnetfeld erkennt man im Stern-Gerlach-Versuch zwei diskrete Linien. Daraus können zwei Schlüsse gezogen werden. Erstens besitzen die Silberatome ein Gesamt-Drehmoment, also ein von Null verschiedenes magnetisches Dipolmoment. Man kann jedoch zeigen, dass es sich bei dem Drehmoment nur um ein Eigendrehmoment des äußersten Elektrons handeln kann. Dieses Eigendrehmoment wird als Spin bezeichnet. Veranschaulichen kann man sich diesen Spin als die Drehung eines kugelförmigen Körpers (z.B. ein Fußball) um seine Achse, wobei man sich der Grenzen dieser Analogie bewusst sein muss (trotz extrem hochauflösender Streuexperimente konnte dem Elektron noch keine Ausdehnung nachgewiesen werden). Die zweite Folgerung bezieht sich auf die diskreten Linien, die im Experiment beobachtet werden. Zunächst könnte man annehmen, dass der Spin des Elektrons gleich verteilt über alle Raumrichtungen auftritt. Dann müsste aber auch die Ablenkung in Richtung des Gradienten des Magnetfelds kontinuierlich Verlaufen (keine Ablenkung für senkrecht auf dem Gradienten stehendes Dipolmoment, maximale für parallele Ausrichtung). Die diskreten Linien zeigen jedoch, dass nur zwei verschiedene Einstellungen des Spins bezüglich der z-Achse möglich sind. Für das Elektron bezeichnet man die beiden Spineinstellungen mit +1/2 und -1/2, das rührt davon her, dass die Komponenten des Spins in Magnetfeldrichtung die Werte 3.1-15 1 sz = ± = 2 annehmen können, also antiparallel zueinander stehen. Quantenmechanisch findet man für alle Drehimpulse, also auch für die Bahndrehimpulse, nur diskrete Werte. Die Bahndrehimpulse können jedoch nur ganzzahlige Vielfache von = annehmen, der Spin auch halbzahlige. - 60 - G ω G L pos. Ladung R neg. Ladung Abbildung 3.1-4: Visualisierung von magnetischen Dipolmomenten – sowohl ein geladenes Teilchen auf einer Kreisbahn als auch eine gleichmäßig geladene, rotierende Kugel erzeugen ein magnetisches Dipolmoment. Das Dipolmoment zeigt in Richtung des Drehimpuls und hängt proportional von diesem ab. Im ersten Fall bezeichnet es Bahndrehimpuls, im zweiten Fall als Eigendrehimpuls oder Spin. Abbildung 3.1-5: Stern-Gerlach-Versuch – ein ausgerichteter Strahl von Silberatomen fliegt durch ein inhomogenes Magnetfeld. Atome mit einem von Null verschiedenen Dipolmoment werden von der geraden Bahn abgelenkt. Das Dipolmoment nimmt allerdings nicht alle möglichen Orientierungen zum Magnetfeld ein, sonst ergäbe sich eine gleichmäßige Verteilung der Atome (classical prediction). Man findet stattdessen zwei getrennte Punkte, die auf zwei antiparallele Orientierungen des Dipolmoments hinweisen. Weitere Überlegungen ergeben, dass das Valenzelektron Träger des Dipolmoments sein muss. Diese Eigenschaft wurde Spin genannt. Die Richtung und Größe des Spins bezeichnet die Spinquantenzahl s , mit ihr ist die Beschreibung des quantenmechanischen Zustands des Elektrons komplett. Da der Spin in der Schrödingergleichung nicht enthalten ist, kann dies berücksichtigt werden, indem man die Wellenfunktion des Elektrons als zweidimensionalen Spaltenvektor, dem so genannten Spinor, darstellt. - 61 - G ψ 1 (r , t ) G ψ (r , t ) → 2 G ψ − 1 (r , t ) 2 3.1-16 Zur vollständigen Beschreibung eines elektronischen Zustands, zum Beispiel in einem Quantenpunkt, brauchen wir also vier Quantenzahlen nx, ny, nz und s. 3.1.4. Pauli-Prinzip und Entartung Wie eben erwähnt können Elektronen die beiden Werte -1/2 und +1/2 für den Spin aufweisen. Teilchen, die halbzahlige Werte für den Spin zeigen, nennt man Fermionen. Außer den Elektronen gehören auch Protonen und Neutronen zu dieser Gruppe. Hat ein Teilchen einen ganzzahligen Spin (z. B. +1, 0, -1), so gehört es zur Gruppe der Bosonen, wie zum Beispiel das Photon. Die Zugehörigkeit zu einer dieser beiden Gruppen hat für Vielteilchensysteme dramatische Folgen. Für Fermionen gilt nämlich das Pauli-Prinzip, das besagt, dass sich Fermionen in mindestens einer Quantenzahl unterscheiden müssen. Dieser nur durch eine relativistische Betrachtung der Quantenmechanik zu verstehende Sachverhalt müsste eigentlich noch als weiteres Postulat eingeführt werden. Für Systeme mit mehreren Elektronen hat das Pauli-Prinzip weit reichende Konsequenzen. Es verbietet nämlich zwei Elektronen, denselben Zustand einzunehmen. Nimmt man außerdem an, dass jedes Mehrelektronensystem im Grundzustand minimale Gesamtenergie aufweist, ergeben sich so die Regeln zur Behandlung dieser Systeme. Wir berechnen die möglichen Energieniveaus, bestimmen die Anzahl der vorhandenen Elektronen im System und füllen dann die Energieniveaus von „unten nach oben“1 auf. Neben unseren Quantentöpfen gilt dieses Prinzip auch für Atome und Moleküle und ebenso, wenn sich diese zu einem Festkörper zusammenschließen. Das Pauli-Prinzip wird speziell bei der Behandlung von Elektronen im Kristall in den Kapiteln 4 und 5 noch eine wichtige Rolle spielen. 3.2. Das Wasserstoffatom 3.2.1. Die Wellenfunktionen Genau wie für die abstrakten Potentialtöpfe des letzten Kaptitels muss man für das Wasserstoffatom zunächst die passende Schrödingergleichung aufstellen und diese dann lösen. Im einfachsten Fall besteht unser System aus zwei Teilchen, einem Proton und einem Elektron. 1 Später wird sich zeigen, dass sich die Elektronen bei endlichen Temperaturen nicht nur in den niedrigstmöglichen Zuständen befinden. - 62 - Abbildung 3.2-1 zeigt die Situation. y Elektron me Proton Abbildung 3.2-1: Das Wasserstoffatom besteht aus einem Proton (roter Kreis, Masse mK) und einem Elektron (blauer Kreis, Masse me). Bei exakter Behandlung des Problems hängt die Lösung von G G den Ortsvektoren r und r der beiden Teilchen ab. r mK re e rK z K Nimmt man den schweren Kern als ortsfest an oder separiert Schwerpunktsbewegung und Relativbewegung, so reicht es aus, den Abstand r zwischen beiden Komponenten zu betrachten. x Das Aufstellen der Gleichung ist noch einfach, wir erhalten: − G G G G G G =2 =2 e2 1 G G ∆ eψ (re , rK ) − ∆ Kψ (re , rK ) − ψ (re , rK ) = Wψ (re , rK ) 2me 2mK 4πεε 0 r 3.2-1 V(r) Die ersten beiden Terme bezeichnen die kinetische Energie des Elektrons beziehungsweise des Kerns. Da beide Teilchen die Elementarladung e tragen, wird für das Potential ein Coulombpotential angesetzt, das nur vom Abstand vom Elektron zum Kern abhängt. Da der Kern viel schwerer ist als das Elektron (mK=1837me), kann man die langsamen Bewegungen des Kerns gegenüber der schnellen Elektronenbewegung vernachlässigen. Diesen Vorgehen wird Born-Oppenheimer-Näherung genannt und ist besonders für Systeme aus drei oder mehr Teilchen geeignet, die ohne Näherungen analytisch unlösbar sind. Unser Problem reduziert sich so in eine Bewegungsgleichung des Elektrons in dem Potential des ortsfesten Protons, dessen Aufenthaltsort wir in den Ursprung des Koordinatensystems legen (Abbildung 3.2-2). - 63 - y Elektron 0 Potential -20 Proton z -40 -60 -80 10 x 5 0 -5 y Abbildung 3.2-2: In der Born-OppenheimerNäherung wird die langsame Bewegung des schweren Kerns vernachlässigt. Als Ursprung des Koordinatensystems kann der Aufenthaltsort des Kerns gewählt werden. -10 -10 0 -5 5 10 x Abbildung 3.2-3: Darstellung des Potentials in zwei Dimensionen. Der Kern sitzt im Ursprung, so dass das Coulomb-Potential Rotationssymmetrie um diesen besitzt. Mit diesen Näherungen vereinfacht sich die Gleichung 3.2-1 zu einer Schrödingergleichung für ein Elektron im zentralsymmetrischen Coulombpotential: 3.2-2 G G e0 2 1 G =2 − ∆ψ ( r ) − ψ ( r ) = Wψ ( r ) 2me 4πεε 0 r V (r ) Der erste Schritt zur Lösung dieser Gleichung besteht in der Wahl eines passenden Koordinatensystems. Da es sich um ein zentralsymmetrisches Potential handelt, das also nur vom Radius abhängt, stellen wie bei zentralsymmetrischen Problemen in der Elektrodynamik die Kugelkoordinaten (r, θ, φ) eine gute Wahl dar. Eine kleine Erinnerung zum Thema Kugelkoordinaten enthält die Abbildung 3.2-4: - 64 - Abbildung 3.2-4: Der Punkt P in Kugelkoordinaten. Die Umrechnung der Koordinaten erfolgt gemäß: x1 = r sinθ cos ϕ x2 = r sinθ sin ϕ x3 = r cosθ bzw. r = x12 + x2 2 + x3 2 θ = arc cot x3 x + x22 2 1 x1 für y ≥ 0 arccos 2 2 + x x 1 2 ϕ= x 1 2π − arccos für y < 0 2 2 + x x 1 2 Nach einigen mühsamen Umformungen erhalten wir für den Laplace-Operator in kartesischen Koordinaten ∂2 ∂2 ∂2 ∆= + + ∂x12 ∂x2 2 ∂x3 2 ∂2 ∂2 ∂2 + + bzw. ∂x 2 ∂y 2 ∂z 2 3.2-3 den Ausdruck in Kugelkoordinaten: ∆= 1 ∂2 1 1 ∂ 1 ∂2 ∂ r sin + θ + . r ∂r 2 r 2 sinθ ∂θ ∂θ sin2 θ ∂φ 2 3.2-4 Damit können wir die Schrödinger-Gleichung 3.2-2 zu folgendem Ausdruck umschreiben: 1 ∂2 1 (rψ ) + 2 2 r ∂r r 1 ∂ ∂ψ sinθ ∂θ sinθ ∂θ e2 1 1 ∂ 2ψ 2m = − 2 W + ψ + 2 2 = 4πε r sin θ ∂φ 3.2-5 Auf den ersten Blick scheinen wir mit den durchgeführten Umformungen nicht viel erreicht zu haben, die Gleichung sieht auch in Kugelkoordinaten nicht sonderlich erquicklich aus. Wir können allerdings jetzt eine Lösung mit einem Separationsansatz suchen. Das heißt, dass wir unsere Wellenfunktion als die Produktwellenfunktion zweier Komponenten ansetzen, die erste hängt nur vom Radius, die zweite nur von den Winkelkoordinaten ab: ψ (r ,θ ,φ ) = f (r )Y (θ ,φ ) 3.2-6 - 65 - Es ergeben sich nun genau wie beim dreidimensionalen Quantenpunkt wieder verschiedene Zustände mit bestimmten Energieeigenwerte und Quantenzahlen und es tritt auch wieder Entartung auf. Die mathematische Ableitung der genauen Wellenfunktionen ist im Anhang I dargestellt. Die Eigenzustände ψ n,l ,m,s (r ,θ ,φ ) lassen sich nach den verschiedenen Quantenzahlen n,l,m klassifizieren. Für die erlaubten Quantenzahlen gelten die folgenden Einschränkungen: n = 1,2,3,… (Hauptquantenzahl) l = 0,1,2, …n-1 (Nebenquantenzahl, Drehimpulsquantenzahl) m = -l,-l+1,..0,..l (Magnetquantenzahl) s = -½,½ Die Energieeigenwerte hängen hierbei nur von der Hauptquantenzahl ab: Wn = − W 1 e4m = − Ryd 2 2 2 2= (4πε 0 ) n n2 3.2-7 . Hierbei ist die Rydbergkonstante WRyd = 13.6 eV. Alle Zustände sind wiederum entartet. Für die ersten beiden Hauptquantenzahlen ergeben sich z.B. die folgenden Möglichkeiten für die Wahl der anderen Quantenzahlen. Hauptquantenzahl Drehimpulsquanten- Magnetquantenzahl Spinquantenzahl n zahl l m s 1 0 0 -½ ½ 2 0 0 -½ ½ 1 -1 -½ ½ 1 0 -½ ½ 1 1 -½ ½ - 66 - 3.2.2. Interpretation der Ergebnisse In Abbildung 3.2-5 findet man die ersten Energieniveaus in einen Schnitt durch das Coulombpotential aufgetragen. Abbildung 3.2-5: In Übereinstimmung mit dem Bohrschen Atommodell findet man für das zentralsymmetrische Potential des Wasserstoffatoms quantisierte Energiewerte. Abbildung 3.2-6: Das optische Spektrum des Wasserstoffatoms kann durch die diskreten Energieniveaus erklärt werden. Beim Übergang von einem Zustand Wn1 auf einen niederenergetischen Wn2 wird ein Photon der Frequenz f2→1 = (Wn 2 − Wn1 ) / h ausgesendet werden. Die räumliche Aufenthaltswahrscheinlichkeit des Elektrons im Wasserstoffatom ergibt sich als Absolutquadrat der Wellenfunktion |ψ(r,θ,φ)|2, die von den Parametern n, l und m abhängt. Höhere Drehimpulsquantenzahlen bedeuten eine größere Abweichung von einer kugelsymmetrischen Elektronenverteilung. Die Abbildung 3.2-7 illustriert einige Wellenfunktionen. - 67 - s-Orbital d-Orbitale p-Orbitale Abbildung 3.2-7: Schema einiger Orbitale(s-Orbital: l=0, p-Orbital: l=1, d-Orbital: l=2) Bei der Bezeichnung der Wellenfunktionen oder Orbitale haben sich kleine Buchstaben anstelle der Drehimpulsquantenzahl eingebürgert. Der Hauptquantenzahl wird in der Bezeichnung des Zustands der Buchstabe entsprechend der Drehimpulsquantenzahl nachgestellt, ein 2p Zustand hat also n=2 und l=1. Auch die Magnetquantenzahl wird meistens durch Buchstaben angegeben. So werden die in Abbildung 3.2-7 dargestellten p-Orbitale meistens entsprechend ihrer Ausrichtung entlang einzelner Koordinatenachsen als px,py und pz-Orbitale bezeichnet. Im Energiediagramm in Abbildung 3.2-8 sind die untersten Energieniveaus des Wasserstoffatoms aufgetragen. Im realen Wasserstoffatom ist bei genauem Hinschauen die Entartung der Energieniveaus aufgehoben. Dieses rührt von Prozessen her, die wir in unserer vereinfachten Darstellung für das Wasserstoffatom vernachlässigt haben. So müssen zum Beispiel relativistische Korrekturen durchgeführt werden, die sowohl von der Hauptquantenzahl, als auch von der Drehimpulsquantenzahl abhängen. Im Energieschema des Wasserstoffs fällt des Weiteren die Spin-Bahn-Kopplung, eine Wechselwirkung zwischen dem Magnetfeld, das durch die Bahnbewegung des Elektrons erzeugt wird und dem Spin, ins Gewicht. Weitere Effekte wie die Kopplung des magnetischen Moments des Kerns mit Bahnmoment und Spin sind ebenfalls nur mit speziellen Vorrichtungen messbar. - 68 - W Abbildung 3.2-8: Die untersten Energieniveaus des Wasserstoffatoms. -WI - 69 -