Hydromechanik und Thermodynamik Inhaltsverzeichnis
Werbung

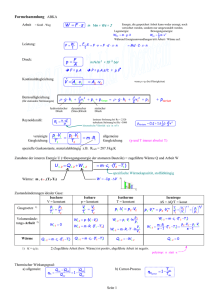
Skript zum Ferienkurs Physik für Elektroingenieure Wintersemester 2015 / 16 Nr. 4 Katrin Oberhofer 17.03.2016 Hydromechanik und Thermodynamik Inhaltsverzeichnis Hydromechanik und Thermodynamik 1 1 Definition des Fluids 2 2 Arten von Fluiden 2 3 Hydrostatik 3.1 3.2 3.3 3.4 3.5 3.6 3.7 3 Dichte & Druck . . . . . . . . . . . . . . . Pascalsches Prinzip . . . . . . . . . . . . . Schweredruck, Hydrostatisches Paradoxon Barometrische Höhenformel . . . . . . . . Auftrieb . . . . . . . . . . . . . . . . . . . Hydraulik . . . . . . . . . . . . . . . . . . Kompressibilität . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 3 3 3 4 4 5 5 4 Oberflächenspannung 5 5 Hydrodynamik 7 5.1 5.2 5.3 5.4 5.5 5.6 5.7 Strömungen . . . . . . . . . Kontinuitätsgleichung . . . Bernoulligleichung . . . . . Gesetz von Toricelli . . . . . Viskosität . . . . . . . . . . Gesetz von Hagen-Poiseuille Strömungswiderstand . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 7 8 8 9 10 10 12 6 Stoffmenge, Avogadrogesetz 7 Ideales Gas 13 7.1 Die ideale Gasgleichung . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 13 8 9 13 Innere Energie und Wärme 14 8.1 Wärme . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 8.2 Innere Energie . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 8.3 Kinetische Gastheorie . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 14 14 15 Thermodynamische Systeme 16 9.1 Definitionen . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 9.2 1. Hauptsatz der Thermodynamik . . . . . . . . . . . . . . . . . . . . . . . . . 16 17 9.3 Zustandsänderungen 9.3.1 Isobare . . . 9.3.2 Isochore . . . 9.3.3 Isotherme . . 9.3.4 Adiabaten . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 10 Entropie 10.1 (Ir)Reversible Prozesse . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 10.2 2. Hauptsatz der Thermodynamik . . . . . . . . . . . . . . . . . . . . . . . . . 11 Kreisprozesse 11.1 Carnotscher Kreisprozess . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 11.2 Wirkungsgrad . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 12 Reales Gas 17 17 18 18 19 20 20 20 21 21 23 23 Hydromechanik 1 Definition des Fluids Die Hydrodynamik bezeichnet die Mechanik von flüssiger oder gasförmiger Materie. Die Unterscheidung von Festkörpern und Fluiden erfolgt durch die Betrachtung der Wirkung kleinster Scherspannungen. Festkörper reagieren auf Scherspannungen mit einer endlichen Abbildung 1: Wirkung von Scherspannungen auf Festkörper und Fluide Verformung und nehmen die ursprüngliche Form wieder an, wenn die Scherspannung weg ist. Fluidpartikel können sich frei gegeneinander bewegen und fließen unter der kleinsten tangentialen (Scher-) Kraft. Sie reagieren auf Scherspannungen mit einer endlichen Verformungsgeschwindigkeit. 2 Arten von Fluiden Man unterscheidet zwei Arten von Fluiden: • Gase sind Fluide mit schwachen Anziehungskräften zwischen den einzelnen Fluidpartikeln. Ein Gas füllt stets den ganzen zur Verfügung stehenden Raum in einem Behälter aus und bildet keine freie Oberfläche. • Flüssigkeiten sind Fluide mit starken Anziehungskräften zwischen den einzelnen Fluidpartikeln. Sie behalten Ihr Volumen bei und bilden freie Oberfläche sogar gegen Vakuum aus. 3 Hydrostatik 3.1 Dichte & Druck Die Massendichte ρ von Materie bezeichnet das Verhältnis der schweren Masse m und des Volumens V eines Körpers. ρ= m V Als Einheit dient die Kombination der SI Einheiten kg/m3 . Oftmals wird auch die Einheit g/cm3 verwendet (Umrechnungsfaktor 1000). Der Druck ist definiert als die auf eine Oberfläche A senkrecht wirkende Kraft FN , oftmals auch Normalkraft FN bezeichnet, geteilt durch durch die Oberfläche A. p= FN A Als Einheit dient im SI-System das sogenannte Pascal, welches als das Verhältnis von den Einheiten der Kraft, dem Newton N, und der Fläche definiert ist. 1Pa (Pascal) = 1 N m2 In der Praxis ist oft die Einheit bar 1bar = 100kPa gebräuchlich. 3.2 Pascalsches Prinzip Das Pascalsche Prinzip besagt, dass sich Druck in Fluiden ungehindert auf jeden Punkt in der Flüssigkeit ausbreitet. Veranschaulicht wird dies im Versuch der kommunizierenden Röhren. Abbildung 2: Veranschaulichung des Pascalschen Prinzips Die Höhe der Wassersäule ist in allen verbundenen Röhren gleich. 3.3 Schweredruck, Hydrostatisches Paradoxon Eine Flüssigkeitssäule der Höhe h und dem Querschnitt A hat die schwere Masse m = ρhA und übt auf ihren Boden die Gewichtskraft F = mg = gρhA aus. Der auf den Boden wirkende Druck p wird als Schweredruck bezeichnet. (1) p = ρ·g·h Diese Gleichung gilt für alle Gefäße unabhängig von ihrer spezifischen Form. Der Schweredruck ist deshalb nur von der Höhe der Fluidsäule abhängig und nicht von der Menge des aufgestauten Fluids! Abbildung 3: Darstellung des hydrostatischen Paradoxons. Der Schweredruck ist überall am Boden des Gefäßes gleich und entspricht dem Druck der gesamten Fluidsäule h. Das Kräftegleichgewicht an den Wänden des ruhenden Gefäßes erzeugt eine dem Innendruck entgegengesetzte Kraft auf das Fluid. 3.4 Barometrische Höhenformel In Gasen ist aufgrund der hohen Kompressibilität die Dichte ρ druckabhängig. Für die Berechnung des Luftdrucks als Funktion der Höhe in der Erdatmosphäre muss diese Druckabhängigkeit berücksichtigt werden. Die Gleichung für den Schweredruck gilt dann nur für eine dünne Schicht h2 − h1 → dh. dp = − g · ρ · dh bei konstanter Temperatur gilt: p p = 0 ρ ρ0 Durch Einsetzen und integrieren ergibt sich die barometrische Höhenformel p(h) = p0 e− gρ0 h/p0 3.5 Auftrieb Der Schweredruck des Wassers wirkt auf alle Seitenflächen eines im Wasser schwebenden Körpers mit Querschnitt A und Höhe h. Die Kräfte auf den Seitenflächen heben sich auf. Die Kräfte auf Grund- und Deckfläche des Körpers hängen von deren Tiefe ab. Abbildung 4: Auftriebskraft Als Auftriebskraft ergibt sich die Differenz der Kräfte auf Grund- und Deckfläche. Fa = F1 − F2 = ρgh1 A − ρgh2 A = ρgV Der Auftrieb entspricht also der Schwerkraft des durch den Körper verdrängten Wassers. Für die Frage ob ein Körper im Wasser schwebt, sinkt oder an die Oberfläche steigt ist also allein dessen Dichte relevant. Ragt ein Teil des Körpers aus dem Wasser heraus so trägt dieses Volumen nicht zum Auftrieb bei und es stellt sich ein Kräftegleichgewicht zwischen Schwerkraft und Auftriebskraft ein. 3.6 Hydraulik Das Pascalsche Prinzip kann analog zu den Hebelgesetzen eingesetzt werden um mechanische Kräfte zu übersetzten. Veranschaulicht wird dies in der Wirkung einer Hydraulischen Presse: Abbildung 5: Hydraulische Presse Nach dem Pascalschen Prinzip ist der Druck in beiden Behältern gleich. Wirkt nun eine Kraft F1 = p · A1 auf den kleineren Zylinder, so ergibt sich bei konstantem Druck p eine Kraft auf den größeren Zylinder F2 = p · A2 . F2 = A2 · F1 A1 Die durch diese Kraft verrichtete Arbeit wird als Druckarbeit W bezeichnet W1 = F1 · ∆x1 = p · A1 · ∆x1 = p · ∆V. Unter Vernachlässigung von Reibung, d.h. W1 = −W2 , und für inkompressible Flüssigkeiten, d.h. ∆V1 = −∆V2 , folgt dann das hydraulische Hebelverhältnis: x2 = A1 · x1 A2 3.7 Kompressibilität Reale Fluide können durch die Ausübung von Druck komprimiert werden. Die Kompressibilität κ eines Materials ist definiert als die relative Volumenänderung pro Druckänderung κ=− 1 dp V dV Die Kompressibilität eines Fluids ist abhängig von seiner Art und seinen Zustandsgrößen wie Druck und Temperatur. Dabei sind Flüssigkeiten durch eine geringe Kompressibilität charakterisiert. Gase hingegen sind aufgrund der geringen Teichendichte in hohem Maße kompressibel. 4 Oberflächenspannung Eine Flüssigkeit wird durch die Anziehungskraft zwischen den Molekülen zusammengehalten. Auf Moleküle im Inneren der Flüssigkeit hebt sich die Summe der Kräfte zu den anderen Molekülen im zeitlichen Mittel auf. Auf Moleküle an der Phasengrenzfläche ergibt sich eine Summenkraft, die in die Flüssigkeit hinein gerichtet wirkt. Abbildung 6: Darstellung der Oberflächenspannung Die Oberflächenspannung σ versucht die Oberfläche A des Fluids möglichst klein zu halten. Sie ist definiert als die pro Flächenzuwachs dA zu verrichtende Arbeit dE dE = σdA. Diese Energieänderung erzeugt eine Kraft die entgegen der Vergrößerung der Oberfläche wirkt. Ziehen wir den Balken nach rechts verrichten wir gegen die Oberflächenspannung Arbeit. ∆W = F∆x Die Vergrößerung der Oberfläche ist ∆A = 2l · ∆x Daraus kann die Randkraft berechnet werden. F = 2l · σ Die Randkraft ist also proportional zum Umfang und zur Oberflächenspannung. Für die Grenzfläche zwischen Flüssigkeiten und Festkörpern, kann die Energieänderung positiv oder negativ sein, je nachdem ob die Anziehungskräfte zwischen Flüssigkeitsmolekülen und dem Festkörper kleiner oder größer ist als zwischen den Molekülen der Flüssigkeit. Aus der durch die Oberflächenspannung resultierenden Kraft folgt der Kapillareffekt, d.h. das Ansteigen oder Absinken von Flüssigkeit in dünnen Rohren. Dies führt zur Ausbildung von Tropfen auf Oberflächen oder zur Benetzung des Festkörpers mit der Flüssigkeit. Ein quantitatives Maß für das Verhalten einer Flüssigkeit auf einer Festkörperoberfläche ist der Kontaktwinkel Φ. Die Steigungshöhe im Rohr kann aus dem Gleichgewicht von Gewichtskraft und Oberflächenkraft(Randkraft) berechnet werden: hkap = 2σ cos(Φ) ρgr Abbildung 7: Kapillareffekt für Flüssigkeiten unterschiedlichen Kontaktwinkels in einem dünnen Glasröhrchen 5 Hydrodynamik 5.1 Strömungen Die Hydromechanik beschreibt die Bewegungen von Fluiden als Wirkungen innerer und äusserer Kräfte und Spannungen. Die Bewegung einen Fluids wird auch als Strömung bezeichnet. Mathematisch können Strömungen z.B. im Bild der Massenpunkte verstanden werden. Dabei hat jeder Massepunkt des Fluids eine individuelle Bahn. • Stromfaden: Die Bahn eines individuellen Massepunktes • Stromlinie: Gesamtheit der Vektoren der Geschwindigkeiten an allen Punkten des Stromfadens Für stationäre Strömungen, d.h. die Stromlinien sind nicht von der Zeit abhängig, sind Stromfaden und Stromlinien identisch. Stationäre Strömung bedeutet nicht, dass sich die Geschwindigkeit eines Massepunktes nicht mit der Zeit ändert. Man unterscheidet hierbei zwischen zwei allgemeinen Fällen: • Laminare Strömung: Bei kleinen Geschwindigkeiten und starker innerer Reibung des Fluids richten sich die die Stromlinien so parallel wie möglich aus. (Wasser in dünnem Rohr) • Turbulente Strömung: Bei hohen Geschwindigkeiten und schwacher innerer Reibung bilden sich Verwirbelungen der Stromlinien. (Luftumströmung eines Fahnenmasten) Abbildung 8: Darstellung von Stromlinien laminarer und turbulenter Strömung 5.2 Kontinuitätsgleichung Für stationäre Strömungen gilt: Durch jeden Punkt im Rohr muss in derselben Zeit die gleiche Menge an Flüssigkeit strömen. Das heißt der Massenstrom dM/dt = ρAv ist eine Erhaltungsgröße. Abbildung 9: Darstellung der Kontinuitätsgleichung Es gilt, dass die Masse dm des Volumenelementes A1 ds1 dass pro Zeitintervall dt durch einen Querschnitt A1 fließt (2) dm = ρ1 · A1 ds1 = ρ2 · A2 ds2 eine konstante an allen Orten des Rohrs ist. Für inkompressible Fluide gilt weiterhin, dass die Dichte an allen Orten und zu allen Zeiten konstant ist, d.h. ρ1 = ρ2 , und der Volumenstrom (3) dV = A1 v1 = A2 v2 = const. dt ebenfalls Erhaltungsgröße ist. Man kann also die Fließgeschwindigkeit an allen Stellen im Rohr sofort berechnen, wenn die Querschnitte und der Volumenstrom bekannt sind. 5.3 Bernoulligleichung Für die stationäre Strömung und unter Vernachlässigung von Reibungskräften gilt der Energieerhaltungssatz. Das heißt die Summe aus potentieller Energie (Druck- und Lageenergie) und kinetischer Energie ist erhalten. Für ein Massenelement ρdV folgt, dass Änderungen der Lageenergie ρ · dV · g · h und der kinetischen Energie 1/2ρ · dV · v2 durch die Druckarbeit pdV ausgeglichen werden. Abbildung 10: Die grüne Flüssigkeitsmenge ist um y2 − y1 angehoben worden und wurde von v1 auf v2 beschleunigt. Es folgt also 1 pdV + ρdVv2 + ρdVgh = const. 2 Das unbekannte Volumenelement kann aus der Gleichung eliminiert werden und man erhält die Bernoulligleichung. 1 p + ρv2 + ρgh = const. 2 (4) Zusammen mit der Kontinuitätsgleichung ist damit der Druck an allen Stellen im Rohr durch den Querschnitt und die Lage im Raum zu errechnen. 5.4 Gesetz von Toricelli Abbildung 11: Darstellung des Gesetzes von Toricelli Die Geschwindigkeit v des ausströmenden Wassers aus dem Loch B kann aus der Bernoulligleichung hergeleitet werden. Auf den beiden Ebenen A und B lastet jeweils der Atmosphärendruck p A = pB , da das Gefäß auf beiden Ebenen offen ist. Für die Geschwindigkeit des ausströmenden Wassers folgt nun: 1 p A + ρgy A = pB + ρg(y A − h) + ρv2 2 Die Fließgeschwindigkeit im Behälter wird vernachlässigt (kleines Loch). Es folgt die Geschwindigkeit v des ausströmenden Wassers: p v = 2gh Das gleiche Ergebnis folgt aus der Energieerhaltung. 5.5 Viskosität Bisher haben wir die Mechanik der Fluide unter Vernachlässigung der Reibung betrachtet. Die innere Anziehungskraft der Fluidpartikel führt zu Reibungskräften, wenn verschiedene Flüssigkeitsschichten mit unterschiedlicher Geschwindigkeit aneinander vorbei strömen. Eine konstante Geschwindigkeit kann nur durch ständiges Anlegen der treibenden Kraft erreicht werden. Abbildung 12: Geschwindigkeitsprofil einer viskosen Flüssigkeit bei laminarer Strömung zwischen planparallelen Platten Wir betrachten die Bewegung einer Flüssigkeit zwischen zwei planparalellen Platten der Fläche A, von denen eine mit konstanter Geschwindigkeit v bewegt wird. Es wird angenommen, dass die Flüssigkeit direkt an den Platten mit derselben Geschwindigkeit bewegt wird, d.h. dass die erste Molekülschicht der Flüssigkeit an der Platte haftet. Ist die innere Reibungskraft unabhängig von der Fließgeschwindigkeit (Newtonsche Flüssigkeit), so stellt sich ein lineares Geschwindigkeitsprofil ein. Als zum Antrieb notwendige Kraft Ft findet man v Ft = η A . z Die dynamische Viskosität wird mit η bezeichnet und ist eine Materialeigenschaft, die aber stark von der Temperatur abhängt. Ihre Einheit ist Ns/m2 . Eine allgemeinere Formulierung der viskosen Reibungskraft gelingt durch die Einführung der Schubspannung τ. τ= dFt dvx =η dA dz 5.6 Gesetz von Hagen-Poiseuille Eine technisch bedeutsame Anwendung ist die Berechnung der laminaren Rohrströmung. Abbildung 13: Kräftegleichgewicht der laminaren Rohrströmung Wir betrachten ein Zylinderelement mit Radius r in einem Rohr der Länge l und Mantelfläche A = 2πrl. Die Kraft Fp des treibenden Drucks auf das Zylinderelement ist Fp = πr2 (p1 − p2 ), und gleicht der auf die Zylindermantelfläche wirkenden Reibungskraft dv dv = η2πrl . dr dr Durch Aufstellen des Kräftegleichgewichts Fp = Ft und lösen der Differentialgleichung mit der Randbedingung, dass die Flüssigkeit am Rande des Rohres r = R ruht, erhält man das Geschwindigkeitsprofil der laminaren Rohrströmung: Ft = η A v(r ) = p1 − p2 · ( R2 − r 2 ) 4ηl Aus dem Geschwindigkeitsprofil kann man den Volumenstrom durch die Rohrleitung berechnen. Abbildung 14: Darstellung des zylinderförmigen Volumenelementes und des parabolischen Geschwindigkeitsprofils Die Integration findet über die ringförmigen Volumenelemente der Dicke dr statt mit Volumenstrom dV̇ = 2πrdrv(r ), und es folgt der gesamte Volumenstrom V̇ = Z R 0 p1 − p2 2 2 2πr · R − r dr 4ηl Nach Lösen des Integrals und Umformung erhält man das Gesetz von Hagen-Poiseuille für die laminare Rohrströmung. V̇ = π (p1 − p2 ) 4 R 8ηl 5.7 Strömungswiderstand Werden Festkörper von Fluiden umströmt, so ergibt sich aufgrund der Reibungskräfte im Fluid eine Kraft auf den Körper, welche als Strömungswiderstand bezeichnet wird. Hierbei gibt es große Unterschiede zwischen laminarer Strömung und turbulenter Strömung. Die Art der Umströmung eines Körpers hängt von vielen Faktoren ab, die in der sogenannten Reynoldszahl zusammengefasst sind Re = vρL , η wobei v die Strömungsgeschwindigkeit ist, ρ die Dichte des Fluids, L die charakteristische Größe des Objekts senkrecht zur Flussrichtung und η die dynamische Viskosität. Abbildung 15: Darstellung der Stromlinien turbulenter Umströmung einer Platte Bei der turbulenten Strömung kann die Reibung über die Arbeit, die verrichtet werden muss, um die Fluidpartikel von der Geschwindigkeit v auf 0 abzubremsen, errechnet werden. v2 Ft = cW Aρ 2 Der Strömungswiderstandskoeffizient cW hängt von der Gestalt und der Oberfläche des Körpers sowie dem Turbulenzgrad der Strömung ab. Für die laminare Strömung ergibt sich analog zur Reibungskraft der ebenen Platte eine lineare Abhängigkeit von Reibungskraft und Strömungsgeschwindigkeit. Abbildung 16: Stromlinien der laminaren Umströmung einer Kugel Ein Beispiel ist die Stokessche Reibungsformel für laminare Strömungen und kugelförmige Körper. Ft = 6πηrv Thermodynamik 6 Stoffmenge, Avogadrogesetz Gleiche Volumina idealer Gase enthalten bei gleichem Druck und bei gleicher Temperatur gleich viele Moleküle. Ein Volumen von 22.4l eines idealen Gases unter Normalbedingungen (p = 1013mbar, T = 273K ) enthält immer dieselbe Anzahl Atome oder Moleküle, nämlich 1Mol. In einem Mol befinden sich NA = 6.022 · 1023 Gasatome/-moleküle. Diese Zahl wird als Avogadrokonstante bezeichnet. 7 Ideales Gas Als ideales Gas bezeichnet man in der Physik eine idealisierte Modellvorstellung eines realen Gases. Zur Vereinfachung der physikalischen Betrachtung geht man von folgenden drei Annahmen aus: • Punktteilchen, d.h. Moleküle haben kein eigenes Volumen • Keine Wechselwirkung zwischen den Teilchen • Stöße der Moleküle untereinander und mit den Wänden sind elastisch Der Zustand eines idealen Gases wird durch die Zustandsgrößen Volumen V, Druck p, absolute Temperatur T in K und die Teilchenzahl N beschrieben. 7.1 Die ideale Gasgleichung Experimentiell findet man zwischen den Zustandsgrößen folgende Zusammenhänge: a) Gesetz von Boyle und Mariotte (T = const. und N = const.): p · V = const. b) Gesetz von Gay-Lussac (p = const. und N = const.): V = const. T c) Gesetz von Amontons (V = const. und N = const.): p = const. T d) Ausserdem findet man für p = const. und T = const. N = const. V Aus diesen empirischen Beobachtungen, die jeweils für viele Gase über weite Temperatur und Druckbereiche hervorragende Beschreibungen der makroskopischen physikalischen Situtaion erlauben, folgt die Zustandsgleichung des idealen Gases (5) pV = Nk B T, mit der Boltzmann-Konstante k B = 1.38 · 10−23 J/K. Statt der Teilchenzahl N kann die ideale Gasgleichung auch mit der Molzahl ν = N/NA formuliert werden (6) pV = νRT, wobei R = 8.314J/(mol · K ) als Gaskonstante bezeichnet wird. Es gilt R (7) kB = NA Die Gaskonstante ist R = 8.314 J/(mol K ). 8 Innere Energie und Wärme 8.1 Wärme Wärme ist die Energie, die von einem Körper zum anderen aufgrund einer Temperaturdifferenz übertragen wird. Wird den Teilchen eines Körpers durch Zufuhr von Wärme Q Energie zugeführt, erhöht sich die Temperatur proportional zur zugeführten Wärme. Q = C · ( T2 − T1 ) Hierbei ist C die Wärmekapazität mit Einheit J/K. Sie ist ein Maß daüfr, welche Wärmemenge notwendig ist, um einen Körper um ein Grad Kelvin zu erwärmen. Die Wärmekapazität eines Körpers geteilt durch die Masse des Körpers ergibt die spezifische Wärmekapazität c mit Einheit J/(kgK ). Sie ist eine Materialkonstante und beschreibt die Fähigkeit eines Materials aufgrund seiner atomaren Struktur Wärme aufzunehmen und zu speichern. Für Gase muss zwischen der spezifischen Wärme bei konstantem Druck cp oder konstantem Volumen cV unterschieden werden, weil bei der Ausdehnung des Gases bei konstantem Druck Druckarbeit Wp = pdV verrichtet wird. Ihr Verhältnis cp κ= cV wird Adiabatenindex genannt. Aus der idealen Gasgleichung sehen wir, dass bei konstantem Druck p bei einem Anstieg der Temperatur T auch das Volumen V ansteigt. Der Betrag der vom Gas geleisteten Arbeit ist |∆W | = p∆V Diese Energie muss dem Gas zusätzlich zugeführt werden. Die Wärmekapazität ist höher. Bei konstantem Volumen hingegen wird keine zusätzliche Arbeit verrichtet. 8.2 Innere Energie Die innere Energie U eines Gases im Volumen V bezeichnet den gesamten Energieinhalt des Volumens, soweit es vom inneren Zustand abhängt, d. h. die gesamte Energie seiner Moleküle. Voraussetzung ist, dass sich das Gas in Ruhe und im thermodynamischen Gleichgewicht befindet. Die innere Energie umfasst insbesondere: • die thermische Bewegungsenergie der Gasteilchen, • die chemische Energie der Moleküle, usw. Wird das gesamte Volumen bewegt oder befindet sich in einem äußerem Potential, so werden diese makroskopischen Energien nicht zur inneren Energie gezählt, da sie von externen Kräften abhängen. 8.3 Kinetische Gastheorie Die kinetische Gastheorie leitet die makroskopischen Eigenschaften des idealen Gases aus den mikroskopischen Bewegungen und Stößen der einzelnen Atome her. Der Schritt von mikroskopischen, mechanischen Bewegungen zur makroskopischen thermodynamischen Zustandsgröße erfolgt durch Summation über alle ≈ 1023 Teilchen. Der makroskopische Druck lässt sich durch den Impulsübertrag der Stöße der Gasteilchen mit der Wand erklären. Die aufsummierte Impulsänderung aller Stöße pro Zeitintervall erlaubt dann die Berechnung von Kraft F und Druck p. Abbildung 17: Molekül 1 führt in ∆t einen Wandstoß aus, der Impuls wird wegen des elastischen Stoßes an der Wand gespiegelt. Die Geschwindigkeit von Molekül 2 senkrecht zur Wand reicht nicht aus, um in ∆t die Wand zu erreichen. Die Impulsänderung des einzelnen Stoßes ist ∆p = 2mvz . Die Moleküle Z die im Zeitintervall ∆r die Wand mit Fläche A treffen sind höchstens vz ∆t von der Wand entfernt. Z= 1 N Avz ∆t V 2 Hierbei ist N/V die Teilchendichte, und der Faktor 1/2 berücksichtigt, dass nur die Hälfe der Moleküle auf die Wand zu fliegen. Die gesamte Impulsänderung der Gasmoleküle beim Wandstoß in ∆t ist: ∆pz = ∆pZ = Fz ∆t = pA∆t Auflösen der Gleichung ergibt den kinematischen Druck: N D E p = m v2z V Die Klammern hi bezeichnen die Summation und Mittelung über alle Moleküle. Die Mittelung und das Quadrat kommutieren nicht! D E v2 6 = h v i2 Die mittlere kinetische Energie eines Teilchens kann so mit den makroskopischen Zustandsgrößen in Bezug gebracht werden. 1 D E 1 D E D E D E 3 D E Ēkin = m v2 = m v2x + v2y + v2z = m v2z 2 2 2 Über die ideale Gasgleichung können die makroskopischen thermodynamischen Zustandsgrößen so mit der mikroskopischen Geschwindigkeit und kinetischen Energie in Bezug gebracht werden. Einsetzten in die ideale Gasgleichung und vereinfachen liefert Ēkin = 3 kB T 2 Die absolute Temperatur ist ein Maß für die Bewegungsenergie eines Moleküls. Die absolute Temperatur 0K kann nicht erreicht werden, da immer langsamer werdende Moleküle immer weniger Energie über Stöße abgeben können. Es folgt die innere Energie des idealen Gases U |V =const. = N · Ēkin = (8) 3 3 Nk B T = νRT 2 2 und damit die Wärmekapazität bei konstantem Volumen CV = dQ dU 3 = = Nk B dT dT 2 Die Wärmekapazität bei konstantem Druck ist höher da zusätzlich Ausdehnungsarbeit verrichtet wird. Mit der Definition der inneren Energie und der idealen Gasgleichung folgt. Cp = dU pdV 3 5 dQ = + = Nk B + Nk B = Nk B dT dT dT 2 2 Und damit der Adiabatenexponent des idealen Gases. κ= Cp = 1.4 CV 9 Thermodynamische Systeme 9.1 Definitionen In der Thermodynamik unterscheidet man im Allgemeinen unter offenen, geschlossenen und abgeschlossenen Systemen. Abbildung 18: Darstellung offener, geschlossener und abgeschlossener Systeme 9.2 1. Hauptsatz der Thermodynamik Die Änderung der inneren Energie ∆U eines Systems ist gleich der Summe der mit der Umgebung ausgetauschten Wärme ∆Q und der am System bzw. vom System verrichteten Arbeit ∆W. (9) ∆U = ∆Q + ∆W bzw. dU = δW + δQ Der erste Hauptsatz der Thermodynamik ist direkte Folge der Energieerhaltung und verbietet die Konstruktion einer Maschine mit einem Wirkungsgrad größer eins. 9.3 Zustandsänderungen Zustandsänderungen eines Systems können als Wege im Druck-Volumen-Diagramm (kurz pV-Diagramm) dargestellt werden. Die vom System geleistete Arbeit ist (10) δW = −p · dV Die Vorzeichenkonvention ist wie folgt: • δW < 0 Das System verrichtet Arbeit an seiner Umgebung (Expansion) • δW > 0 Die Umgebung verrichtet Arbeit am System (Kompression) Da V2 > V1 expandiert das Gas im System unseres Beispiels und verrichtet Arbeit am System. Die Arbeit ist folglich (11) W1→2 = − Z 2 pdV. 1 Aus dem p-V-Diagramm sieht man sofort, dass die Arbeit und somit auch die Wärme des Systems nicht nur von den beiden Endzuständen abhängen sondern auch vom Integrationsweg. Im Folgenden diskutieren wir einige Spezialfälle der Zustandsänderung. Aus diesen kann man alle technisch relevanten thermodynamischen Kreisprozesse (Carnot, Otto, Diesel, usw.) konstruieren und berechnen. 9.3.1 Isobare Ein isobarer Prozess beschreibt eine Zustandsänderung mit konstantem Druck (vgl. Gesetz von Gay-Lussac). Die Isobare ist eine im p-V-Diagramm horizontale Linie. Die innere Energie berechnet sich zu: (12) ∆U12 = U2 − U1 = W12 + Q12 Im System zugefügte Arbeit: (13) W12 = − Z 2 1 pdV = − p Z 2 1 dV = − p(V2 − V1 ) Im idealen Gas ist Cp konstant und die Wärmeenergie folgt als (14) Q12 = Z 2 1 Cp dT = Cp ∆T = C p p∆V νR 9.3.2 Isochore Ein isochorer Prozess beschreibt eine Zustandsänderung mit konstantem Volumen (vgl. Gesetz von Antomons). Die Isochore ist eine im p-V-Diagramm vertikale Linie. Zugeführte Wärme leistet keine Arbeit. Nur Erhöhung der inneren Energie, d.h. Temperaturerhöhung. Im idealen Gas ist CV konstant und die Wärmeenergie folgt als Q12 = CV ( T2 − T1 ) = ∆U12 (15) 9.3.3 Isotherme Ein isothermer Prozess findet bei konstanter Temperatur statt (vgl. Gesetz von Boyle und Mariotte). Dies wird durch einen im Vergleich zum Prozess schnellen Wärmeaustausch mit der Umgebung realisiert. Weil sich hierbei die innere Energie des idealen Gases ∆T ∝ ∆U = 0 nicht ändert, wird zugeführte Wärme direkt in Arbeit umgesetzt. Die Berechnung der verrichteten Arbeit erfolgt durch Integration der idealen Gasgleichung: (16) W12 = − Z 2 1 pdV = − Z 2 νRT 1 V dV = νRTln V1 V2 Die freiwerdende Wärme folgt sogleich: Q12 = −W12 = −νRTln (17) V1 V2 Die Isotherme ist eine Hyperbel im p-V-Diagramm. 9.3.4 Adiabaten Adiabatische Prozesse finden ohne jeden Wärmeaustausch mit der Umgebung statt. Dies geschieht entweder, weil die Prozesse viel schneller vonstatten gehen als der Temperaturausgleich, oder wenn die Prozesse in einem abgeschlossenem System ablaufen. Aus dem ersten Hauptsatz folgt mit ∆Q = 0 ∆U12 = ∆W12 = CV ( T2 − T1 ) (18) Wir können schreiben δW = −pdV = − νRT dV V δU = CV dT und es folgt nach Integration ln T2 νR V = − ln 2 T1 CV V1 Für ideale Gase folgen mit dem Adiabatenindex κ = Cp /CV = 1 + (νR)/CV die Adiabatengleichungen T · V κ −1 = const. p · V κ = const. Abbildung 19: Adiabaten und Isothermen im p-V-Diagramm Bei der adiabatischen Expansion wird die mechanische Arbeit der inneren Energie entnommen. Die sinkende Temperatur hat einen niedrigeren Endruck zur Folge im Vergleich zur äquivalenten isothermen Expansion. 10 Entropie Die Entropie S ist eine thermodynamische Zustandsgröße, die wie Temperatur, Volumen und Druck den Zustand eines Systems beschreibt. Die Entropie ist ein Maß für die Anzahl der Mikrozustände, durch die der beobachtete Makrozustand des Systems realisiert werden kann – anders ausgedrückt: Entropie ist ein Maß für die Unordnung eines Systems. Die Entropieänderung ist definiert als dS = dQ T Die Änderung der Entropie S in einem abgeschlossenen System (bleibt konstant oder steigt) ist ein Maß für die Irreversibilität eines Vorgangs (reversibel/irreversibel). Anmerkung: Adiabatische Zustandsänderungen sind durch dQ = 0 definiert. Die Entropie S bleibt bei adiabatischen Zustandsänderungen konstant! 10.1 (Ir)Reversible Prozesse Die Irreversibilität bestimmter Prozesse kann man z.B. für ideale Gase mit Hilfe des ersten Hauptsatzes ∆U = ∆Q − p∆V berechnen. dS = dU pdV dV dT dQ = + = νCV + νR T T T T V Integrieren für konstantes CV gibt: ∆S = νCV · ln T2 V + νR · ln 2 T1 V1 Ein Beispiel für einen irreversiblen Prozess ist die isotherme Expansion T2 = T1 des idealen Gases. Abbildung 20: Ein ideales Gas befindet sich zu Anfang ganz auf der linken Seite des Behälters. Nach Entfernen der Wand strömt das Gas in den ganzen Behälter. Die Entropieänderung ist somit ∆S = νR · ln V2 >0 V1 10.2 2. Hauptsatz der Thermodynamik Der zweite Hauptsatz der Thermodynamik besagt, dass thermische Energie nicht in beliebigem Maße in andere Energiearten umwandelbar ist. Eine alternative Formulierung ist, dass die Entropie, also die Unordnung in abgeschlossenen Systemen bei irreversiblen Prozessen immer zunimmt. Bei reversiblen Prozessen gilt ∆S = 0. 11 Kreisprozesse Wärmekraftmaschinen sind zyklisch laufende Maschinen, die mechanische Arbeit in Wärme umwandeln und umgekehrt. Sie werden durch geschlossene Kurven im p-V-Diagramm beschrieben. Diese Kurven werden auch als Kreisprozesse bezeichnet. Zur vereinfachten physikalischen Beschreibung werden diese Kreisprozesse schrittweise in Zustandsänderungen zerlegt. Abbildung 21: a) Wirkprinzip einer Wärmekraftmaschine bzw. Verbrennungsmotor b) Wirkprinzip einer Kältemaschine bzw. Wärmepumpe Die Umlaufrichtung des Kreisprozesses ist hier von entscheidender Bedeutung! Die Vorzeichen von Arbeit und Wärme wechseln bei Umkehr der Umlaufrichtung des Kreisprozesses. Das heißt, dass ein Kreisprozess je nach Umlaufrichtung einen Verbrennungsmotor bzw. Wärmekraftmaschine oder eine Kältemaschine bzw. Wärmepumpe beschreibt. Eine Wärmekraftmaschine ist ein offenes thermodynamisches System, das kontinuierlich Wärme und Arbeit mit seiner Umgebung austauscht. 11.1 Carnotscher Kreisprozess Ein Kreisprozess nach Carnot ist aus zwei Isothermen und zwei Adiabaten aufgebaut und stellt, wenn er im Uhrzeigersinn durchlaufen wird, eine idealisierte Wattsche Dampfmaschine dar. Die einzelnen Schritte des Carnot-Zyklus sind wie folgt: • 1 → 2: isotherme Expansion, Arbeit wird abgegeben, T = const. Wärme muss zugeführt werden V2 W12 = −νRT · ln <0 V1 V2 Q12 = νRT · ln >0 V1 • 2 → 3: adiabatische Expansion, Arbeit wird abgegeben, kein Wärmeaustausch, Temperatur sinkt W23 = −CV · ( T2 − T1 ) < 0 Q23 = 0 • 3 → 4: isotherme Kompression, Arbeit wird zugeführt, T = const, Wärme muss abgegeben werden W34 = −νRT · ln Q34 = νRT · ln V4 >0 V3 V4 <0 V3 • 4 → 1: adiabatische Kompression, Arbeit wird zugeführt, kein Wärmeaustausch, Temperatur sinkt W23 = CV · ( T2 − T1 ) > 0 Q23 = 0 Durch einsetzen in die Adiabatengleichung erhält man das Verhältnis der Volumina. V V1 = 4 V2 V3 Als Gesamtarbeit in einem Umlauf des Carnot-Zyklus folgt dann: ∆W = W12 + W23 + W34 + W41 V V = −νRT1 · ln 2 − CV · ( T1 − T2 ) + νRT2 · ln 2 + CV · ( T1 − T2 ) V1 V1 V2 = νR ( T1 − T2 ) · ln < 0 V1 Die Gesamtarbeit pro Umlauf ist kleiner als null, d.h. das System verrichtet in jedem Umlauf Arbeit an seiner Umgebung. In gleicher Weise kann die Nettowärme in einem Umlauf des Carnot-Zyklus berechnet werden: ∆Q = Q12 + Q23 + Q34 + Q41 V V = νRT2 · ln 2 − νRT1 · ln 2 V1 V1 V2 = νR ( T2 − T1 ) · ln > 0 V1 Die Gesamtwärme pro Umlauf ist größe als null, d.h. dem System wird Wärme in jedem Umlauf zugeführt. Die Summe von Gesamtwärme und Gesamtarbeit ist null. Das System ist wieder im Ausgangszustand. 11.2 Wirkungsgrad Der Wirkungsgrad einer Wärmekraftmaschine berechnet sich allgemein über den Quotienten aus der von der Maschine geleisteten Arbeit |∆W | und der zugeführten Wärme Q12 aus dem heißen Wärmereservoir zu (19) η= |∆W | < 1. Qzu Für den Carnot-Zyklus lässt sich diese Formel umformen zu (20) ηC = |∆W | T − T1 = 2 < 1. Qzu T2 Nur ein Teil der Wärme von Reservoir T2 kann in mechanische Arbeit umgesetzt werden. Der Rest erwärmt Reservoir T1 . Der Carnot-Wirkungsgrad ist der höchste theoretisch mögliche Wirkungsgrad einer Wärmekraftmaschine. 12 Reales Gas Das reale Gas ist ein erweitertes Modell, das die Eigenschaften von Gasen bei hohen Drücken und niedrigen Temperaturen besser beschreibt als das ideale Gasmodell. Dies geschieht durch die Korrektur zweier Annahmen des idealen Gasmodells. • Die Moleküle haben eine endliche Ausdehnung. Das Volumen muss um das Eigenvolumen der Moleküle korrigiert werden Vreal = Videal + νb, wobei b das Eigenvolumen von 1 Mol des Gases ist. • Es gibt Anziehungskräfte zwischen den Molekülen. Zumeist ist dies die sogenannte vander-Waals Kraft. Diese Anziehungskräfte heben sich im Gas auf. Am Rand des Gases jedoch existiert eine nach innen gerichtete Kraft vergleichbar mit der Oberflächenspannung von Flüssigkeiten. Diese Kraft reduziert den Druck gemäß preal = pideal − a · ( ν 2 ) , V wobei a · (ν/V )2 als Binnendruck des realen Gases bezeichnet wird. Die Konstanten a, b sind nur von der Gasart abhängig und können aus den mikroskopischen Eigenschaften der Wechselwirkung, genauer gesagt dem Potential der anziehenden und abstoßenden Kräfte, hergeleitet werden. Für die Gasgleichung des realen Gases folgt nun ν2 p + a · 2 · (V − νb) = νRT. V