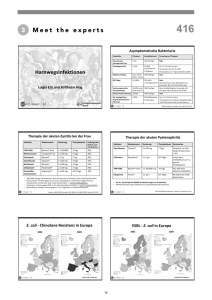
Problemkeime und rationale Antibiotika
Werbung

Problemkeime und rationale Antibiotikatherapie in der Nierentransplantation Priv. Doz. Dr. Reinhard Hoffmann Institut für Labormedizin und Mikrobiologie Infektionen nach Transplantation: Zeitverlauf Fishman, NEJM 2007, 357: 2601 Infektionen nach Organtransplantation 16 Infektionen/1000 Tage 14 12 Niere+Pankreas Lunge Leber Herz Niere 10 8 6 4 2 0 1. Monat San Juan, Am J Transplant 2007, 7: 964 2.-6. Monat >6. Monat Infektionen im ersten Jahr nach NTx (137/192 Pat, 71%) Maraha, Clin Microbiol Infect 2001, 7: 619 Spätinfektionen nach Nieren-Tx 0,07 Episoden/1000 Tage 0,06 0,05 0,04 0,03 0,02 0,01 0 San Juan, Am J Transplant 2007, 7: 964 Epidemiologie von HWI post-NTx % (7,3%, 0,45 Episoden /1000 Transplant-Tage) 90 80 70 60 50 40 30 20 10 0 Vidal, Transplant Infect Dis 2012, 14: 595 Anzahl Pat. Einfluß von HWI auf Überleben 16 14 12 10 8 6 4 2 0 ohne HWI mit HWI Todesursache Chuang, Clin Transplant 2005, 19: 230 OR for death: 3,5 (95%CI: 1,68-7,23) Post-NTx HWI als Risikofaktor? Kamath Transplant Infect Dis 29006, 8: 140 Isolierte Erreger von HWI post Nieren-Tx E. faecalis; 4% C. krusei; 2% BK Virus; 2% KNS; 4% M. morganii; 4% K. pneumoniae; 5% P. aeruginosa; 10% E. coli; 54% E. coli ESBL; 17% Valera, Transplant Proc 2006, 38: 2414 Entstehung klinischer Antibiotikaresistenzen Molton, CID 2013, 56: 1310 Resistente Erreger auf deutschen ITS 30 % der Isolate 25 20 MRSA 15 E. coli, Cipro - R E. coli, ESBL K. pneumoniae, ESBL 10 5 0 Meyer, Crit Care 2010,14: R113; NRZ Surveillance nosokomialer Infektionen E. faecium VRE Antibiotika-Verbrauch auf deutschen ITS 220 DDD/1000 Pat.-Tage 200 180 160 140 120 100 80 60 Meyer, Crit Care 2010,14: R113; NRZ Surveillance nosokomialer Infektionen Chinolone Gruppe 3/4 Cephalosporine Carbapeneme Induktion von Antibiotikaresistenzen bei gram-negativen Erregern Harbarth, CID 2001, 33:1462 Erhöhung der MRSA-Inzidenz pro 1 DDD/100 Pat-Tage MRSA-Inzidenz und Antibiotikaverbrauch 0,03 0,025 0,02 0,015 0,01 0,005 0 1 Monat 2 Monate 3 Monate 4 Monate Zeitraum Chinolone Nach Aldeyab, JAC 2008, 62:593 Amox. /Clavulansre. Gr. 3 Cephalosporine Makrolide Erhöhung der VRE-Inzidenz pro 1 DDD/100 Pat-Tage VRE-Inzidenz und Antibiotikaverbrauch 0,025 0,02 0,015 0,01 0,005 0 -0,005 -0,01 1 Monat 2 Monate 3 Monate Zeitraum Glycopeptide Gr. 3/4 Cephalosporine Nach Kritsotakis, Clin Microbiol Infect 2008, 14:747 Chinolone Penicilline+BLI Induktion von AB-Resistenzen durch Therapie von HWI in der Praxis 6 5 OR (95%KI) 4 3 2 1 0 1 Monat Costelloe 2010, BMJ 340: c2096 3 Monate 6 Monate 12 Monate Risikofaktoren für Besiedlung mit resistenten gramnegativen Stäbchen nach NTx 7 6 Adj. OR 5 4 3 2 1 0 Nieren-Pankreas TX vorangegengene ABTherapie Linares, Am J Transplant 2008, 8: 1000 Dialyse post-NTx Ureterobstruktion post Tx BreitspektrumCephalosporin Ceftazidim Cefuroxim BasisCephalosporin Ceftriaxon Cefazolin Gram-positiv Gram-negativ Cephalosporine und ESBL Cephalosporine mit erweitertem Spektrum Extended Spectrum Cephalosporins Spaltung durch Extended beta-Lactamasen = ESBL Spectrum Multiresistenz bei ESBL-Bildnern EARSS 2010 Ein typisches Resistenzplasmid Périchon Antimicrob Agents Chemother 52 (2008): 2581 Resistenzgene auf pIB1206 Tetracycline Chloramphenicol Sulfonamide Aminoglycoside Timethoprim Beta-Lactame Chinolone Therapie: zuverlässig nur mit Carbapenemen möglich Imipenem, Meropenem, Doripenem, Ertapenem Périchon Antimicrob Agents Chemother 52 (2008): 2581 Die Bedrohung – Carbapenemasen 2008 2009 2010 2011 Spalten Carbapeneme – Imipenem, Meropenem, Ertapenem Aztreonam kann teilweise noch wirken, Polymyxine als Alternative Oftmals Multi- oder „Panresistenzen“ EARSS 2008-2011 Ausbreitung der Imipenem-Resistenz bei K. pneumoniae in Griechenland Eurosurveillance 2008, 13 (4) Verbreitung von NDM-1 Molton, CID 2013, 56: 1310 Neue Antibiotika gegen multiresistente gram-negative Erreger 0 Prävention von Antibiotika-Resistenzen Resistenz ≠ Virulenz! Beispiel: S. aureus CAP Sicot, Clin Microbiol Infect 2013 (19): E142 Infektion vs. Kolonisation – z.B. VAP • • Verdacht bei: – Neuem oder progressiven Lungeninfiltrat plus – mind. einem klinischen Symptom: Fieber, Leukozytose, eitriges Trachealsekret Clinical Pulmonary Infection Score: • CPIS ≥ 6 und PCT ≥ 2,99 ng/ml 67% Sensitivität, 100% Spezifität Luna, Crit Care Med 2003 (31): 676, Ramirez, Eur Resp J 2007 (31): 356 Mortalität bei hämodynamisch stabilen Patienten 100 Mortalität 80 60 40 20 0 agressiv Hranjec et al., Lancet Infect Dis 2012 (12):774 konservativ Antibiotikagabe und Überleben im septischen Schock Kumar et al., Crit Care Med 2006 (34): 1589 Überleben in Abhängigkeit von adäquater Therapie Valles, Chest 2003 (123): 1615 Auswahl eines geeigneten Antibiotikums – z. B. HWILeitlinie Cephalosporine! Chinolone! Rationaler Antibiotika-Einsatz: Die Tarragona-Strategie Hit hard, hit early: Frühestmöglicher Einsatz einer hohen Dosis eines breit wirksamen Antibiotikums Get to the point: Ausreichende Gewebespiegel müssen erreicht werden Look at your patient: Einbeziehung der Vortherapien und Begleiterkrankungen in die Wahl der initialen antibiotischen Therapie Listen to your hospital: Einbeziehung lokaler Epidemiologie und Resistenzsituation Focus, Focus, Focus: Re-Evaluation und Fokussierung nach 72 Stunden, frühestmögliches Absetzen der Antibiose Sandiumenge, Intens Care Med 2003 (29): 876 Prävention von Antibiotika-Resistenzen Restriktiver Einsatz von Antibiotika Möglichst kein kalkulierter Einsatz von oralen DrittgenerationsCephalosporinen oder Chinolonen in der hausärztlichen Praxis Antibiotika nur bei nachgewiesener bakterieller Infektion Keine Therapie einer Besiedlung ohne Infektion Beispiel: E. coli im Trachealsekret bei beatmeten Patienten Keine Therapie von Kulturkontaminationen Beispiel: Staphylokokkus epidermidis in 1 von 3 Blutkulturen Fokussierung der Antibiose nach Vorliegen der mikrobiologischen Befunde Rechtzeitiges Beenden der antibiotischen Therapie http://www.cdc.gov/drugresistance/healthcare/default.htm, Sandiumenge, Intens Care Med 2003 (29): 876 Effekt der Reduktion des AB-Verbrauches Makrolid/ S. pyogenes Global/ S. pneumoniae Enne, J. Antimicrob. Chemother. 2010;65:179-182 Trimethoprim/ E. coli Sulfonamid/ E. coli Chinolon/ E. coli Hygienemaßnahmen Besiedelung häufig gastrointestinal, Atemwege Kein längeres Überleben auf trockenen Oberflächen von ESBL A. baumannii, S. aureus sehr umweltresistent Hände des medizinischen Personals sind wichtigster Vektor BASISHYGIENE HÄNDEDESINFEKTION Abhängig von lokalen Gegebenheiten: Einzelzimmerisolation; Kittelpflege Mund-Nasen-Schutz Regelmäßige Desinfektion patientennaher Flächen Grundreinigung des gesamten Zimmers bei A. baumannii! Keine Sanierung möglich Patient behält ESBL-Status für den gesamten Aufenthalt und darüber hinaus (6-9 Monate) Bedeutung der zeitnahen effektiven Antibiose im septischen Schock Kumar al., Crit Care Med 2006 (34): 1589 Permafrostboden am Yukon D‘Costa Nature 2011, 477: 457 Isolation funktioneller vanA-Gene D‘Costa Nature 2011, 477: 457 Angaiza – eine extrem isolierte humane Population 2 Stunden 7 Stunden 4 Stunden Pallecchi, PLOS Negl Trop Dis 2012, 6: e1790 Antibiotikaresistenzen in Angaiza, Peru 100 % Pers. mit res. Isolaten 90 80 70 60 50 40 30 20 10 0 Pallecchi, PLOS Negl Trop Dis 2012, 6: e1790 2002 2002 2009 Multiresistenzen bei CipR E. coli-Isolaten aus Angaiza (n=28) 6 5 4 3 2 1 0 Pallecchi, PLOS Negl Trop Dis 2012, 6: e1790 Pneumocystis jirovecii-Pneumonie nach NTx Goto Transplant Infect Dis 2011, 13:551 Übertragung von P. jirovecii von Mensch zu Mensch Le Gal, CID 2012, 54: e62 Altersabhängigkeit von Infektionen 35 30 CMV unklar VZV Sepsis Pneumonie Pyelonephritis Cellulitis 25 20 15 10 5 0 <17 Dharmidharka, Transplantation 2006, 81: 1662 18-50 >51 Faktoren, die das Infektionsrisiko beeinflussen Parasuraman, Transpl Rev 2010, 24: 43 Erreger später Infektionen nach Nieren-Tx 25 % aller Erreger 20 15 10 5 0 San Juan, Am J Transplant 2007, 7: 964 Interaktionen zwischen Antibiotika und Immunsuppressiva Parasuraman Transplant Rev 2010, 24: 43