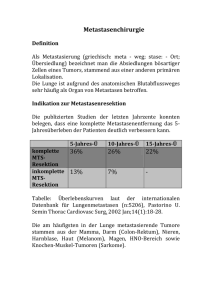
Präsentation - GI
Werbung
Aktuelle chirurgische Therapie hepatobiliärer Tumore (und Metastasen) Hans J. Schlitt Klinik und Poliklinik für Chirurgie Universitätsklinikum Regensburg Aktuelle chirurgische Therapie hepatobiliärer Tumore (und Metastasen) Hepatozelluläres Karzinom (HCC) - Prätherapeutische / periinterventionelle Diagnostik - Ablation vs. Resektion - Resektion vs. Transplantation - „Downstaging“ vor Transplantation Gallengangskarzinom (GG-Ca.) - Hiläres GG-Ca. (Klatskin-Tumor) Verbesserte Resektabilität von Lebertumoren - 2-zeitige Resektion mit PV-Ligatur und „in-situ-split“ Behandlungsstrategien HCC nach BCLC Stadium 0 Stadien A - C PS 0-2, Child-Pugh A-B PS 0, Child-Pugh A Sehr frühes Stadium (0) Singuläre RF Frühes Stadium (A) Intermediäres Stadium (B) Milan Kriterien, PS 0 UCSF, Multilokulär, PS 0 Singulär Portal invasion, N1, M1, PS 1-2 Milan Kriterien Portalinvasion, N1, M1 Portal-Druck/ Bilirubin Begleiterkrankungen erhöht Normal Fortgeschritten (C) Nein Nein Ja Ja +/Resektion Transplantation RFA Kurative Ansätze (30%) 5-Jahres-Überleben: 50% - 80% TACE Sorafenib Nicht-kurativ (70%) 3-Jahres-ÜL :40%- 50% vs. 10% Modifiziert nach Barcelona Clinic Liver Cancer Group (BCLC) Behandlungsstrategien HCC nach BCLC Stadium 0 Stadien A - C PS 0-2, Child-Pugh A-B PS 0, Child-Pugh A Sehr frühes Stadium (0) Singuläre RF Frühes Stadium (A) Intermediäres Stadium (B) Milan Kriterien, PS 0 UCSF, Multilokulär, PS 0 Singulär Portal invasion, N1, M1, PS 1-2 Milan Kriterien Portalinvasion, N1, M1 Portal-Druck/ Bilirubin Begleiterkrankungen erhöht Normal Fortgeschritten (C) Nein Nein Ja Ja +/Resektion Transplantation RFA Kurative Ansätze (30%) 5-Jahres-Überleben: 50% - 80% TACE Sorafenib Nicht-kurativ (70%) 3-Jahres-ÜL :40%- 50% vs. 10% Modifiziert nach Barcelona Clinic Liver Cancer Group (BCLC) KM-Sonografie (CEUS) als wichtiges tool zur Diagnostik und Therapiedurchführung - Präoperative Differentialdiagnostik von Leber-Läsionen - Intraoperative Detektion von HCCs - Periinterventionelle Diagnostik bei RFA und Embolisation Wiggermann P et al, Clin Hemorheol Microcirc 2011 Loss M et al, Clin Hemorheol Microcirc 2012 FDG-PET zur Prognoseabschätzung beim HCC von Transplantation (und Resektion) Kornberg A et al, Liver Transplant 2012 FDG-PET zur Prognoseabschätzung beim HCC von Transplantation (und Resektion) V.a. bei grenzwertiger Indikationsstellung zur LTx: FDG-PET als wichtiges Prognosekriterium (PET-positiv = schlechte Prognose) Kornberg A et al, Liver Transplantation 2012 Tumor-“Downstaging“ vor Transplantation: Erfolgreiches downstaging prognostisch günstig Metaanalyse: 8 Studien, 720 Patienten erfolgreiches „downstaging“ in 24-69 % der Patienten erreicht Gordon-Weeks AN et al, Br J Surg 2011 Tumor-“Downstaging“ vor Transplantation: AFP-Verlauf wichtiger als Initialwert (basierend auf US-Registry-Daten (SRTR)) Merano S et al, J Hepatol 2011 Resektion vs. Ablation beim HCC ? solitäres HCC 5 cm, med. Follow-up: 28 Mo.; prospektiver RCT n=180 (90 vs. 90) Resektion Resektion Rezidiv-freies Ü. Rezidiv-freies Ü. Ablation Rezidiv-freies Ü. Ablation Rezidiv-freies Ü. Resektion Gesamt-Ü. Ablation Gesamt-Ü. Jahre Chen MS et al, Ann Surg 2006 Resektion vs. Ablation beim HCC ? - prospektiv randomisiert - innerhalb Milan-Krit. - 2 x 115 Patienten Huang J et al, Ann Surg, Dez 2010 Resektion vs. Ablation beim HCC ? Huang J et al, Ann Surg, Dez 2010 Resektion vs. Ablation beim HCC ? Frage „Resektion vs. Ablation“ beim HCC weiterhin offen: offensichtlich sehr Zentrums-abhängig (!) Huang J et al, Ann Surg, Dez 2010 Resektion vs. Ablation mit kurativem Ansatz Resektabel Abladierbar Optimal Resectable individualisierte Behandlung Ablatable im “Graubereich” hängt von vielen Faktoren ab, u.a. auch von Erfahrung und Geschick des Interventionalisten bzw des Chirurgen Resektion vs. Transplantation beim HCC (innerhalb Milan-Kriterien) - nicht randomisiert, aber vergleichbares Tu-Stadium - Resektion: 40 LTx: 215 Gelistet/nicht-LTx: 33 Koniaris LG et al, Ann Surg 2011 Resektion vs. Transplantation beim HCC (innerhalb Milan-Kriterien) - insgesamt: 363 Patienten - Resektion: 106 LTx: 270 Koniaris LG et al, Ann Surg 2011 Resektion vs. Transplantation beim HCC (innerhalb Milan-Kriterien) - nicht randomisiert - Resektion: 287 LD-LTx: 50 Fan ST et al, Br J Surg 2011 Resektion vs. Transplantation beim HCC (innerhalb Milan-Kriterien) - nicht randomisiert - Resektion: 287 LD-LTx: 50 Bei resektablem Tumor (ausreichender Leberfunktion, nicht zu starke port. Hypertension !) ist die Resektion der primären LTx vorzuziehen Fan ST et al, Br J Surg 2011 „Gallenwegs-Karzinom“: ein sehr heterogenes Krankheitsbild Intrahepatisches Gallenwegs-Karzinom („cholangiozelluläres Karzinom“, CCC) Gallenblasen-Karzinom Hepatikusgabel-Karzinom („Klatskin-Tumor“) Karzinom des mittleren Gallengangs (Lig. hepatoduodenale) Distales Gallengangs-Karzinom (Pankreaskopf-Tumor) „Gallenwegs-Karzinom“: ein sehr heterogenes Krankheitsbild Intrahepatisches Gallenwegs-Karzinom („cholangiozelluläres Karzinom“, CCC) Gallenblasen-Karzinom Hepatikusgabel-Karzinom („Klatskin-Tumor“) Karzinom des mittleren Gallengangs (Lig. hepatoduodenale) Distales Gallengangs-Karzinom (Pankreaskopf-Tumor) Typischer ERCP-Befund beim Klatskin-Tumor Ursache: i.d.R. ein sehr kleiner Tumor Leber Ausgedehnte Resektion beim Klatskin-Tumor z.B. erweiterte Hemihepatektomie rechts incl. Segm. I + Hepatikusgabel (oft + PV-Gabel) + Lymphadenektomie Ausgedehnte Resektion beim Klatskin-Tumor z.B. erweiterte Hemihep. links incl. Segm. I + Hepatikusgabel (+ PV-Gabel) (ggf. + Arteriensegment !) + Lymphadenektomie Natsume S et al, Ann Surg 2012 Klatskin-Tumor: Präop. Diagnostik 3-Phasen-CT NMR / MRCP oft nur indirekte Tumorzeichen idealerweise keine Endoskopie / ERCP (!!!) wenn möglich: PTCD im vermutlich zu erhaltenden Leberlappen (und nur da !) evtl. Laparoskopie zum Ausschluß Peritoneal-Ca. oft präop. kein definitiver Tumornachweis Resektabilitäts-Beurteilung meist erst intraop. möglich Klatskin-Tumor: Präop. Diagnostik 3-Phasen-CT NMR / MRCP oft nur indirekte Tumorzeichen idealerweise keine Endoskopie / ERCP (!!!) wenn möglich: PTCD im vermutlich zu erhaltenden Leberlappen (und nur da !) evtl. Laparoskopie zum Ausschluß Peritoneal-Ca. oft präop. kein definitiver Tumornachweis Resektabilitäts-Beurteilung meist erst intraop. möglich Strategiebesprechung mit erfahrenem Chirurgen vor jeglicher Intervention Klatskin-Tumor: Erw. Hemihepatektomie re., Hepatikusgabel- und PfortadergabelResektion sowie Lymphadenektomie (en-bloc !!!) Klatskin-Tumor Ergebnisse nach Resektion Periop. Mortaliät: 5-JÜR: Tumorrezidivrate 5 (– 10) % 25 (– 50) % z.T. nur 40 % Mortalität und Morbidität sinken und R0-Resektionsraten steigen mit zunehmender Erfahrung !!! Natsume S et al, Ann Surg 2012 Cannon RM et al, HPB 2012 Therapie von Klatskin-Tumoren: Fazit Bei Verdacht sofort Vorstellung in erfahrenem Zentrum Primär nur CT- oder NMR-Diagnostik (keine ERCP!) Gemeinsame Therapieplanung Gastroenterologie / Viszeralchirurgie / Radiologie Individualisierte Therapiestrategie festlegen Operation durch Klatskin-erfahrenen Operateur Erhöhung der „Resektabilität“ von Lebertumoren (und –metastasen) Tumorverkleinerung durch Vorbehandlung (neoadj. Chemotherapie) Vergrößerung der Leberfunktionsreserve z.B. PV-Embolisation oder „in-situ-split“ Kombinierte oder sequentielle Verfahren (zweizeitige Resektion, Resektion + RFA) umfangreiche Leberchirurgie-Erfahrung von Chirurg und Zentrum Problematik Befund: z.B. multiple Lebertumore und tumorfreier Leberteil, der (für ausreichende Funktion) zu klein ist Technische Resektabilität ABER Funktionelle Irresektabilität „In-situ Split“ (1. Schritt) 1. Operation: Durchtrennung des Lebergewebes und Durchtrennung der rechten Pfortader (und ggf. der mittleren Lebervene), Entfernung von Tumoren im Leberteil, der erhalten werden soll Schnitzbauer AA, Lang SA et al, Ann Surg 2012 „In-situ Split“ (2. Schritt) Beginn der 2. Operation (nach ca. 1 Woche): Tumortragender Leberteil ist kleiner geworden, tumorfreier Leberteil ist deutlich gewachsen: Tumortragender Leberteil wird nun entfernt Schnitzbauer AA, Lang SA et al, Ann Surg 2012 „In-situ Split“ (2. Schritt) Ende der 2. Operation: tumorfreier (und jetzt ausreichend großer) Leberteil bleibt übrig Patient ist jetzt tumorfrei Schnitzbauer AA, Lang SA et al, Ann Surg 2012 „In-situ-Split“ + PV-Ligatur rechts Situs am Ende der 1. Operation Komplette Devaskularisation Segm. IV Rasche Volumenzunahme des li.-lat. Leberlappens nach „in-situ split“ 1000 Mittl. Vol.Zunahme: 900 800 74 % Volumen (ml) 700 600 500 400 nach median 300 9 Tagen 200 100 0 vor 1. Op. vor 2. Op. Schnitzbauer AA, Lang SA et al, Ann Surg 2012 Ist Chirurgie bei grenzwertig resektablen Lebermetastasen wirklich sinnvoll ? Chirurgie: - 65 Patienten - multiple Lebermetastasen - neoadj. Chemotherapie - dann: 2-zeitige Resektion Vergleichsgruppe: - 62 Patienten - vergleichbare Metastasen - Chemotherapie-Responder - keine Resektion Brouquet A et al, J Clin Oncol 2011 Chirurgie ist auch bei grenzwertig resektablen Lebermetastasen sinnvoll ! Brouquet A et al, J Clin Oncol 2011 Für bestmögliche Patientenversorgung: Optimal abgestimmte Kooperation von internistischem, chirurgischem (und radiologischen) Onkologen notwendig „Hohe Lokalrezidivrate und kürzere Zeit-zum-Progress bei primärer Ablation (resektabler Metastasen)“ Lokalrezidivrate Zeit-zum-Progress Otto G et al, Ann Surg 2010 „ Hohe Lokalrezidivrate und kürzere Zeit-zum-Progress, aber gleiches Gesamtüberleben bei primärer Ablation “ Sekundäre Interventionen Gesamtüberleben Otto G et al, Ann Surg 2010