45 4.1.1 Isoelektrischer Punkt - Medi
Werbung

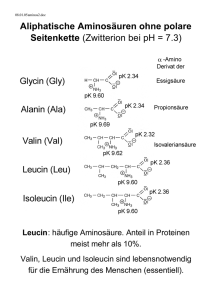
4.1.1 Isoelektrischer Punkt Übrigens ... Um ein Gemisch aus Aminosäuren zu trennen, kann man die Dünnschichtchromatographie verwenden. Hierbei laufen die Aminosäuren bei der Elektrophorese abhängig von ihrer Masse und ihrer Ladung unterschiedlich weit. Häufig wird nach der Verbindung Cystin gefragt: Cystin entsteht bei der Reaktion von zwei Molekülen Cystein durch Ausbildung einer Disulfidbrücke. Dabei werden 2H abgespalten, es ist also eine Dehydrierung (s. Hydratisierung/­ Dehydratisierung, Hydrierung/Dehydrierung, S. 7 ff) und KEINE Dehydratisierung. Cystin enthält KEINE Peptidbindung (s. 4.1.4, S. 47). COO– H 3N + C H COO– H 3N + CH2 C H CH2 S S Disulfidbrücke medi-learn.de/6-ch2-98­ Abb. 98: Cystin 4.1.1 Isoelektrischer Punkt Weil Aminosäuren sowohl eine saure Carboxylgruppe als auch eine basische Aminogruppe haben sind sie amphoter, d. h. sie reagieren sowohl sauer als auch basisch, je nach Umgebungsmilieu. Die Carboxylgruppe gibt in wässriger Lösung ein Proton ab, die Aminogruppe nimmt eines auf. O O C H 2N C – C H H 3N + R C H R Zwitterion oder: COO– COOH H 2N O O H C H R Abb. 99: Zwitterion www.medi-learn.de H 3N + C H R medi-learn.de/6-ch2-99­ So entsteht ein Zwitterion, das mit der ungeladenen Form im Gleichgewicht steht. Abhängig vom pH-Wert des umgebenden Mili­ eus kann auch nur eine der beiden funktionellen Gruppen dissoziiert/assoziiert vorliegen: –– Im sauren Milieu nimmt nur die Aminogruppe ein Proton auf, die Carboxylgruppe kann ihres aber nicht abgeben. Folglich ist die Aminosäure positiv geladen. –– Im alkalischen Milieu verhält es sich genau umgekehrt. Die Carboxylgruppe gibt ihr Proton ab und die Aminosäure ist negativ geladen. Der pH-Wert, bei dem die Nettoladung null ist (also entweder die ungeladene Form oder das Zwitterion vorliegt), heißt isoelektrischer Punkt. Er ist für jede Aminosäure eine charakteristische Konstante. Berechnet wird der isoelektrische Punkt aus dem arithmetischen Mittel der pKS-Werte der funktionellen Gruppen: pKS1 + pKS2 2 Bei den neutralen AS ergeben sich daraus für den isoelektrischen Punkt Werte zwischen pH5 und 6,5. Die sauren und die basischen Aminosäuren haben eine zusätzliche Carboxyl-/Aminogruppe, die berücksichtigt werden muss: Der isoelektrische Punkt einer sauren AS errechnet sich als arithmetisches Mittel der pKs-Werte der beiden Säuregruppen (niedrige pKs-Werte), der einer basischen AS als arithmetisches Mittel der pKs-Werte der beiden basischen Gruppen (hohe pKs-Werte). So erklärt sich, dass der isoelektrische Punkt bei den sauren AS Glutaminsäure und Asparaginsäure im sauren Bereich, bei den basischen AS Arginin, Lysin und Histidin im alkalischen Bereich liegt. Die Polarität (also die positiven bzw. negativen Ladungen) der basischen und sauren AS im neutralen pH Bereich sorgen übrigens dafür, dass sie sich hydrophil verhalten und im elektrischen Feld wandern: bei pH 7 –– sind die basischen AS positiv geladen und wandern daher zur negativen Elektrode (Kathode). 4 45