Kein Folientitel
Werbung

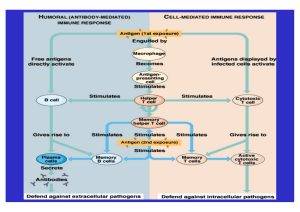
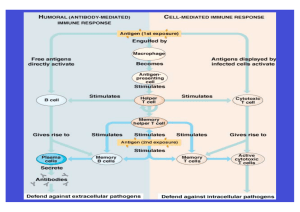
Allgemeine Virologie – SS 2016 Zytokine und Chemotherapie Mi 15.06.16 PD Dr. Stefan Finke Friedrich-Loeffler-Institut, Greifswald - Insel Riems [email protected] Zytokine • Proteine die der zellulären Kommunikation dienen • von Zellen produziert • binden an Rezeptoren • wirken teils als Wachstumsfaktoren • Antwort auf Reiz (auch mikrobiellen Reiz) • regulierbar • Zytokine im Blut sind eines der ersten Anzeichen einer Infektion Zytokine pro-inflammatorische Zytokine (z.B.: IL-1, TNF, IL-6, IL-12) aktivieren Leukozyten anti-inflammatorische Zytokine (z.B: IL-10, IL-4, Tgf-ß) inhibieren Aktivität von pro-inflammatorischen Zytokinen Chemokine (z.B: IL-8) Rekrutieren Immunzellen während der frühen Phase der Infektion Wachstumsfaktoren Zytokine partizipieren in nahezu jeder Phase der Wirtsantwort auf eine virale Infektion Induktion eines antiviralen Status Kontrolle der Inflammation Regulation der adaptiven Immunantwort Regulation der Kommunikation zwischen angeborener und adaptiver Immunität Muster einer typischen Zytokinreaktion auf eine Virusinfektion 1. Produktion von Zytokinen durch infizierte Zelle 2. Bindung der Zytokine an Rezeptoren auf „sentinal“ Dendritische Zellen, Makrophagen und benachbarten nicht infizierten Zellen 3. Massive Zytokinsynthese durch Dendritische Zellen, Makrophagen und benachbarten nicht infizierten Zellen Amplifizierung der initialen „response“ Zytokine, die in hohen Konzentrationen auftreten: erst: IFN-a und IFN-ß (Typ-I Interferone) dann: Tumornekrosefaktor a (Tnf-a), Interleukine 6 und 12 (IL-6, -12) und IFN-g (Typ-II Interferon) Typ I – Interferone: Induktion und IFN-stimulierte Genexpression aus Haller et al., Virology 2006 PKR: dsRNA-abhängige Proteinkinase; TRAF: TNF-Rezeptor assoziierter Faktor; IKKa/ß: Kinase; NF-kB: Transkriptionsfaktor RIG-I/MDA-5: intrazelluläre RNA-Helicasen; IPS: IFN-ß-Promotor Stimulator 1; MAVS: Mitochondrial antiviral signaling; TBK-1/ IKKe: IRF-3 phosphorylierende Kinasen; IRF-3: IFN-regulatorischer Faktor (Transkritpionsfaktor) JAK: Janus-Kinase; TYK: Tyrosin-Kinase; STAT: signal transducer and activator of transcription ISGF: IFN-stimulierter Genfaktor; ISRE: IFN-stimulated response element Jak: Janus Kinase Tyk: Tyrosine Kinase STAT: signal transducer and activator of transcription IRF9: Interferon Response Factor 9 GAS: Gamma Activated Sites ISRE: Interferon Stimulated ResponseElements Toll Like Rezeptoren Sandra N. Lester , Kui Li Toll-Like Receptors in Antiviral Innate Immunity Journal of Molecular Biology, Volume 426, Issue 6, 2014, 1246 - 1264 http://dx.doi.org/10.1016/j.jmb.2013.11.024 Fig. 1 Recognition of viral PAMPs such as viral proteins, dsRNA, ssRNA, and CpG DNA, initiates an antiviral innate immune response mediated by TLRs. TLR2 and TLR4 are present on the cell surface and recognize viral proteins. TLR3, TLR7, TLR8, and TLR9 are ... Erkennung von pathogenspezifischen Strukturen (z.B. ssRNA, dsRNA, CpG-reiche DNA) z.B.: intrazelluläre Rezeptoren für dsRNA: RIG-I; PKR oder Oberflächenrezeptoren: Toll like Rezeptoren Induktion der IFN b Gentranskription Sekretion von IFN b Bindung an IFN a Rezeptor auf der Zelloberfläche (Bindung von IFN a und IFN b) Signaltransduktionskaskade Transkription von ISGs (Interferon Stimulierte Gene) Interferon induzierte Effekte erfolgen meist durch die Inhibition zellulärer Aktiviäten Interferon induzierte Effekte erfolgen meist durch die Inhibition zellulärer Aktiviäten Viren interferieren mit fast allen Schritten aus Haller et al., Virology 2006 • Zytokine als Sofortreaktion auf Virusinfektion • Erkennung von „Fremdstrukturen“ (PAMPs) • TLR: 3, 7, 8 und 9: Erkennung von viralen Nukleinsäuren • Endogene dsRNA-Rezeptoren • Typ I Interferon Induktion • Kontrolle der Interferon-Antwort • Virale Antagonisten der Interferonantwort Antivirale Chemotherapie Action of antivirals: enzyme inhibition, fusion inhibition, blocking of shedding, neutralization by monoclonal antibodies Viele antivirale Substanzen sind Nukleosidanaloga z.B.: Acyclovir: HSV, VZV Gancylovir: CMV Lamivudin: HBV Ribavirin: HCV Azidothymidin (AZT): HIV Phosphorylierung von Acyclovir (Pro-Drug) zu ACV-Triphosphat durch virale und zelluläre Kinasen Prinzip der Hemmung der Herpesvirus Vermehrung 1. Prodrug – Prozessierung durch virale Proteine 2. höhere Spezifität für virale DNA-Polymerasen Acyclovir – Acycloguanosine (Valacyclovir -1-valylester von acyclovir) • Phosphorylierung durch HSV and VZV Thymidine kinase (TK) zu Monophosphat • Weitere Phosphorylierungen zu Triphosphate durch zelluläre Kinasen • Kompetition mit dGTP • Kettenabbruch bei der DNA-Synthese • Pharmakology: iv, oral; Halbwertszeit 2.5-3.5 Stunden, Ausscheidung über Niere, bei oraler Aufnahme Bioverfügbarkeit bei 10-20% (Val-ACV 60%) • Nebeneffekte: Lokale Entzündungen, Phlebitis (Entzündung venöser Gefäße), Übelkeit, Erbrechen, Diarrhoe, Übelkeit, Nierenversagen Indikation: HSV, VZV Ganciclovir – Guanosinanalog (Valganciclovir – 1-valylester von Gancyclovir) • Phosphorylierung zum Monophosphat durch CMV-Thymidinkinase (UL97) • Di- und Triphosphate durch zelluläre Kinases • Kompetitiver Inhibitor (dGTP) • Kettenabbruch, Akkumulierung von nichtinfektiösen DNA-Fragmenten im Nukleus • iv Administration, Halbwertszeit im Plasma 3h, Ausscheidung über Niere, orale Bioferfügbarkeit: 6-9% (valGCV 60%). • Indikation: CMV - Erkrankungen (Retinitis, Organtransplantationen) • Nebeneffekte: Neutropenie, Anaemie, teratogen Cidofovir – 3-hydroxy-2-phosphonymehtyloxypropyl-cytosine • • • • • Analog von Desoxycytidine-Monophosphate (keine TK Aktivität nötig) Phosphoryliert zu Triphosphate durch zelluläre Enzyme iv Administration, Halbwertszeit 2.5 h, 70% wird über Niere ausgeschieden Nebenwirkungen: Nephrotoxien aktiv gegen: CMV, HSV, Variolavirus, Vacciniavirus, HIV Foscarnet – trisodium phosphonoformate • Nichtkompetitiver Inhibitor der viralen Polymerase (Blockierung der Pyrophosphatebindestelle) • Halbwertszeit 0.3 – 6.8 h, 90% wird mit Urin ausgeschieden • Antivirale Aktiviät gegen EBV, CMV, HSV, VZV, HIV • Nebeneffekte: Nierenschäden, Anämie, Krämpfe Ribavirin – Guanosine/Inosin-Analogon • inhibiert zelluläre IMP dehydrogenase Reduktion der GTP-Level • inhibiert Translation viraler mRNAs durch Interferenz mit 5‘-Capping • inhibiert virale RNA-abhängige RNAPolymerasen • Halbwertszeit: 9.5 h, Ausscheidung über Nieren, Abbau über Leber • aktiv gegenüber RNA Viren: RSV in Kindern, mit peg-IFN bei HCV, Hanatvirus, Lassa fever virus • Nebenwirkungen: Bronchospasmen, Konjunktivitis, hämolytische Anämie, Ausschlag, Übelkeit IMP: Inosinmonophosphat Hypothetische Wirkungen von Ribavirin HIV-Therapie • Kombinationstherapie: Nukleosidische RT Inhibitoren Nichtnukleosidische RT-Inhibitoren Protease Inhibitoren Die Kombination von Substanzen gegen unterschiedliche virale Funktionen / Targets verringert die Wahrscheinlichkeit des Auftretens von Mutationen (da mehrere Mutationen gleichzeitig notwendig sind) HAART: Highly Active Antiretroviral Therapy Bei Auftreten von Resistenzen: Therapieumstellung (Austausch einzelner oder mehrer Substanzen) Gary et al., HIV infection: epidemiology, pathogenesis, treatment, and prevention The Lancet, 2014 http://dx.doi.org/10.1016/S0140-6736(14)60164-1 Azidothymidin (AZT) Phosphorylierung zum Triphosphat durch zelluläre Kinasen Inhibition of the reverse transcriptase Nature Med 2003; 9:870 Proteaseinhibitoren Virusreifung wird blockiert nicht infektiöse Virionen Novel Hepatitis C (HCV) Antivirals from Scheel and Rice, 2013, Nature Medicine from Scheel and Rice, 2013, Nature Medicine Novel Hepatitis C (HCV) Antivirals Influenzavirus Replikation Neuraminidase Inhibitoren Amantadin ( Uncoating) Oseltamivir - Tamiflu • Sialinsäure-Analog, blockiert Neuraminidase von Influenza A und B Virusfreisetzung wird blockiert! • funktioniert nur innerhalb der ersten 48 hrs nach Virusaufnahme Amantadin / Rimantadin = methyl-amantadin • Inhibition der Ionenkanalaktiviät des M2 Proteins von Influenza A Virus • keine Ansäuerung des Viruskapsids Uncoating wird blockiert • aktuell zirkulierende Viren sind Amantadin-Resistent Hepatitis B – Inhibition der HBV-Replikation • Möglichkeiten der antiviralen Therapie begrenzt, aber ansteigend • Nukelosidanaloga Kettenabbruch • Prodrug-Prinzip (ACV, GCV in der Herpesvirus-Therapie) • HIV-Therapie: HAART, Inhibition diverser Schritte im retroviralen Zyklus (Wirkmechanismen)