Druckversion
Werbung

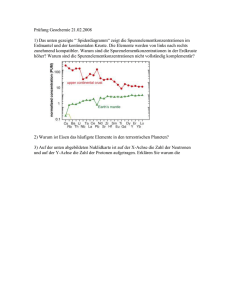
Allgemeine Chemie Der Atombau Dirk Broßke Berlin, Dezember 2005 1 1. Atombau 1.1. Der Atomare Aufbau der Materie 1.1.1. Der Elementbegriff Materie besteht aus... # 6.Jh.v.Chr. Empedokles: Erde, Wasser, Luft, Feuer # Mittelalter Alchimisten: S; Hg und Salz # 1642; 1661 Jungius und Boyle: Elemente sind Substanzen, die sich nicht in andere Stoffe zerlegen lassen. 1.1.2. Daltons Atomtheorie Chemische Elemente bestehen aus kleinsten, nicht weiter zerlegbaren Teilchen, den Atomen. Alle Atome eines Elements sind einander gleich, besitzen also gleiche Masse und gleiche Gestalt. Atome verschiedener Elemente haben unterschiedliche Eigenschaften. Jedes Element besteht also aus nur einer für das Element typischen Atomsorte Chemische Verbindungen entstehen durch chemische Reaktionen von Atomen verschiedener Elemente. Die Atome verbinden sich in einfachen Zahlenvrhältnissen, und werden durch chemische Gleichungen beschrieben. z.B.: C + O = CO C + 2O = CO2 Gesetz zur erhaltung der Masse (Lavoisier 1785). Bei allen chemischen Vorgängen bleibt die Gesamtmasse der an der Reaktion beteiligten Stoffe konstant. Gesetz der konstanten Proportionen (Proust 1799). Eine chemische Verbindung bildet sich immer aus konstanten Massenverhältnissen der Elemente. Gesetz der multiplen Proportionen (Dalton 1803). Bilden zwei Elemente mehrere Verbindungen miteinander, dann stehen die Massen desselben Elements zueinander im Verhältnis kleiner ganzer Zahlen. 2 1.2. Der Atomaufbau 1.2.1. Elementarteilchen, Atomkern, Atomhülle Atome sind aus noch kleineren Teilechen (Elementarteilchen) zusammengesetzt Elementarteilchen sind kleinste Bausteine der Materie, die nicht aus noch kleineren Einheiten zusammengesetzt sind. Sie sind aber ineinander umwandelbar, also keine Grundbausteine im Sinne unveränderlicher Teilchen. Einige hunter dieser Elementarteilchen sind gegenwertig bekannt, abber nur wenige sind sind für den Atombau von Bedeutung (Elektronen, Protonen, Neutronen). Elementarteilchen Elektron Proton Neutron Symbol e p n Masse 0,9109*10-30 kg 5,4859*10-4 u 1,6725*10-27 kg 1,007277 u 1,6748*10-27 kg 1,008665 u leicht Ladung schwehr, nahezu gleiche Masse -e +e keine Ladung negative positive neutral Elementarladung Elementarladung Elementarladung: e = 1,6022 * 10-19 C Alle auftretenden Ladungsmengen können nur ein ganzzahliges Vielfaches von e sein. Eine atomare Masseneinheit (u) ist definiert als 1/12 der Masse eines Atoms des Kohlenstoffnuklids 12C 1 u = 1,6606 * 10-27 kg Schematische Darstellung eines Atoms: Kernladungszahl = Zahl der Protonen = 4 Massenzahl = Zahl der Protonen + Neutronen = 9 Zahl der Elektronen = Zahl der Protonen = 4 3 1.2.2. Chemische Elemente, Isotope, Atommassen Die meisten Elemente bestehen nicht aus identischen Atomen, sondern aus einen Gemisch von Atomen die sich in der Zusammensetzung der Atomkerne unterscheiden. Die drei Atomarten des Wasserstoffs: Ein chemisches Element besteht aus Atomen mit gleicher Protonenzahl (Kernladungszahl), die Zahl der Neutronen kann unterschiedlich sein. gleiche Kernladungszahl = gleiche Elektronenzahl = gleiche Elektronenhülle = gleiches chemisches Verhalten Eine durch Kernladungszahl und Neutronenzahl charakterisierte Atomsorte bezeichnet man als Nuklid. Nuklide mit gleicher Protonenzahl, aber verschiedener Neutronenzahl heißen Isotope. Die meisten Elemente sind Mischelemente, das heißt sie bestehen aus mehreren Isotopen, die in unterschiedlicher häufigkeit vorkommen. Isobare sind Nuklide mit gleicher Nukleonenzahl, aber verschiedener Protonenzahl Die Atommasse eines Elementes erhält man aus den Atommassen der Isotope unter Berücksichtigung der natürlichen Isotopenhäufigkeit. Die relative Atommasse Ar eines Elementes X ist auf 1/12 der Atommasse des Nuklids 12C bezogen Ar(X) = mittlere Atommasse von X 1/ 12 (Nuklidmasse von 12C 4 1.2.3. Massendefekt, Äquivalenz von Masse und Energie Bei der Vereinigung von Neutronen und Protonen zu einem Kern wird Kernbindungsenergie frei. Der Energieabnahme des Kerns äquivalent ist eine Massenabnahme, den E = mc2. c = 2,99793 * 108 m s-1 (Lichtgeschwindigkeit) Das Gesetz besagt, dass Masse in Energie umwandelbar ist und umgegkehrt. Einer atomaren Masseneinheit entspricht die Energie von 931 * 106 eV = 931 MeV (1 u = 931 MeV ) m ( 4He ) = 2mn + 2mp - 0,03 ( 2mn + 2mp = 4,0319 u ) mn = Masse Neutron mp = Masse Proton 1.3. Kernreaktion chemische Reaktion: Veränderung der Elektronenhülle, Kern bleibt unverändert, Energieumsatz nur wenige eV => Gesetz der Erhaltung der Masse (Änderung nicht erfassbar). Kernreaktion: Veränderung der Atomkerne (Elektronenhülle spielt keine Rolle); hoher Energieumsatz => Massenänderung. 1.3.1. Radioaktivität 1896, Becquerel: Uranverbindung strahlt spontan 1888, Pierre und Marie Curie:, Endeckung des Radiums 1903, Rutherford und Soddy: Entdeckung der Radioaktivität α - Strahlen: bestehen aus 4He2+ - Kernen β - Strahlen: bestehen aus Elektronen γ - Strahlen: energiereiche, elektromagnetische Strahlung α - Zerfall (Massezahl nimmt von Glied zu Glied um vier ab) 5 β - Zerfall (Massezahl bleibt konstant) β - Zerfall : n -> p + e (Das Element mit einer um eins erhöhten Ordnungszahl entsteht) Die bei radioaktiven Umwandlungen entstehenden Elemente sind meist ebenfals radioaktiv und zerfällt weiter, so dass Zerfallsreihen entstehen. Diese wird solange fortgesetzt bis ein stabieles Nukleotid entsteht. Maß für die Stabilität eines Nuklids ist die Hablbwertzeit t ½ Es gilt dann: Halbwertzeiten liegen zwischen 10-9 und 1014 Jahren. Radioaktive Zerfallsgeschwindigkeit ist unabhängig von der Temperatur, vom Druck und von der chemischen Umgebung. Sie wird deshalb auch als geologische Uhr bezeichnet. Zerfallsreihe Nukleonenzahl Ausgangsnuklid Stabieles Endprodukt Abgegebene Teilchen α β Thoriumreihe 4n 6 4 Neptuniumreihe 4n + 1 7 4 Uran-RadiumReihe 4n + 2 8 6 Actinium-UranReihe 4n + 3 7 4 Altersbestimmung mit Hilfe der 14C - Methode In der oberen Atmosphäre wird durch Kosmische Strahlung Die Halbwertzeit von erzeugt. durch β - Zerfall beträgt t½ =5730 Jahre. Im laufe der Erdgeschichte hat sich ein konstantes Verhältnis zu inaktiven CO2 ( 13CO2 ; 12CO2 ) eingestellt. Durch Assimilation wird das CO2 auf die Pflanzenwelt übertragen und dann auch von der Tierwelt aufgenommen. Nach dem Absterben hört der Stoffwechsel auf und damit auch die Gleichstellung von CO2 . Durch messung des 14CO2 Gehaltes lässt sich der Zeitpunkt des Absterbens bestimmen. Das Alter von Mineralien kann über den 238U - Gehalt im Verhältnis zum Zerfallsprodukt (z.B. 204Pb ) bestimmt werden. 6 1.3.2. Künstliche Nuklide Kernreaktionen können erzwungen werden, wenn man Kerne mit α - Teilchen, Protonen, Neutronen, Deutronen, u.a. beschießt. Nuklide mit den Ordnungszahlen 93-112; 114 konnten bereits hergestellt werden. 1.3.3. Kernspaltung, Kernfusion Spaltung von Uran durch thermische Neutronen Energiegewinn durch Zerfall des schweren Urankerns in zwei leichte Kerne Bei der Spaltung entstehenden Neutronen führen zu einer Kettenreaktion. ungesteuert: Es sind mehr (K) zur spaltung befähigte Neutronen vorhanden als benötigt werden (z.B. Atombombe) gesteuert: K = 1 (Atomreaktor) natürliches Uran als Spaltstoff Konkurenzreaktion: 238U + nschnell 239U* (nschnell => Bremssubstanz (Graphit) => nlangsam) nur 235U ist von den natürlichen Isotopen mit langsamen Neutronen spaltbar => Anreicherung Aber: 238U + nschnell 239U* 239Np 239Pa (auch Spaltbar) Kernenergie kann auch durch verschmelzung sehr leichter Kerne entstehen: 2H + 3H Aber sehr hohe Teilchenenergie ist erforderlich (107-108°C) 1952 in der Wasserstoffbombe realisiert: 6Li + n 3H Thermonukleare Reaktion + 4He / 2H + 3H => 22MeV; 4x mehr Energie als bei der Kernspaltung der gleichen Masse Kontrolierte Kernfusion ist noch nicht möglich, ist aber Wichtig: • • Rohstoffe sind in beliebiger Menge vorhanden Produkte sind nicht Radioaktiv 7 4He 235U 4He +n +n 1.3.4. Elementhäufigkeit, Elemententstehung Modell für die Entstehung der Elemente (ersten 50 Jahre): • • • Urknall Wasserstoff ist gebildet, Ausdehnung und Bildung kleiner Dichtefluktuationen Dichtere Stellen haben durch Gravitation Materie angezogen, Sterne entstehen, kinetische Energie wird zu Wärme 1.4. Die Strucktur der Elektronenhülle 1.4.1.Bohrsches Modell des Wasserstoffatomes 8