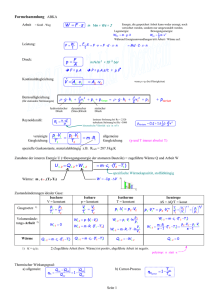
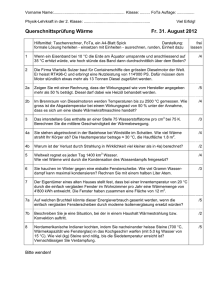
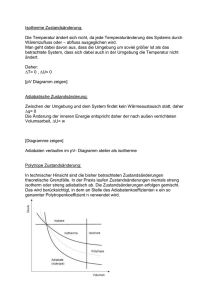
2. Klausur in "Technischer Thermodynamik I" 30.01
Werbung

UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Apl. Professor Dr.-Ing. K. Spindler 2. Klausur in "Technischer Thermodynamik I" 30.01.2012 (WS 2011/2012) ! Name:___________________ Fachr.:___________ Matr.-Nr.:______________ Es sind keine Hilfsmittel zugelassen. Zutreffende Aussagen sind anzukreuzen. Mehrere Antworten sind möglich. Falsche Antworten führen zu Punktabzug. Aufgabe 1 (5 Punkte) a) Der Gütegrad eines Verdichters kann bestimmt werden als Nutzen/Aufwand theoretisch zuzuführende Arbeit / tatsächlich zugeführte Arbeit tatsächlich zugeführte Arbeit / theoretisch zuzuführende Arbeit. b) Skizzieren Sie im nachfolgenden Diagramm, ausgehend vom Zustandspunkt 1, eine reversible polytrope Expansion (Polytropenexponent n=1) eines idealen Gases (=1,4). p c) Die Gleichung ds du dv zur Bestimmung der spezifischen Entropieänderung kann T T nur bei reversiblen Zustandsänderungen verwendet werden nur bei irreversiblen Zustandsänderungen verwendet werden sowohl bei reversiblen als auch irreversiblen Zustandsänderungen verwendet werden. d) In einem adiabaten System kann die Entropie zunehmen abnehmen gleichbleiben. e) Aus welchen reversiblen Zustandsänderungen setzt sich ein Carnot-Prozess zusammen 2 adiabate, 2 isochore 2 adiabate, 2 isotherme 2 adiabate, 2 isobare. f) Kennzeichnen Sie die richtige(n) Aussage(n): Arbeit kann vollständig in Exergie umgewandelt werden Wärme kann vollständig in Exergie umgewandelt werden. Exergie kann in Anergie umgewandelt werden. g) Ausgehend vom Zustand 1 wird einem idealen Gas irreversibel isobar Wärme zugeführt. Die Fläche unter der Zustandsänderung bis zur Entropieachse in einem T,s-Diagramm entspricht der zugeführten Wärme der Dissipationsarbeit der Summe aus Dissipationsarbeit und zugeführter Wärme Es sind keine Hilfsmittel zugelassen. Bearbeitete Aufgaben werden als vollständig richtig bewertet, wenn neben dem korrekten Endergebnis auch der Rechengang ersicht-lich ist. Aufgabe 2 (3 Punkte) Ein Kreisprozess kann durch die folgenden reversiblen Zustandsänderungen beschrieben werden: 1 - 2 Isentrope Kompression 2 - 3 Isobare Wärmezufuhr 3 - 4 Isentrope Expansion 4 - 1 Isochore Wärmeabfuhr. a) Zeichnen Sie den Kreisprozess im p,V- und T,S-Diagramm. p T V S b) Welches energetische Bewertungsmaß (=Nutzen/Aufwand) muss für den Kreisprozess verwendet werden? …………………………………………………………………………………………………… c) Kennzeichnen (Schraffieren) Sie den Nutzen sowie den Aufwand des Kreisprozesses in dem jeweils dafür geeigneten Diagramm (vgl. Teilaufgabe a)). Hinweis: Zur Darstellung des Nutzens und des Aufwands des Kreisprozesses sind jeweils unterschiedliche Diagramme zu verwenden. Aufgabe 3 (6 Punkte) Stickstoff (ideales Gas ; RN2 = 296,8 J/(kg K), = 1,4) vom Zustand p1 = 5 bar, T1 = 300 K wird adiabat (ohne Arbeitsabgabe nach außen) auf p2 gedrosselt, wodurch die spezifische Entropie um s12=0,4777 kJ/(kg K) zunimmt. Es findet keine Änderung von potentiellen und kinetischen Energien statt. a) Wie groß ist die Temperatur nach der Drosselung? T2 = …………… K b) Bestimmen Sie den Druck p2 nach der adiabaten Drosselung. p2 = …………… bar Die adiabate Drosselung soll nun durch eine adiabate Expansion von T1=300 K, p1 = 5 bar auf p2 = 1 bar in einer Turbine ersetzt werden. Der Turbinenwirkungsgrad beträgt G,T = 0,75. Es findet keine Änderung von potentiellen und kinetischen Energien statt. c) Wie groß ist spezifische Turbinenarbeit wt,12? wt,12 = …………… kJ/kg Aufgabe 4 (8 Punkte) 4.1 Einem Carnot-Prozess, der zwischen den Temperaturen 45°C und 10°C als Wärmepumpe arbeitet, wird die Antriebsleistung PWP = 11 kW zugeführt. Wie groß ist der Nutzwärmestrom Q ab der Wärmepumpe? Q ab = …………… kW 4.2 Ein voll gefüllter Warmwasserspeicher mit einem Volumen von 300 l und einer Anfangstemperatur von 1 = 50 °C kühlt sich infolge von Wärmeverlusten an die Umgebung (am = 22 °C) isochor auf 2 = 30 °C ab. Die folgenden Stoffwerte von Wasser sind gegeben: Spezifische Wärmekapazität cw = 4186 J/(kg K), Dichte bei 50°C 50°C = 988,1 kg/m3. a) Berechnen Sie die Verlustwärme Q12, die Entropieänderung des Wassers S12 sowie die Entropieänderung der Umgebung Sam Q12 =……………….... kJ, S12 = …………….kJ/K, Sam = …………… kJ/K b) Zeigen Sie mit Hilfe des 2. H.S., dass es sich bei diesem Vorgang um eine irreversible Zustandsänderung handelt. Formelzusammenstellung - 1. Hauptsatz: geschlossenes System dU dE kin dE pot dQ dW mit dh de kin de pot dq dw t offenes System mit - 2. Hauptsatz: dW pdV dWdiss dWmech, dw t vdp dw diss dw mech, geschlossenes System dS dS a dS i mit dS (dU pdV)/T (dH Vdp)/T dS a dQ/T , dS i dW diss /T du c V dT , dh c p dT - ideale Gase: dp dT dT dv - Ri cv Ri T p T v p V m Ri T ds c p =cp/cv; cp= cv + Ri p v const. , reversibel adiabate Zustandsänderung: T v 1 const. , -1 T/ p const. du dh c dT - inkompressible Medien (Flüssigkeiten / Festkörper): - Gütegrad (Turbine): G,T= wt , irreversibel Pirreversibel gewonnene Arbeit gewinnbarer Arbeit wt , reversibel Preversibel Kreisprozessarbeit zugeführte Wärme genutzte Wärme = Kreisprozessarbeit - Thermischer Wirkungsgrad: (Wärme-/Kraftmaschine) th= - Leistungszahl (Wärmepumpe / Kältemaschinen) - Umrechnung: 1 bar = 105 Pa = 105 N/m2= 105 J/m3 - Universelle (molare) Gaskonstante: R m 8,314 J/(mol K), R m M R i , M m/n - Mathematische Zusammenhänge: du ln(u) u