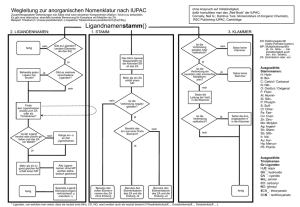
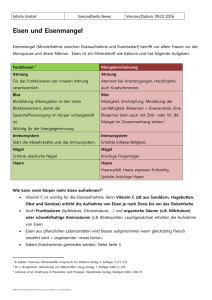
Extraktion/Komplexbildung
Werbung

Extraktion/Komplexbildung Inhalte dieser Lerneinheit: Quantitativer Nachweis von Eisen mit o-Phenanthrolin Quantitativer Nachweis von Kupfer mit Bichinolin Dabei werden Grundlagen der: Komplexbildung und der Extraktion besprochen. Quantitative Bestimmung von Fe und Cu Prinzip: Eisen- und Kupferionen sind in wässriger Lösung farblos, können aber mit sog. Liganden (organische Moleküle) stark gefärbte Komplexe bilden. Diese Komplexe können fotometrisch vermessen werden, aus der Extinktion errechnet man sich mit Hilfe des Lambert-Beer‘schen Gesetzes die Eisen- bzw. Kupferkonzentration. Der Eisenkomplex: Fe2+ bildet mit 3 Molekülen o-Phenanthrolin einen intensiv rot gefärbten Komplex: (3x) N N Fe2+ Wie entstehen diese N-Fe2+-Bindungen? Allg.: Struktur von Komplexverbindungen: Zentralatom: Metallion oder Metallatom Liganden: Moleküle oder Ionen, die sich an das Zentralatom anlagern freier Ligand: verfügt über mindestens ein Elektronenpaar, das er auf das Zentralatom übertragen kann. Meistens handelt es sich um nichtbindende (einsame oder freie) Elektronenpaare. Koordinationszahl: die Anzahl der direkt an das Zentralatom gebundenen Atome Komplexverbindungen: Die Übergangsmetalle haben eine ausgeprägte Tendenz zur Bildung von Komplexen an den Bindungen in Komplexen der Übergangsmetalle sind d-Orbitale des Zentralatoms beteiligt bei der Mehrzahl der Komplexe ist die Koordinationszahl zwei, vier oder sechs (am häufigsten) das Koordinationspolyeder bei Komplexen mit der Koordinationszahl sechs ist ein Oktaeder: 18-Elektronen-Regel: Es bilden sich Komplexe mit so vielen Liganden, dass eine Zahl von 18 Elektronen in der Valenzschale des Zentralatoms erreicht wird. Chelat-Komplexe: Manche Liganden können mehr als eine Koordinationsstelle am Zentralatom einnehmen diese Liganden bilden mit dem Zentralatom ringförmige Strukturen. Solche Komplexe werden Chelat-Komplexe (grichisch chele = Krebsschere) genannt Chelat-Komplexe sind im allgemeinen stabiler als Komplexe von sogenannten einzähnigen Liganden. Beispiel: Häm-Gruppe Die Häm-Gruppe im Hämoglobin ist ein ChelatKomplex des Fe2+. Das Metallion ist an einen vierzähnigen Liganden (Porphyrin) gebunden: M V N M M Fe2+ N N P V N P M M, Methyl-; P, Propionat; V, Vinyl- Häm-Gruppe: Das Eisenatom im Hämoglobin ist oktaedrisch koordiniert. Vier Koordinationsstellen entfallen auf die planare HämGruppe, mit der fünften wird die gesamte Häm-Gruppe an das Protein-molekül gebunden und in der sechsten Position wird entweder ein Molekül H2O (Hämoglobin) oder ein Molekül O2 (Oxyhämoglobin) gebunden. Die Koordination an der sechsten Position ist reversibel und hängt vom O2Partialdruck ab. Hämoglobin + O2 Oxyhämoglobin + H2O Häm-Gruppe: Hämoglobin nimmt in der Lunge O2 auf und gibt es im Körper wieder ab, wo es zur Oxidation von Nahrungsstoffen verwendet wird. Hämoglobin reagiert aber auch mit CO und CN-- Ionen, wobei Komplexe entstehen, die stabiler als Oxyhämoglobin sind. Deshalb wirken Kohlenmonoxid und Cyanide (Salze der Blausäure) toxisch. Zurück zum Eisen/o-Phenanthrolin-Komplex: Vergleichbar mit Hämoglobin handelt es sich hier um eine typische Komplexverbindung. O-Phenanthrolin agiert als zweizähniger Ligand, d.h., seine beiden Stickstoffatome stellen ihre nichtbindenden Elektronenpaare für die Bindung an das Zentralatom Eisen (genau: Fe2+-Ion) zur Verfügung. Drei o-Phenanthrolin-Moleküle lagern sich um das Eisen herum an, somit ist das Eisen oktaedrisch koordiniert (3 mal 2N = 6N-atome). Quantitative Bestimmung von Eisen: Fe2+ bildet mit o-Phenanthrolin einen intensiv rot gefärbten Komplex. In wässriger, sauerstoffhaltiger Lösung liegt aber Fe3+ vor, das vor der Komplexbildung reduziert werden muss. Der Komplex kann Licht einer ganz bestimmten Wellenlänge (510 nm) absorbieren. Die Fotometrie (Lichtmessung) ermöglicht es uns, von der absorbierten Lichtintensität auf die Konzentration der gefärbten Substanz (=Eisen/o-Phenanthrolin-Komplex) rück-zuschließen. Für nicht allzu stark konzentrierte Lösungen gilt das Lambert-Beer‘sche Gesetz: Die Extinktion (E) ist proportional dem Produkt der Stoffmengenkonzentration c [mol/L] und der Dicke d [cm] der absorbierenden Flüssigkeitsschicht. Die Proportionalitätskonstante ε wird als molarer Extinktionskoeffizient [L/mol cm] bezeichnet. Somit kann man sich bei bekanntem ε aus der im Laborversuch gemessenen Extinktion die Konzentration der gefärbten Substanz (in unserem Fall des Eisen/oPhenanthrolin-Komplexes) ausrechnen. • E=εcd Quantitative Bestimmung von Kupfer: Hier wird die Kupferbestimmung mittels fotometrischem Verfahren nach Landers und Zak beschrieben. Die Bestimmung basiert auf der Bildung eines intensiv gefärbten Komplexes von einem Ion Cu+ mit 2 Molekülen Bichinolin: N N Cu+ N N Reduktion des Kupfers: Nur Cu+ kann diesen Komplex bilden. In der zu untersuchenden Lösung muss (eventuell vorhandenes) Cu2+ zu Cu+ reduziert werden: • 2 Cu 2+ + 2 Asc 2 Cu + + 2 Dehydro-Asc + 2 H + CH2OH CH2OH HCOH HCOH O O O O HO OH Ascorbinsäure O O Dehydro-Ascorbinsäure Probleme in der Praxis: Üblicherweise bestimmt man in der Medizin Kupfer aus wässrigen Lösungen (z.B. aus Serum). Allerdings: das Komplexierungsmittel Bichinolin ist nahezu wasserunlöslich, aber sehr gut löslich in organischen Lösungsmittleln, wie z.B. Butanol. Wie kann hier eine Komplexbildung erfolgen, wo sich doch Zentralion und Ligand in unterschiedlichen, nicht mischbaren Phasen befinden? Problemlösung: man gibt beide Phasen (Phase 1: Cu+ in Wasser; Phase 2: Bichinolin in Butanol) in einen Scheidetrichter. Durch kräftiges Schütteln entstehen große „Austauschoberflächen“, sodass sich der Kupfer/BichinolinKomplex bilden kann. Extraktion: Butanolphase: enthält Bichinolin wässrige Phase: enthält Cu+ Kräftiges Schütteln: Durch das Schütteln geht Bichinolin spurenweise in die Wasserphase über. Die Konzentrationsverhältnisse werden durch das Nerst‘sche Verteilungsgesetz beschrieben: K = c(I) / c(II) Butanol Bichinolin Bichinolin Wasser • K…Nernst‘scher • • Verteilungskoeffizient c(I)…Konzentration des zu extrahierenden Stoffes in Phase I (z.B. Wasser) c(II)…Konzentration des zu extrahierenden Stoffes in Phase II (z.B. Butanol) Extraktion: In unserem Fall lautet das Nernst‘sche Verteilungsgesetz: K = cBichinolin in Wasser / cBichinolin in Butanol Für K ergibt sich ein sehr niedriger Wert, da Bichinolin in Wasser sehr schlecht löslich ist, aber sehr gut in Butanol. In Worten: das Verhältnis der Gleichgewichtskonzentrationen des Bichinolins in Wasser bzw. Butanol ist konstant. Extraktion: Butanol Bichinolin/Cu+-Komplex Bichinolin Bichinolin + Cu+ Bichinolin/Cu+-Komplex Wasser In Wasser reagiert das Bichinolin mit Cu+, es bildet sich ein BichinolinKupfer-Komplex. Dadurch ergeben sich 2 Folgereaktionen: 1. der Bichinolin-Kupfer-Komplex löst sich in Butanol besser als in Wasser, daher geht der Komplex laufend ins Butanol über 2. die Konzentration an freiem Bichinolin nimmt in der Wasserphase durch die Komplexbildung ab, es wird daher aus der Butanolphase nachgeliefert (= Einhaltung des Nernst‘schen Verteilungssatzes) Extraktion Somit geht das in Wasser gelöste Cu+ (fast) vollständig in die Butanolphase über: Cu+Wasser Cu+Butanol als Komplex Fotometrische Vermessung des BichinolinKupferkomplexes: Messlösung: Bichinolin-Kupfer-Komplex in Butanol Spuren von Wasser könnten zu Trübungen führen. Deshalb wird die Butanolphase vor der Messung mit Natriumsulfat(= hygroskopisches Salz) getrocknet. Wie schon weiter oben für Eisen beschrieben, errechnet man sich aus der gemessenen Extinktion mit Hilfe des Lambert-Beer‘schen Gesetzes die Kupferkonzentration (ε muss bekannt sein).