8 Ultraschalluntersuchung bei Erkrankungen der
Werbung
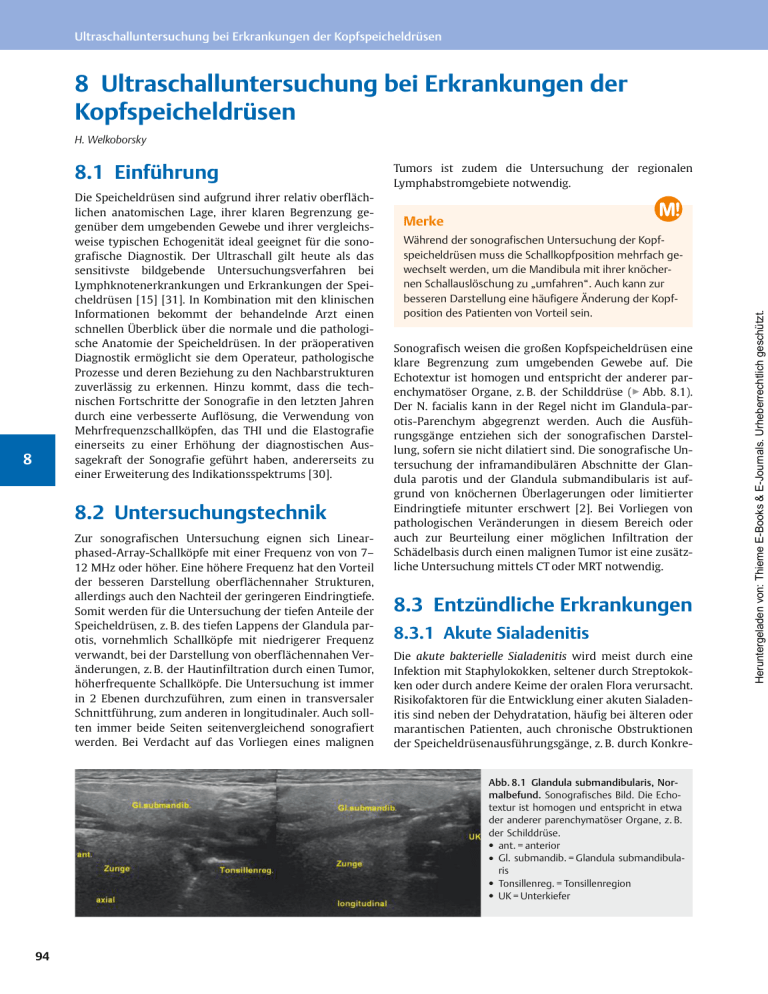
Ultraschalluntersuchung bei Erkrankungen der Kopfspeicheldrüsen 8 Ultraschalluntersuchung bei Erkrankungen der Kopfspeicheldrüsen H. Welkoborsky Die Speicheldrüsen sind aufgrund ihrer relativ oberflächlichen anatomischen Lage, ihrer klaren Begrenzung gegenüber dem umgebenden Gewebe und ihrer vergleichsweise typischen Echogenität ideal geeignet für die sonografische Diagnostik. Der Ultraschall gilt heute als das sensitivste bildgebende Untersuchungsverfahren bei Lymphknotenerkrankungen und Erkrankungen der Speicheldrüsen [15] [31]. In Kombination mit den klinischen Informationen bekommt der behandelnde Arzt einen schnellen Überblick über die normale und die pathologische Anatomie der Speicheldrüsen. In der präoperativen Diagnostik ermöglicht sie dem Operateur, pathologische Prozesse und deren Beziehung zu den Nachbarstrukturen zuverlässig zu erkennen. Hinzu kommt, dass die technischen Fortschritte der Sonografie in den letzten Jahren durch eine verbesserte Auflösung, die Verwendung von Mehrfrequenzschallköpfen, das THI und die Elastografie einerseits zu einer Erhöhung der diagnostischen Aussagekraft der Sonografie geführt haben, andererseits zu einer Erweiterung des Indikationsspektrums [30]. 8 8.2 Untersuchungstechnik Zur sonografischen Untersuchung eignen sich Linearphased-Array-Schallköpfe mit einer Frequenz von von 7– 12 MHz oder höher. Eine höhere Frequenz hat den Vorteil der besseren Darstellung oberflächennaher Strukturen, allerdings auch den Nachteil der geringeren Eindringtiefe. Somit werden für die Untersuchung der tiefen Anteile der Speicheldrüsen, z. B. des tiefen Lappens der Glandula parotis, vornehmlich Schallköpfe mit niedrigerer Frequenz verwandt, bei der Darstellung von oberflächennahen Veränderungen, z. B. der Hautinfiltration durch einen Tumor, höherfrequente Schallköpfe. Die Untersuchung ist immer in 2 Ebenen durchzuführen, zum einen in transversaler Schnittführung, zum anderen in longitudinaler. Auch sollten immer beide Seiten seitenvergleichend sonografiert werden. Bei Verdacht auf das Vorliegen eines malignen Tumors ist zudem die Untersuchung der regionalen Lymphabstromgebiete notwendig. H ● Merke Während der sonografischen Untersuchung der Kopfspeicheldrüsen muss die Schallkopfposition mehrfach gewechselt werden, um die Mandibula mit ihrer knöchernen Schallauslöschung zu „umfahren“. Auch kann zur besseren Darstellung eine häufigere Änderung der Kopfposition des Patienten von Vorteil sein. Sonografisch weisen die großen Kopfspeicheldrüsen eine klare Begrenzung zum umgebenden Gewebe auf. Die Echotextur ist homogen und entspricht der anderer parenchymatöser Organe, z. B. der Schilddrüse (▶ Abb. 8.1). Der N. facialis kann in der Regel nicht im Glandula-parotis-Parenchym abgegrenzt werden. Auch die Ausführungsgänge entziehen sich der sonografischen Darstellung, sofern sie nicht dilatiert sind. Die sonografische Untersuchung der inframandibulären Abschnitte der Glandula parotis und der Glandula submandibularis ist aufgrund von knöchernen Überlagerungen oder limitierter Eindringtiefe mitunter erschwert [2]. Bei Vorliegen von pathologischen Veränderungen in diesem Bereich oder auch zur Beurteilung einer möglichen Infiltration der Schädelbasis durch einen malignen Tumor ist eine zusätzliche Untersuchung mittels CT oder MRT notwendig. 8.3 Entzündliche Erkrankungen 8.3.1 Akute Sialadenitis Die akute bakterielle Sialadenitis wird meist durch eine Infektion mit Staphylokokken, seltener durch Streptokokken oder durch andere Keime der oralen Flora verursacht. Risikofaktoren für die Entwicklung einer akuten Sialadenitis sind neben der Dehydratation, häufig bei älteren oder marantischen Patienten, auch chronische Obstruktionen der Speicheldrüsenausführungsgänge, z. B. durch Konkre- Abb. 8.1 Glandula submandibularis, Normalbefund. Sonografisches Bild. Die Echotextur ist homogen und entspricht in etwa der anderer parenchymatöser Organe, z. B. der Schilddrüse. ● ant. = anterior ● Gl. submandib. = Glandula submandibularis ● Tonsillenreg. = Tonsillenregion ● UK = Unterkiefer 94 Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. 8.1 Einführung 8.3 Entzündliche Erkrankungen Abb. 8.2 Akute Sialadenitis der Glandula submandibularis links. Die Sialadenitis wurde durch ein Konkrement hervorgerufen. Es ist aufgelockertes Drüsenparenchym mit Inhomogenitäten, Sekretstau und aufgestauten Speichelgängen auszumachen. Das Konkrement stellt sich im Drüsenparenchym als kalkdichte Struktur mit dorsalem Schallschatten dar. 8.3.2 Chronische Entzündung Chronische Entzündungen der Speicheldrüsen können durch eine Reihe von unterschiedlichen Erkrankungen hervorgerufen werden. Beispiele sind chronische Sialadenitiden bei folgenden Erkrankungen: ● Konkremente in den Ausführungsgängen ● ektatische Ausführungsgänge der Glandula parotis bei Kindern und Jugendlichen ● Sarkoidose oder andere granulomatöse Entzündungen ● Sjögren-Syndrom ● Küttner-Tumor ● atypische Mykobakteriose 8 Das sonografische Bild der chronischen Sialadenitis ist nicht einheitlich und durch die zugrunde liegende Erkrankung bestimmt [35]. Oft findet sich eine heterogene Echotextur mit intraparenchymal gelegenen, echoärmeren Bezirken. In vielen Fällen können zusätzliche ovaläre bis längliche, echoarme bis echoleere Areale nachgewiesen werden, die ektatischen Ausführungsgängen entsprechen können (▶ Abb. 8.5). Farb-Doppler-sonografisch ist die Vaskularisierung insgesamt vermindert; lediglich beim Vorliegen von granulomatösen Erkrankungen (z. B. beim Heerfordt-Syndrom) kann sie erhöht sein [28]. Im Endzustand einer chronischen Sialadenitis ist das gesamte Drüsenparenchym echoarm. Häufig kommen intraoder periglandulär gelegene Lymphknoten zur Darstellung. Sonderformen der chronischen Sialadenitis sind der Küttner-Tumor, die atypische Mykobakteriose und das Sjögren-Syndrom. Bei der atypischen Mykobakteriose im Kopf-Hals-Bereich handelt es sich genau genommen nicht um eine Entzündung der Speicheldrüsen, sondern eine der Lymphknoten. 95 Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. mente oder Strikturen. Die klinische Diagnosestellung bereitet in der Regel keine Schwierigkeiten. Die betroffene Drüse ist akut schmerzhaft geschwollen; mitunter lässt sich eitriges Sekret aus der Drüse ausmassieren. Sonografisch ist die betroffene Drüse vergrößert und echoarm. Das Drüsenparenchym selbst stellt sich aufgelockert und inhomogen dar, immer wieder unterbrochen durch hypodense Areale unterschiedlicher Größe. In vielen Fällen können Lymphknoten im Drüsenparenchym oder in der Umgebung der Drüse nachgewiesen werden, die meist ovalär sind und eine Hilusstruktur aufweisen (▶ Abb. 8.2). In der Farb-Doppler-Sonografie stellt sich die akut-entzündlich veränderte Drüse mit zahlreichen Gefäßen dar, die in Septen zwischen den echoarmen Arealen verlaufen. In den Lymphknoten können häufig Hilusgefäße mit zentraler Vaskularisierung der Knoten sowie Hypervaskularisierung und Hyperperfusion nachgewiesen werden (▶ Abb. 8.3). Die Erkennung einer Abszessbildung und deren Abgrenzung gegenüber einer reinen akuten Entzündung sind klinisch nur schwer möglich. Sonografisch fallen unscharf begrenzte, echoarme oder echoleere Bezirke auf, meist mit einer dorsalen Schallverstärkung und unscharfer Begrenzung (▶ Abb. 8.4). Farb-Doppler-sonografisch können in diesen Arealen keine Gefäße sichtbar gemacht werden. Bei Unsicherheit sollte eine sonografisch gesteuerte Feinnadelpunktion erfolgen, mit der der Abszess gesichert und gegebenenfalls drainiert werden kann [14] [35]. Virale Entzündungen (z. B. mit dem Mumpsvirus) führen in der Regel zu einer beidseitigen Schwellung der Speicheldrüsen, insbesondere der Glandula parotis. Sie sind die häufigste Ursache der akuten Speicheldrüsenentzündung im Kindesalter. Die sonografischen Charakteristika sind ähnlich denen einer akuten bakteriellen Entzündung. 8 Abb. 8.3 Akute Parotitis links. a Die Drüse ist insgesamt vergrößert. Das Drüsenparenchym ist aufgelockert mit Inhomogenitäten. Keine fokale Läsion, die auf eine Abszessbildung hindeuten könnte. b Innerhalb der Drüse kommen mitunter Lymphknoten zur Darstellung. c In der Farb-Doppler-Sonografie können zahlreiche Gefäße als Hinweis auf eine Hyperperfusion identifiziert werden. ● M. masseter = M. masseter ● UK = Unterkiefer Abb. 8.4 Glandula-parotis-Abszess. Der Abszess weist einen intraparenchymal gelegenen, unscharf begrenzten Bezirk mit dorsaler Schallverstärkung auf. ● Mandib. = Mandibula 96 Abb. 8.5 Chronische Sialadenitis der Glandula submandibularis rechts. Auffallend ist eine insgesamt im Vergleich zu normalem Speicheldrüsengewebe kleinere Drüse und eine echoärmere und heterogene Echotextur mit eingestreuten echoarmen oder echoleeren Arealen. ● GSM = Glandula submandibularis Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. Ultraschalluntersuchung bei Erkrankungen der Kopfspeicheldrüsen Abb. 8.6 Atypische Mykobakteriose und Küttner-Tumor. a Atypische Mykobakteriose im Bereich der Glandula-parotis-Loge. Echoarme, ovaläre, unscharf begrenzte Raumforderungen, intraglandulär bis in das subkutane Gewebe reichend. Die Knoten sind septiert und von unterschiedlicher Größe. b Korrespondierende Aufnahme zu a. ● LK = Lymphknoten ● PAR/PAROTIS = Glandula parotis ● RF = Raumforderung ● UK = Unterkiefer Fallstricke R ● Häufig sind aber bei der atypischen Mykobakteriose die intraparotidealen Lymphknoten und die Lymphknoten in der Submandibularloge befallen; dies kann eine Sialadenitis oder einen Speicheldrüsentumor vortäuschen. Die Krankheit befällt häufig Kinder und wird durch eine Infektion mit nicht tuberkulösen Mykobakterien, meist Mycobacterium avium oder Mycobacterium malmoense, hervorgerufen. Als Eintrittspforte werden u. a. die Tonsillen diskutiert. Auch ein Zusammenhang mit dem Genuss von nicht pasteurisierter Milch wird angenommen [10] [23]. Sonografisch imponieren solitäre oder multiple, echoarme, unscharf begrenzte Raumforderungen, die intraparotideal gelegen sein und bis in das subkutane Fettgewebe reichen können. Die Lymphknoten sind von Septen durchzogen (▶ Abb. 8.6a und ▶ Abb. 8.6b). Der Küttner-Tumor ist eine chronische Entzündung, die in der Glandula submandibularis auftritt (Synonym: chronisch-sklerosierende Sialadenitis). Das histologische Bild wird geprägt von einer erheblichen Vermehrung der interlobulären Bindegewebeschicht mit Fibrosierung, Infiltration von Entzündungszellen und Ablagerung von Kalk. Sonografische Charakteristika sind multifokale echoarme Areale in einer normal begrenzten Drüse und eine heterogene Echotextur (▶ Abb. 8.7). Differenzialdiagnostisch muss immer eine Neoplasie der Speicheldrüse ausgeschlossen werden [7]. Das Sjögren-Syndrom ist eine chronische Autoimmunerkrankung. Meist sind Frauen jenseits des 40. Lebensjahrs betroffen. Klinisch steht eine verminderte Tränenund Speichelproduktion mit Mund- und Augentrocken- heit im Vordergrund. Histologisches Charakteristikum ist eine lymphozytäre und plasmazelluläre Infiltration der Speichel- und Tränendrüsen, die hierdurch zerstört werden. Das sonografische Erscheinungsbild ist, je nach Erkrankungsstadium, relativ charakteristisch [25]. Es ist gekennzeichnet durch eine erheblich heterogene Echotextur mit multiplen kleinen, intraparenchymal gelegenen, echoarmen bis echoleeren, runden oder ovalen Arealen, die den zerstörten Drüsenanteilen mit lymphozytärer Infiltration und dilatierten Ausführungsgängen entsprechen (▶ Abb. 8.8) [24] [27]. Farb-Doppler-sonografisch ergibt sich in diesen Arealen ein erhöhter Blutfluss. 8 Abb. 8.7 Küttner-Tumor der Glandula submandibularis links (Synonym: chronisch-sklerosierende Sialadenitis). In der Drüse finden sich echokomplexere und echoarme Areale sowie eine heterogene Echotextur. Die Veränderungen betreffen die gesamte Drüse. 97 Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. 8.3 Entzündliche Erkrankungen Abb. 8.8 Sjögren-Syndrom. Sonografische Bilder. Charakteristisch sind die multiplen, im gesamten Parenchym eingestreuten echoarmen oder echoleeren, ovalären Areale, die den zerstörten Drüsenanteilen mit lymphozytärer Infiltration und dilatierten Ausführungsgängen entsprechen. a Glandula parotis. b Glandula submandibularis. ● GSM = Glandula submandibularis ● Parotis = Glandula parotis Merke H ● Das Sjögren-Syndrom ist in einigen Fällen mit lymphoproliferativen Erkrankungen assoziiert. Daher müssen bei jeder sonografischen Untersuchung der Speicheldrüsen, die unter dem Verdacht eines Sjögren-Syndroms vorgenommen wird, auch die regionären Lymphknoten mituntersucht werden. 8 Mittels Sonografie kann die Diagnose eines Sjögren-Syndroms bereits in frühen Phasen der Erkrankung mit einer Sicherheit von etwa 90 % gestellt werden. Von manchen Autoren wird zur Evaluation der sonografischen Befunde ein parenchymatöser Inhomogenitäts-Score empfohlen, der die Treffsicherheit noch weiter erhöhen soll [21] [22] [29]. 8.3.4 Lymphadenitis Die intraparotidealen Lymphknoten stellen die erste Drainagestation von Stirn- und Wangenhaut, Orbita, Ohrmuschel und Oberkieferzähnen dar. In der Glandula submandibularis sind keine Lymphknoten vorhanden. Allerdings befinden sich periglandulär in der Glandula-submandibularis-Loge zahlreiche Lymphknoten, die eine Drainagestation für die Unterkiefer- und Mundbodenregion sowie die Gesichtshaut sind. Die intraparotidealen Lymphknoten sind normalerweise nicht darstellbar. Bei Entzündungen mit intraglandulärer Lymphadenitis können diese Lymphknoten gut vom umgebenden Gewebe unterschieden werden. Sie kommen echoarm mit einer Hilusstruktur zur Darstellung (▶ Abb. 8.9). Eine dorsale Schallverstärkung fehlt meist. Lymphknoten treten isoliert oder multipel auf. R ● 8.3.3 Sialadenosen Fallstricke Bei den Sialadenosen handelt es sich um eine heterogene Gruppe von Erkrankungen der Speicheldrüsen. Die Ursachen sind unterschiedlich. Sonografisch sind die Veränderungen im Drüsenparenchym unspezifisch. Es kann eine Vergrößerung des gesamten Organs ohne strukturelle Auffälligkeiten vorliegen. Daneben werden auch kleine zystische Ektasien und Auflockerungen gefunden. Generell ist das Speicheldrüsenparenchym meist etwas echoreicher. Ein typisches sonografisches Bild, ähnlich wie beim Sjögren-Syndrom, liegt nicht vor. Fehlt eine Hilusstruktur, so können Lymphknoten mit intraglandulärer Lymphadenitis, vor allem bei fehlender entzündlicher Klinik, differenzialdiagnostische Schwierigkeiten hinsichtlich der Abgrenzung gegenüber einem malignen Lymphom, einer Lymphknotenmetastase, einer Sarkoidose oder einer Neoplasie bereiten. Sie sollten sonografisch bezüglich ihrer Wachstumstendenz kontrolliert und gegebenenfalls sonografisch gesteuert punktiert werden, um eine zytologische Klärung der Dignitätsdiagnose zu erreichen. Bei einer Borreliose lassen sich meist vergrößerte Lymphknoten im Bereich des kaudalen Glandula-parotis-Poles 98 Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. Ultraschalluntersuchung bei Erkrankungen der Kopfspeicheldrüsen Abb. 8.9 Lymphadenitis im Bereich der Glandula parotis rechts. Die Lymphknoten sind echoarm und können gut von Drüsenparenchym abgegrenzt werden. In den Lymphknoten kommt eine Hilusstruktur zur Darstellung. und in der Umgebung des Foramen stylomastoideum nachweisen. Diese gelten bei gleichzeitiger Fazialisparese als geradezu typisch für das Vorliegen einer Borelliose. Die Diagnose der periglandulären Lymphkoten in der Glandula-submandibularis-Region bereitet in der Regel keine Schwierigkeiten. Die Lymphknoten sind echoarm und können meist gut von dem Drüsenparenchym abgegrenzt werden. Bei einer reaktiven Lymphadenitis kommt in der Regel eine Hilusstruktur zur Darstellung. laufsrichtung des Wharton-Ganges. Auch eine höhere Kalziumkonzentration des von der Glandula submandibularis gebildeten Speichels mit hierdurch einhergehender höherer Konkrementneigung wird diskutiert [18]. Klinisch steht eine Vergrößerung der Drüse im Vordergrund. Diese kann sich bei Nahrungsaufnahme verstärken und dann auch schmerzhaft sein. Der diagnostische Nachweis von Konkrementen bereitet mitunter Schwierigkeiten. Im CT stellen sich nur größere Konkremente dar. Die MRT-Sialografie ist ein kostenintensives und aufwendiges Verfahren, bei dem eine Sialografie mit der MRT-Untersuchung kombiniert wird. Hiermit gelingt der Steinnachweis in 90 % der Fälle. Auch ermöglicht sie bei Aufstau der Drüse die Differenzialdiagnose zwischen einem Konkrement und einer narbigen Striktur des Ausführungsgangs. Ein weiteres diagnostisches Verfahren ist die Sialoendoskopie, bei der mit einem dünnen Endoskop in den Stenon- bzw. WhartonGang eingegangen wird. Bei Nachweis eines Konkrements kann dieses mittels spezieller Instrumente entfernt werden (s. Kap. 11.6) [12] [13]. Sonografisch gelingt der Steinnachweis regelmäßig ab einer Größe von etwa 2 mm, in Einzelfällen auch bei einer Größe von weniger als 1 mm [16]. Die Sensitivität wird mit 94 %, die Spezifität mit bis zu 100 % und die diagnostische Treffsicherheit mit bis zu 96 % angegeben [16]. In der B-Mode-Sonografie findet sich eine Erweiterung des Ausführungsgangsystems proximal des Konkrements. Der betroffene Ausführungsgang stellt sich als echoarme tubuläre Struktur dar [17]. Häufig führt ein Stein in einem großen Ausführungsgang zu einem Aufstau und einer Dilatation des gesamten Gangsystems; dies kann bis in die Peripherie hinein nachverfolgt werden (▶ Abb. 8.10). Die Farb-Doppler-Sonografie erleichtert im Zweifelsfalle die Differenzialdiagnose zwischen einem dilatierten Gang 8 8.4 Sialolithiasis Über die Hälfte der Speicheldrüsenentzündungen wird durch Konkremente verursacht. Die Konkremente können sowohl im Ausführungsgang als auch im Drüsenparenchym lokalisiert sein. Sie können solitär oder multipel auftreten. Liegen sie weit distal, so können sie meist palpiert werden. Weit intraparenchymal gelegene Steine entziehen sich häufig der Palpation. Während sich die Konkremente der Glandula parotis überwiegend im distalen Ausführungsgang befinden, liegen sie bei Erkrankung der Glandula submandibularis entweder im distalen Ausführungsgang oder im Drüsenparenchym. Etwa 90 % der Konkremente in den Speicheldrüsen treten in der Glandula submandibularis auf, nur 10–15 % in der Glandula parotis. Die Gründe hierfür liegen einerseits in dem von der Glandula submandibularis gebildeten zäheren Speichel, andererseits in der aufsteigenden Ver- Abb. 8.10 Aufgestauter Ausführungsgang der Glandula parotis links. Der Gang stellt sich als tubuläre, echoarme Struktur dar. Der Aufstau kann bis in die Peripherie verfolgt werden. Differenzialdiagnostisch kommen als Ursache entweder ein Konkrement, ein Tumor oder eine narbige Striktur infrage. ● Mand = Mandibula ● Parotis = Glandula parotis 99 Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. 8.4 Sialolithiasis a M. sternocleidomastoideus Glandula submadibularis A. facialis Konkrement Lymphknoten 8 b c Abb. 8.11 Sialolithiasis der Glandula submandibularis. Die Konkremente stellen sich als echoreiche Strukturen im Gangsystem mit dorsaler Schallauslöschung dar. a Deutliche Dilatation der Ausführungsgänge. (Konkrement mit Pfeil markiert). b Schematische Darstellung der Lagebeziehungen der einzelnen Strukturen in c. c Neben dem Konkrement (+ ... +) überdies Nachweis eines Lymphknotens in der Glandula-submandubularis-Loge. Das Konkrement ist im Drüsenparenchym impaktiert (mit gestrichelten Linien markierter Bereich). ● GSM RE = Glandula submandibularis rechts und einem Blutgefäß ( Video 8.1). Typisch ist der Nachweis eines Schallschattens durch das Konkrement (▶ Abb. 8.11). Allerdings verursachen in der Regel nur Konkremente mit einem Durchmesser von mehr als 2 mm einen Schallschatten. Mittels der Sonopalpation kann in solchen Fällen die Treffsicherheit der Sonografie 100 erhöht werden. Hierbei wird der Schallkopf mit einer Hand auf der betroffenen Drüse fixiert, während die andere Hand die Drüse von enoral palpiert. Dieses Verfahren erleichtert insbesondere die Darstellung von kleineren Steinen [15]. Mitunter gelingt es sogar, den Stein sonografisch kontrolliert „auszumassieren“. Bei typischer Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. Ultraschalluntersuchung bei Erkrankungen der Kopfspeicheldrüsen 8.5 Tumoren der Speicheldrüsen Video 8.1 Farb-Doppler-Sonografie einer Glandula parotis mit aufgestautem Gangsystem. Eine Gefäßversorgung findet sich nur in den Randbereichen des dilatierten Ganges. Da es bei über 50 % der Patienten mit einem Konkrement zu einer Sialadenitis kommt, finden sich im Sonogramm im akuten Stadium auch Zeichen der akuten Sialadenitis. Bei fortgeschrittenem Steinleiden geht die Entzündung in eine chronische Sialadenitis über, im Rahmen derer keine Dilatation der Ausführungsgänge mehr nachweisbar ist, da die Drüse im Endstadium keine oder nur noch eine sehr eingeschränkte sekretorische Funktion ausübt. Zur Verbesserung der Visualisierung des Gangsystems und damit einhergehender höherer diagnostischer Treffsicherheit insbesondere von kleinen Konkrementen wurde die IA-CEUS (intraduktale kontrastverstärkte Sonografie, Intraductally applied Contrast-enhanced Ultrasound) beschrieben. Hierbei wird ein Kontrastverstärker intraduktal verabreicht [5] [34]. Inwieweit sich hierdurch die diagnostische Aussagekraft entscheidend erhöhen lässt, muss derzeit noch offen bleiben. 8.5 Tumoren der Speicheldrüsen Bei den Tumoren der Speicheldrüsen handelt es sich in 70–80 % der Fälle um benigne Neubildungen. Der Anteil an malignen Tumoren nimmt allerdings zu, je kleiner die Speicheldrüse ist, in der sie auftreten. Etwa 80 % der Glandula-parotis-Tumoren sind benigne, etwa 60 % der Tumoren in der Glandula submandibularis, aber nur etwa 30 % der Tumoren der kleinen Speicheldrüsen [20]. Zwischen 80 und 90 % der benignen Tumoren sind in der Glandula parotis lokalisiert. ▶ Tab. 8.1 zeigt die klinischen und sonografischen Charakteristika von Raumforderungen der Speicheldrüsen. 8.5.1 Pleomorphe Adenome Bei dem pleomorphen Adenom handelt es sich um den häufigsten benignen Speicheldrüsentumor. Er tritt in nahezu ¾ aller Fälle in der Glandula parotis auf. Klinisch imponiert eine langsam progrediente, in der Regel schmerzlose, palpatorisch relativ derbe, unilaterale und solitäre Raumforderung. Sonografisch kommt das pleomorphe Adenom als echoarme, gut begrenzte Raumforderung zur Darstellung. Eine lobulierte Struktur des Tumors und eine polyzyklische Begrenzung gelten als charakteristisch (▶ Abb. 8.12 und ▶ Abb. 8.13). Bedingt durch die Histologie des Tumors mit chondroiden und fibrotischen neben drüsigen und epithelialen Anteilen kann die Echogenität homogen oder inhomogen sein. Intratumoröse Kalzifikationen sind nicht selten. In der Farb-Doppler-Sonografie findet sich eine geringe oder gar keine Vaskularisation im Tumorparenchym. Die Gefäße sind meist in der Kapsel lo- 8 Tab. 8.1 Synopsis der klinischen und sonografischen Charakteristika bei Raumforderungen der Speicheldrüsen (modifiziert nach [31]). Charakteristika Benigne Raumforderungen Maligne Raumforderungen Klinische Charakteristika Histologie Pleom, Adenom Zystadenolymphom andere (Basalzelladenom, Onkozytom usw.) adenoidzystisches Karzinom, Adenokarzinom usw. Mukoepidermoidkarzinom malignes Lymphom Ausdehnung solitär, unilateral solitär oder multilokulär; auch bilateral (10 %) solitär, unilateral solitär, unilateral solitär, unilateral multilokulär Lymphknotenbefall nein nein nein ja, möglich ja, möglich ja, auch Halslymphknoten Nervparesen in der Regel nicht nein nein möglich möglich nein Wachstumsgeschwindigkeit langsam; bei Karzinom im pleomorphen Adenom schnell langsam langsam langsam bis schnell langsam bis schnell schnell Schmerzen nein nein nein relativ häufig weniger häufig nein 101 Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. Anamnese und sonografisch fehlendem Konkrementnachweis kann durch die Gabe von saueren Drops oder von Vitamin-C-Pulver die Speichelproduktion stimuliert werden. Bei Vorhandensein eines Konkrements kommt es aufgrunddessen zu einer Dilatation des Ausführungsgangs, die sich leicht sonografisch nachvollziehen lässt. Intraduktal gelegene Steine kommen dann häufig zur Darstellung [3]. Ultraschalluntersuchung bei Erkrankungen der Kopfspeicheldrüsen Tab. 8.1 Fortsetzung Charakteristika Benigne Raumforderungen Maligne Raumforderungen Abgrenzbarkeit/Form gut ovalär, polyzyklisch gut ovalär gut ovalär gut, bei infiltrativem Wachstum schlecht ovalär; irreguläre Begrenzung gut, bei infiltrativem Wachstum schlecht ovalär bis rund; mitunter irreguläre Begrenzung gut rund Echoverhalten echoarm echoarm echoarm echoarm bis echokomplex echoarm bis echokomplex echoarm bis echoleer Echotextur homogen; lobuliert inhomogen; zystische Areale homogen inhomogen inhomogen; zahlreiche Binnenechos; auch zystische Areale mit dorsaler Schallverstärkung homogen dorsale Schallverstärkung ++ + ++ + + + Vaskularisierung schlecht schlecht; in sehr echoarmen Anteilen teils gut schlecht uncharakteristisch; Kaliberschwankungen der Gefäße uncharakteristisch; häufig wenig Gefäße im Tumorinneren nachweisbar gut 8 Abb. 8.12 Pleomorphes Adenom in der Glandula parotis links. a Der Tumor stellt sich echoarm mit polyzyklischer Begrenzung und dorsaler Schallverstärkung dar. Einige Inhomogenitäten innerhalb des Tumors entsprechen den Tumorbezirken mit hohem respektive niedrigem Anteil an myxoidem Gewebe. Rechts im Bild ist die V. retromandibularis dargestellt. b Histologisches Bild des pleomorphen Adenoms. Deutlich erkennbar die myxoiden und chondroiden Anteile des Tumors, die sich im Sonogramm als echoreichere Areale darstellen. Hämatoxylin-Eosin-Färbung × 125. (Foto: mit freundlicher Genehmigung von Herrn Prof. Dr. L. Wilkens, Pathologisches Institut des Klinikum Nordstadt, Hannover) ● Parotis = Glandula parotis ● RF = Raumforderung ● UKW = Unterkieferwinkel ● Vene = V. retromandibularis Abb. 8.13 Pleomorphes Adenom im Bereich der Glandula submandibularis rechts. Der Tumor ist gut abgrenzbar gegenüber dem umgebenden Speicheldrüsengewebe. Es sind eine polyzklische Begrenzung und Inhomogenitäten vorhanden. Angedeutete dorsale Schallverstärkung. Somit ergibt sich ein ähnliches sonografisches Bild wie bei den pleomorphen Adenomen der Glandula parotis. 102 Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. Sonografische Charakteristika 8.5 Tumoren der Speicheldrüsen Merke H ● Abb. 8.14 Pleomorphes Adenom der Glandula parotis links. Farb-Doppler-Sonografie. Die Gefäße sind in der Kapsel des Tumors lokalisiert. Im Zentrum ist nur wenig Perfusion vorhanden. Ein zuführendes Gefäß ist erkennbar; es verläuft durch das Parenchym zum Tumor. kalisiert. Ein vorherrschender Perfusionstyp mit zentraler bzw. peripherer Perfusion existiert nicht (▶ Abb. 8.14 und Video 8.2) [6] [11] [33]. Video 8.2 Farb-Doppler-Sonografie bei pleomorphem Adenom. Die Gefäßversorgung erfolgt weitestgehend über die Tumorkapsel. Im Tumorparenchym sind nahezu keine Gefäße darstellbar. Rezidive von pleomorphen Adenomen stellen sich als solitär oder multipel aufretende, echoarme, noduläre Strukturen im Drüsenbett dar (▶ Abb. 8.15). Sie sind in dem Narbengewebe oft schlecht abgrenzbar. Bei Verdacht auf das Vorliegen von Rezidiven von pleomorphen Adenomen ist die Untersuchung des gesamten Drüsenbetts sowie der angrenzenden Haut von besonderer Bedeutung, da die Rezidive häufig durch eine Zellaussaat hervorgerufen werden und dann multilokulär auftreten und auch im subkutanem Fettgewebe lokalisiert sein können. 8.5.2 Monomorphe Adenome Beim Zystadenolymphom handelt es sich um den zweithäufigsten benignen Speicheldrüsentumor und um das häufigste monomorphe Adenom. Es hat einen Anteil von ca. 10 % an allen Speicheldrüsentumoren und tritt meist in der Glandula parotis auf. Männer mit Nikotinkonsum sind häufiger betroffen. Klinische Besonderheit der Zystadenolymphome ist ihre Multilokularität. In etwa 10 % der Fälle treten mehrere Tumoren innerhalb einer Speicheldrüse auf, in weiteren ca. 10 % der Fälle bilateral in beiden Parotiden. 8 Abb. 8.15 Rezidiv eines pleomorphen Adenoms bei Zustand nach Parotistumoroperation 12 Jahre zuvor. Multiple, echoarme Raumforderungen mit dorsaler Schallverstärkung im gesamten Drüsenbett. a Multiple Raumforderungen ohne eindeutige gemeinsame Kapsel. Multiple Rezidive möglich nach Voroperation. b Polyzyklische Raumforderungen im Parotisunterpol. 103 Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. Vorsicht ist geboten, wenn ein seit längerer Zeit bestehender Tumor plötzlich ein rasches Wachstum entwickelt. Hier ist ein Übergang von einem pleomorphen Adenom in ein Karzinom im pleomorphen Adenom nicht auszuschließen; das Risiko nimmt mit der Zeit zu. Auch die Entwicklung einer Fazialisparese kann als Malignitätskriterium gelten. Abb. 8.16 Ausgedehntes Zystadenolymphom in der Glandula parotis rechts. a Der Tumor ist echoarm, relativ gut abgrenzbar und von echoleeren Arealen mit dorsaler Schallverstärkung durchzogen; diese Areale entsprechen den zystischen Anteilen. b Histologischer Schnitt des Tumors. Deutlich erkennbar sind die zystischen Anteile, die sich sonografisch darstellen, neben soliden Tumorformationen. Hämatoxylin-Eosin-Färbung × 125. (Foto: mit freundlicher Genehmigung von Herrn Prof. Dr. L. Wilkens, Pathologisches Institut des Klinikum Nordstadt, Hannover) Sonografisch besteht eine echoarme, gut abgrenzbare, meist ovaläre Raumforderung. Je nach Anteil der zystischen Areale zeigen sich echoleere Anteile mit dorsaler Schallverstärkung. Der Tumor wird meist von Septen durchzogen, in denen Farb-Doppler-sonografisch häufig eine Hypervaskularisation nachgewiesen werden kann (▶ Abb. 8.16) [9]. Eine polyzyklische Begrenzung oder Ausbuchtungen der Tumorwand, wie sie beim pleomorphen Adenom häufig zu finden sind, fehlen meist beim Zystadenolymphom. Nach Gabe eines Kontrastverstärkers weisen Zystadenolymphome eine schnellere Abflutung des Kontrastverstärkers auf als pleomorphe Adenome [33]. In der Elastografie sind die pleomorphen Adenome meist dichter als die Zystadenolymphome, wie aufgrund der Histologie zu erwarten [1]. Allerdings sind die Variationsbreiten bei den sonomorphologischen Charakteristika beträchtlich, sodass eine sichere Unterscheidung zwischen pleomorphen Adenomen und Zystadenolymphomen mitunter nicht möglich ist. Als andere, seltenere Entitäten von monomorphen Adenomen treten in den Speicheldrüsen z. B. Onkozytome 8 oder Basalzelladenome auf. Sonografisch imponieren gut begrenzte, echoarme Läsionen mit oder ohne dorsale Schallverstärkung (▶ Abb. 8.17). Allerdings sind zurzeit keine für einzelne Tumorentitäten spezifischen Charakteristika bekannt, sodass ihre Unterscheidung meist nicht möglich ist und die Diagnose erst anhand einer zytologischen Untersuchung nach Feinnadelpunktion oder anhand des Operationspräparats gestellt wird [4] [19]. 8.5.3 Maligne Tumoren Maligne Tumoren der Speicheldrüsen machen etwa 20 % aller Tumoren in diesen Organen aus. Die häufigste Entität ist das Mukoepidermoidkarzinom, bei dem histologisch in Low-Grade- und High-Grade-Tumoren unterschieden wird. An 2. Stelle der Häufigkeit stehen Adenound adenoidzystische Karzinome, gefolgt von Azinuszellkarzinomen und Metastasen von Tumoren anderer Provenienz. Sehr selten sind primäre Plattenepithelkarzinome. Eine Sonderform ist das Karzinom im pleomorphen Adenom. Abb. 8.17 Basalzelladenom der Glandula parotis links. Der Tumor stellt sich als echoarme, relativ gut abgrenzbare Raumforderung mit dorsaler Schallverstärkung dar. Relativ homogenes Binnenecho. Allerdings sind diese Charakteristika unspezifisch. 104 Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. Ultraschalluntersuchung bei Erkrankungen der Kopfspeicheldrüsen Abb. 8.18 Adenokarzinom der Glandula parotis links. Der echoarme Tumor ist verhältnismäßig gut abgrenzbar; allerdings erscheinen die Randbezirke zum normalen Glandula-parotisParenchym etwas unscharf. Wenig Inhomogenitäten. Anhand dieses Bildes allein ist nicht zwischen einem malignen und einem benignen Tumor zu unterscheiden. ● RF = Raumforderung Die exakte Artdiagnostik aufgrund von sonografischen Charakteristika zu stellen, ist schwierig. Allgemein gelten schlechte Abgrenzbarkeit, irreguläre Form und heterogene Echotextur sowie Zeichen der Infitration von Haut oder Muskulatur als Malignitätskriterien [15] [31]. Diese Kriterien sind unspezifisch, denn auch maligne Tumoren können sich glatt begrenzt oder zystisch darstellen (▶ Abb. 8.18, ▶ Abb. 8.19 und ▶ Abb. 8.20). Ein homogenes Binnenecho oder ein mehr lobuliertes Binnenecho mit dorsaler Schallverstärkung, ähnlich einem pleomorphen Adenom, schließt einen malignen Tumor nicht aus. Abb. 8.19 Adenokarzinom der Glandula submandibularis rechts. In diesem Fall ist der Tumor relativ gut abgrenzbar. Das Echoverhalten ist echoarm mit Binnenechos, die jedoch nicht als spezifisch für ein Malignom angesehen werden können. ● RF = Raumforderung Das Mukoepidermoidkarzinom weist solide und zystische Areale mit dorsaler Schallverstärkung auf. Die Begrenzung ist, wie auch bei den meisten anderen malignen Speicheldrüsentumoren, unscharf und die Echotextur inhomogen (▶ Abb. 8.21). Farb-Doppler-sonografisch sind die Vaskularisierungsmuster der malignen Speicheldrüsentumoren meist uncharakteristisch (▶ Abb. 8.22); es liegen recht häufig Kaliberschwankungen der Gefäße vor und eine im Vergleich zu benignen Tumoren höhere Geschwindigkeit des systolischen Peak-Anstiegs in der FarbDoppler-Sonografie [11]. Insgesamt kann auch mittels derartiger semiquantitativer Parameter sonografisch weder eine sichere Unterscheidung zwischen benignen und 8 Abb. 8.20 Karzinom im pleomorphen Adenom der Glandula parotis links. Der Tumor ist an den Rändern unscharf begrenzt, mit Zeichen der Infiltration in das umgebende Glandula-parotis-Parenchym. Das Echoverhalten ist echoarm mit echokomplexen bzw. echoreicheren Anteilen. a Axiale Schallrichtung. b Longitudinale Schallrichtung. ● Parotis = Glandula parotis ● RF = Raumforderung 105 Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. 8.5 Tumoren der Speicheldrüsen Ultraschalluntersuchung bei Erkrankungen der Kopfspeicheldrüsen 8 Abb. 8.22 Adenokarzinom der Glandula parotis rechts. Der Tumor stellt sich echoarm mit relativ guter Abgrenzbarkeit und einzelnen Binnenechos dar. An den Rändern zum Parotisparenchym wird die Begrenzung etwas unscharf, ein Hinweis auf das infiltrierende Wachstum. In der Farb-Doppler-Sonografie gut erkennbar die Gefäße, die von der Peripherie zur Kapsel des Tumors ziehen. Innerhalb des Tumors einige Gefäße mit Kaliberschwankungen. Der Tumor weist eine bessere Vaskularisierung auf als z. B. ein pleomorphes Adenom. a Farb-Doppler-Sonografie. b B-Mode-Darstellung. ● RF = Raumforderung malignen Tumoren erfolgen noch können einzelne sonografische Kriterien spezifisch bestimmten histologischen Entitäten zugeordnet werden. Mit anderen bildgebenden Untersuchungsverfahren (MRT, CT) gelingt dies ebenfalls nicht [8] [26]. Anders als z. B. bei den Tumoren der Prostata hat die Elastografie bei den Speicheldrüsentumoren nach den bisher publizierten Untersuchungen keine eindeutigen Unterschiede zwischen malignen und benignen Neoplasien erbracht (▶ Abb. 8.23). Der Wert der Sonografie bei Verdacht auf das Vorliegen eines malignen Tumors besteht darin, den Tumor in seiner Ausdehnung und in seinen Nachbarschaftsbeziehungen zu identifizieren und mittels sonografisch gesteuerter Feinnadelpunktion unter visueller Kontrolle Material für die zytologische Untersuchung zu gewinnen. Darüber hi- 106 Abb. 8.23 Adenokarzinom der Glandula parotis rechts. Heterogenes Elastogramm des Tumors mit Arealen sehr hoher Gewebedichte (rot-braune Färbung) und Arealen von niedriger Gewebedichte (bläulich-graue Färbung). (Welkoborsky HJ. Aktuelle Aspekte der Ultraschalluntersuchung der Speicheldrüsen. HNO 2011; 59: 155–165, Fig. 10; with kind permission of Springer Science+Business Media) Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. Abb. 8.21 Mukoepidermoidkarzinom der Glandula parotis rechts. Der echoarme Tumor weist echokomplexere Anteile und zystische Areale mit dorsaler Schallverstärkung auf; er zeigt eine unscharfe Begrenzung zu dem umgebenden Glandulaparotis-Parenchym, mit Zeichen der Infiltration. Anhand des sonografischen Bildes allein kann nicht auf die Tumorentität zurückgeschlossen werden. ● RF = Raumforderung 8.5 Tumoren der Speicheldrüsen naus gestattet die Sonografie der Halsweichteile die Identifikation von Lymphknotenmetastasen. Ist der Tumor inframandibulär oder im tiefen Glandula-parotis-Lappen lokalisiert oder besteht der Verdacht auf das Vorliegen einer Infiltration der Schädelbasis, kann die Ausdehnung mittels Sonografie allein meist nur unzureichend bestimmt werden. In diesen Fällen ist dann eine zusätzliche CT- oder MRT-Untersuchung notwendig [5] [20]. Maligne Lymphome treten als Hodgkin- und NonHodgkin-Lymphome auf. Die befallenen Lymphknoten können sowohl intraglandulär (Glandula parotis) als auch periglandulär als extramedulläre Manifestationen auftreten. Sonografisch zeigen sich dann multiple, mehr runde als ovaläre, echoarme bis echoleere Raumforderungen sehr unterschiedlicher Größe, teilweise mit dorsaler Schallverstärkung. Sie weisen Farb-Doppler-sonografisch eine erhöhte Vaskularisation auf. Auch können meist noch weitere befallene Lymphknoten in der Umgebung der Drüsen oder in den Halsweichteilen nachgewiesen werden; dabei können alle anatomischen Regionen des Halses betroffen sein (▶ Abb. 8.24). Strahlentherapien führen zu sonografisch nachweisbaren strukturellen Veränderungen der Speicheldrüsen. Die Echogenität wechselt von homogen zu mehr heterogen mit echogleichen und echoarmen Arealen im Vergleich zu normalem Speicheldrüsenparenchym. Gleichzeitig nimmt der mittels Doppler-Ultraschall messbare Blutfluss ab (▶ Abb. 8.25) [32]. 8 Abb. 8.25 Zustand nach Parotidektomie links und Strahlentherapie bei Mukoepidermoidkarzinom. Die Glandula-parotisLoge ist unauffällig und ohne Nachweis von nodulären Strukturen. Es fällt eine stärkere Echogenität des Gewebes auf, die auf die Fibrosierung nach Strahlentherapie zurückzuführen ist. 8.5.4 Pseudotumoren der Speicheldrüsen Parotiszysten Bei den Speicheldrüsenzysten handelt es sich um keine Neoplasien im engeren Sinne. Sie sind den Pseudotumoren zuzuordnen. Die lymphoepitheliale Glandula-parotisZyste ist in manchen Fällen mit dem Vorliegen einer HIVInfektion (HIV = humanes Immunschwächevirus) assoziiert. Sonografisch zeigen sich echoarme bis echoleere, gut abgrenzbare, meist ovaläre Raumforderungen mit dorsaler Schallverstärkung (▶ Abb. 8.26). Intraläsional können, je nach Viskosität des Zysteninhalts, fein granulierte Binnenechos nachgewiesen werden, die durch Zelldetritus und Eiweißpräzipitate in der Zystenflüssigkeit hervor- Abb. 8.26 Glandula-parotis-Zyste rechts. Die Lasion ist gut abgrenzbar, echoarm bis echoleer mit feinen Binnenechos, die Zelldetritus und Eiweißpräzipitaten in der Zystenflüssigkeit entsprechen. Dorsale Schallverstärkung. Die Läsion ist wie alle zystischen Veränderungen kompressibel. ● zyst. RF = zystische Raumforderung 107 Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. Abb. 8.24 Malignes Lymphom im Bereich der Glandula-parotis-Loge links. Multiple echoarme, gut abgrenzbare, rundliche bis ovale intraglanduläre Lymphknoten. Kein Nachweis einer Hilusstruktur, allerdings Binnenchos. ● GP = Glandula parotis ● LK = Lymphom ● SCM = M. sternocleidomastoideus ● UK = Unterkiefer Ultraschalluntersuchung bei Erkrankungen der Kopfspeicheldrüsen gerufen werden. Diese Läsionen sind, wie alle zystischen Raumforderungen, kompressibel, d. h., sie ändern ihre Form von mehr rund zu ovalär, wenn Druck mit dem Schallkopf ausgeübt wird. Farb-Doppler-sonografisch finden sich keine Gefäße. Läuft der N. facialis durch die Zyste hindurch, so ist er als feine, echoreichere Struktur zu identifizieren. Differenzialdiagnostisch müssen alle benignen und malignen zystischen Strukturen in Betracht gezogen werden. Die Ranula ist eine Mukozele, die vornehmlich in der Glandula sublingualis auftritt. Sie erstreckt sich in den Mundboden und erreicht hier die submukösen Gewebeschichten. Dementsprechend stellt sich in der Umgebung der anterioren Mundbodenanteile eine echoarme bis echoleere, gut abgrenzbare, nicht vaskularisierte und kompressible Raumforderung mit dorsaler Schallverstärkung dar (▶ Abb. 8.27). Recht charakteristisch ist eine sanduhrförmige Form der Ranula. Sie entsteht, wenn sich die Zyste durch den M. mylohyoideus ausdehnt. Bei diagnostischen Unsicherheiten kann während der Sonografie von enoral palpiert werden. Musculus-masseter-Hypertrophie 8 Bei der Hypertrophie des M. masseter handelt es sich häufig um eine Folge von Dysgnathien, wie z. B. Knirschen, oder von Kiefergelenksveränderungen. Sie ist in der Regel beidseits ausgebildet. Klinisch imponiert eine Schwellung des lateralen Wangenbereichs. Sonografisch besteht eine Hypertrophie des Muskels medial der Glandula parotis (▶ Abb. 8.28). Die Drüse selbst ist unauffällig, mit normalem, homogenem Binnenecho, normaler Größe und Abgrenzbarkeit und ohne fokale Läsionen. Anhand des sonografischen Befunds kann somit die wichtigste Differenzialdiagnose der M.-masseter-Hypertrophie, nämlich eine Erkrankung der Glandula parotis, ausgeschlossen werden. Hämangiome Die Diagnose der Hämangiome ist eine Domäne der FarbDoppler-Sonografie. Kavernöse Hämangiome treten meist in der Kindheit auf und neigen zu spontaner Rück- Abb. 8.27 Ranula im Bereich des Mundbodens. In diesem Fall ist der Befund relativ klein und von enoral deutlich besser sichtbar als sonografisch. Es stellt sich eine echoarme, kompressible Raumforderung im vorderen Mundbodenbereich in der Gegend der Glandula sublingualis dar. Der M. mylohyoideus wird nicht überschritten. In diesem Fall gelingt die sonografische Darstellung besser mithilfe einer enoralen Sonografie. bildung. Sonografisch kommen Hämangiome als echoarme Raumforderungen mit heterogener Echotextur zur Darstellung. Sie sind oft schlecht gegenüber dem umgebenden Gewebe abzugrenzen. Innerhalb der Läsionen sind häufig Kalzifikationen sowie dilatierte Gefäße sichtbar. Farb-Doppler-sonografisch zeigt sich eine Hypervaskularisierung mit Shunt-Gefäßen. Präaurikuläre Raumforderungen Präaurikuläre Raumforderungen können einen Tumor der Glandula parotis vortäuschen. Histologisch handelt es sich um Atherome, Zysten, Dermoide oder Gehörgangsduplikaturen. Sonografisch stellen sich glatt begrenzte, echoarme Raumforderungen mit dorsaler Schallverstärkung dar. Häufig finden sich feine Binnenechos in den Läsionen, die abgeschilferten Epithelien entsprechen können oder einen hohen Eiweißanteil der Zystenflüssigkeit anzeigen. Anhand der Sonografie kann einerseits die Beziehung zum Speicheldrüsenparenchym und andererseits die Ausdehnung der Läsion sowie ihre Lagebeziehung z. B. zum Gehörgang beurteilt werden (▶ Abb. 8.29). Abb. 8.28 M.-masseter-Hypertrophie. Der M. masseter ist medial der Drüse zu erkennen und deutlich hyperplastisch. Die Drüse selbst ist unauffällig. ● cran. = kranial ● Gl. parotis = Glandula parotis ● med. = medial ● M. mass. = M. masseter 108 Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. Ranula 8.5 Tumoren der Speicheldrüsen Literatur [1] Bhatia KS, Rasalkar DD, Lee YP et al. Evaluation of real-time qualitative sonoelastography of focal lesions in the parotid and submandibular glands: applications and limitations. Eur Radiol 2011; 20: 1958–1964 [2] Bialek EJ, Jakubowski W, Zajkowski P et al. US of the major salivary glands: anatomy and spatial relationships, pathologic conditions, and pitfalls. Radiografics 2006; 26: 745–763 [3] Bozzato A, Hertel V, Bumm K et al. Salivary stimulation with ascorbic acid enhances sonografic diagnosis of obstructive sialadenitis. J Clin Ultrasound 2009; 37: 329–332 [4] Brennan PA, Davies B, Poller D et al. Fine needle aspiration cytology (FNAC) of salivary gland tumours: repeat aspiration provides further information in cases with an unclear initial cytological diagnosis. Br J Oral Maxillofac Surg 2010; 48: 26–29 [5] Capaccio P, Cuccarini V, Ottaviani F et al. Comparative ultrasonografic, magnetic resonance sialografic, and videoendoscopic assessment of salivary duct disorders. Ann Otol Rhinol Laryngol 2008; 117: 245– 252 [6] Chikui T, Tokumori K, Yoshiura K et al. Sonografic texture characterization of salivary gland tumors by fractal analysis. Ultrasound Med Biol 2005; 31: 1297–1304 [7] Chouw TL, Chan TT, Choi CY et al. Kuttner‘s tumor (chronic sclerosing sialadenitis) of the submandibular gland: a clinical perspective. Hong Kong Med J 2008; 14: 46–49 [8] De Ru JA, van Leeuwen MS, van Benthem PP et al. Do magnetic resonance imaging and ultrasound add anything to the preoperative workup of parotid gland tumors? J Oral Maxillofac Surg 2007; 65: 945–952 [9] Fischer T, Paschen CF, Slowinski T et al. Differentiation of parotid gland tumors with contrast-enhanced ultrasound. Rofo 2010; 182: 155–162 [10] Fraser L, Moore P, Kubba H. Atypical mycobacterial infection of the head and neck in children: a 5-year retrospective review. Otolaryngol Head Neck Surg 2008; 138: 311–314 [11] Gallipoli A, Manganella G, De Lutiodi di Castelguidone E et al. Ultrasound contrast media in the study of salivary gland tumors. Anticancer Res 2005; 25: 2477–2482 [12] Geisthoff UW, Maune S. Ultrasound-guided mechanical fragmentation of sialoliths (sonoguide forceps). Head Neck 2010; 32: 1641–1647 [13] Geisthoff UW, Lehnert BK, Verse T. Ultrasound-guided mechanical intraductal stone fragmentation and removal for sialolithiasis: an new technique. Surg Endosc 2006; 20: 690–694 [14] Gritzmann N. Ultraschall der Speicheldrüsen. Laryngorhinootologie 2009; 88: 48–56 [15] Jecker P, Orloff LA. Salivary gland ultrasonography. In: Orloff LA, ed. Head and neck ultrasonography. San Diego: Plural Publishing; 2008: 129–152 [16] Katz P, Hartl DM, Guerre A. Clinical ultrasound of the salivary glands. Otolaryngol Clin North Am 2009; 42: 973–1000 [17] Koch M, Iro H, Zenk J. Sialendoscopy-based diagnosis and classification of parotid duct stenosis. Laryngoscope 2009; 119: 1696–1703 [18] Koch M, Bozzato A, Iro H et al. Combined endoscopic and transcutaneous approach for parotid gland sialolithiasis: indications, technique, and results. Otolaryngol Head Neck Surg 2010; 142: 98–103 [19] Kraft M, Lang F, Mihaescu A et al. Evaluation of clinician-operated sonography and fine-needle aspiration in the assessment of salivary gland tumors. Clin Otolaryngol 2008; 33: 18–24 [20] Lee YY, Wong KT, King AD et al. Imaging of salivary gland tumors. Eur J Radiol 2008; 66: 419–436 [21] Milic VD, Petrovic RR, Boricic IV et al. Diagnostic value of salivary gland ultrasonografic scoring system in primary Sjögren‘s syndrome: a comparison with scintigraphy and biopsy. J Rheumatol 2009; 36: 1495–1500 [22] Milic VD, Petrovic RR, Boricic IV et al. Major salivary gland sonography in Sjögren‘s syndrome: diagnostic value of a novel ultrasonography score (0–12) for parenchymal inhomogeneity. Scan J Rheumatol 2010; 39: 160–166 [23] Munck K, Mandpe AH. Mycobacterial infections of the head and neck. Otolaryngol Clin North Am 2003; 36: 569–576 [24] Obinata K, Sato T, Ohmori K et al. A comparison of diagnostic tools for Sjögren syndrome, with emphasis on sialography, histopathology, and ultrasonography. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2010; 109: 129–134 [25] Poul JH, Brown JE, Davies J. Retrospective study of the effectiveness of high-resolution ultrasound compared with sialography in the diagnosis of Sjögren‘s syndrome. Dentomaxillofac Radiol 2008; 37: 392– 397 [26] Rudack C, Jörg S, Kloska S et al. Neither MRI, CT nor US is superior to diagnose tumors in the salivary glands – an extended case study. Head Face Med 2007; 3: 19 [27] Takagi Y, Kimura Y, Nakamura H et al. Salivary gland ultrasonography: Can it be an alternative to sialography as an imaging modality for Sjögren‘s syndrome? Ann Rheum Dis 2010; 69: 1321–1324 [28] Teymoortash A, Werner JA. Parotid gland involvement in sarcoidosis: sonografic features. J Clin Ultrasound 2009; 37: 507–510 [29] Tzioufas AG, Moutsopoulos HM. Ultrasonography of salivary glands: an evolving approach for the diagnosis of Sjögren‘s syndrome. Nat Clin Pract Rheumatol 2008; 4: 454–455 [30] Welkoborsky HJ. Ultrasound usage in the head and neck surgeon‘s office. Curr Opin Otolaryngol Head Neck Surg 2009; 17: 116–121 [31] Welkoborsky HJ. Aktuelle Aspekte der Ultraschalluntersuchung der Speicheldrüsen. HNO 2011; 59: 155–165 [32] Ying M, Wu VW, Kwong DL. Comparison of sonografic appearance of normal and postradiotherapy parotid glands: a preliminary study. Ultrasound Med Biol 2007; 33: 1244–1250 [33] Yuan WH, Hsu HC, Chou YH et al. Gray scale and color Doppler ultrasonografic features of pleomorphic adenoma and Warthin‘s tumor in major salivary glands. Clin Imaging 2009; 33: 348–353 [34] Zengel P, Siedek V, Berghaus A et al. Intraductally applied contrastenhanced ultrasound (IA-CEUS) for improved visualization of obstructive diseases of the salivary glands, primary results. Clin Hemorheol Microcirc 2010; 45: 193–205 [35] Zenk J, Iro H, Klintworth N et al. Diagnostic imaging in sialadenitis. Oral Maxillofac Surg Clin North Am 2009; 21: 275–292 8 109 Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. Abb. 8.29 Präaurikuläre Zyste. Das Glandula-parotis-Parenchym stellt sich unauffällig dar. Es besteht keine Beziehung zwischen Raumforderung und Drüsenparenchym. Die Raumforderung ist kompressibel, septiert, mehrkammerig und nahezu echoleer mit feinen Binnenechos. Es liegt eine dorsale Schallverstärkung als Zeichen für den hohen Wassergehalt des Zysteninhalts vor.