Document
Werbung

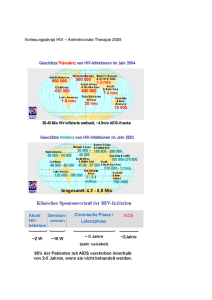
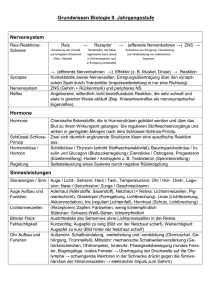
9. Beschreibung der AIDS Problemattik am Beispiel Afrika! a. Verbreitung) Aus epidemiologischer Sicht ist das weltweite Verteilungsmuster von HIV interessant: Während sich die meisten Viren gleichmäßig schnell ausbreiten, war dies bei HIV anders. Während die HIV-Epidemie in den USA bereits vor 20 Jahren begann, gab es einige Länder, die von HIV verschont zu sein schienen, dann aber mit großer Geschwindigkeit vom Virus erobert wurden. So geschah es vor allem in Osteuropa und Asien Mitte der 1990er Jahre. In anderen Ländern, zum Beispiel Kamerun, blieb die Prävalenz von HIV Jahre lang stabil, um dann sprunghaft anzusteigen. Auch eine Obergrenze in der HIV_-Prävalenz scheint es nicht zu geben. So stieg die Quote der schwangeren Frauen mit HIV in städtischen Zentren in Botswana nach 1997 in vier Jahren von 38,5 % auf 55,6 %. Dass HIV erfolgreich zu bekämpfen ist, zeigt das Beispiel Uganda. 1992 lag die Prävalenz von HIV bei schwangeren Frauen bei nahezu 30 % und konnte auf 10 % im Jahre 2000 gesenkt werden. Grundlagen dieses Erfolges waren die landesweite Einführung von Sexualkundeunterricht, flächendeckende Kampagnen zur Steigerung der Akzeptanz von Kondomen, HIV-Tests, deren Ergebnisse noch am selben Tag bekannt gegeben wurden und Selbsthilfe-Kits für sexuell übetragbare Krankheiten. Diese Erfolge sind jedoch nur mit finanziellen Mitteln durchführbar, die viele der Hochendemie-Länder in Afrika nicht allein aufbringen können. Unabdingbar ist ferner ebenso ein politischer Wille, diese Seuche aktiv zu bekämpfen. Weltweit Mit HIV/Aids lebende Personen Neuinfektionen Todesfälle Todesfälle aufsummiert Quelle 1980 (~ 2.000.000)1 1993 (12.900.000)1 (2.500.000)1 1999 4.000.000 2000 3.800.000 2001 34.900.000 (40.000.000)1 3.400.000 2.500.000 20 - 22 Mio 2002 - (42.000.000)1 3.500.000 3.100.000 ~ 21.1 Mio 2003 37.800.000 4.800.000 2.900.000 ~ 24.0 Mio 2004 39.400.000 4.900.000 3.100.000 ~ 27.1 Mio 2005 40.300.000 4.900.000 3.100.000 > 25 Mio Aids epidemic update December 2005 (UNAIDS) 2006 38.600.000 4.100.000 3.100.000 > 25 Mio c) Aids Prävention, Bildung, Generika Ansteckungswahrscheinlichkeit Die Infektionswahrscheinlichkeit liegt bei den meisten Übertragungswegen zwischen 1:100 und 1:1000. Wichtigste Ausnahme ist die Übertragung von der Mutter auf das Kind während der Geburt mit einer Infektionswahrscheinlichkeit von ca. 15 % und durch eine verseuchte Bluttransfusion, wo das Infektionsrisiko 95 % beträgt. Die folgenden Häufigkeiten sind Durchschnittswerte, die durch Partnerstudien und epidemiologische Studien ermittelt wurden. Das individuelle Risiko kann sehr viel höher sein. So erhöht eine gleichzeitig vorliegende andere Geschlechtserkerkrankung das Infektionsrisiko um das 5- bis 10-fache, eine hohe Viruslast des Überträgers sogar um das 10- bis 30-fache. Geschlechtsverkehr während der Regelblutung der Frau ist mit einem erhöhten Infektionsrisiko für beide Partner verbunden, beschnittene Männer haben ein geringeres Infektionsrisiko. Insgesamt scheint das Infektionsrisiko nicht konstant über die Anzahl der Kontakte zu sein, so dass das Risiko einzelner Kontakte womöglich erheblich zu niedrig angegeben ist. Mit besseren Medikamenten sinkt möglicherweise das Übertragungsrisiko. • Ungeschützter vaginaler Geschlechtsverkehr mit einem HIV-positiven Partner ist mit einem Risiko einer HIV-Infektion von ca. 0,05 - 0,15 % für die Frau, und zwischen 0,03 - 5,6 % für Männer verbunden, tendenziell jedoch für Männer etwas geringer als für Frauen. • Das Infektionsrisiko für Oralverkehr beim Mann, bei dem Sperma in den Mund aufgenommen wird, ist geringer, eine Infektion ist jedoch nicht ausgeschlossen. Eine Infektion durch Vorflüssigkeit („Lusttropfen“) ist sehr unwahrscheinlich. Bei Oralverkehr bei der Frau wird das Risiko ebenfalls als geringer als beim vaginalen Geschlechtsverkehr angesehen. Auch das Risiko beim sogenannten Rimming wird als äußerst gering eingeschätzt. • Bei Analverkehr treten häufig kleine Risse an der Schleimhaut auf. Dementsprechend liegt das Risiko für den passiven Teilnehmer beim Analverkehr um 0,8 % und um 0,3 % für den aktiven Teilnehmer. • Andere Sexualpraktiken, bei denen kein Kontakt zu Schleimhäuten, Blut, Sperma oder Vaginalsekret besteht, haben ein extrem geringes Infektionsrisiko. • Das Infektionsrisiko durch Nadelstiche hängt sehr von der Situation ab. Das Infektionsrisiko wird durchschnittlich mit 0,3 % angegeben und steigt mit folgenden Faktoren: sehr tiefe Verletzungen (16-fach erhöht), sichtbare Blutspuren auf der Nadel oder Nadel war vorher in einer Vene oder Arterie des Überträgers (jeweils 5-fach erhöht), bei hoher Viruslast des Überträgers (6fach erhöht). Das Risiko bei Hohlnadeln ist höher als bei geschlossenen Nadeln. • Das Risiko, sich bei gemeinsamer Benutzung einer Kanüle , meist beim Spritzen von Heroin , zu infizieren, liegt um 0,7 % und sinkt mit dem zeitlichen Abstand zwischen den Injektionen, allerdings nur langsam, da in der Kanüle eingeschlossene Viren lange infektiös bleiben können, teilweise auch noch nach Tagen. Ein Auskochen der Nadeln ist zwar generell möglich, wenn es lange genug durchgeführt wird, allerdings sind handelsübliche Nadeln nicht dafür geeignet, weil die verwendeten Kunststoffe nicht entsprechend hitzefest sind. Eine chemische Desinfektion (Alkohol oder andereDesinfektionsmittel) ist nicht ausreichend, weil nicht gewährleistet ist, dass die Substanzen ganz in die Kanüle eindringen. Teilweise besteht die Möglichkeit einer Postexpositionsprophylaxe. Diese besteht aus allgemeinen Maßnahmen (Waschen des Penis nach dem Verkehr, Ausdrücken der Stichwunden und Behandlung mit Desinfektionsmittel) und spezifischen Maßnahmen wie der Gabe von antiretroviralen Medikamenten. Nach einem Ansteckungsverdacht sollte immer sofort ein Arzt aufgesucht werden, der über mögliche Maßnahmen informiert und diese auch einleiten kann. Untersuchung HIV-Test Der Begriff HIV-Test steht für den HIV-Antikörper-Test, der die An- oder Abwesenheit von Antikörpern gegen HIV-Proteine, nicht jedoch das HI-Virus selbst nachweist. Wie gegen andere als „körperfremd“ erkannte Eiweißmoleküle bildet das Immunsystem Antikörper, um sich vor eingedrungenen HI-Viren zu schützen. Sind Antikörper vorhanden, ist der Test „HIV-positiv“, d. h. es hat ein Kontakt mit dem HI-Virus stattgefunden. Werden keine Antikörper nachgewiesen, lautet das Resultat des Testes „HIV-negativ“. Ein Problem beim HIV-Antikörper-Test ist die diagnostische Lücke: In der Zeit, die der Körper braucht, um die ersten Antikörper zu bilden, können solche auch nicht nachgewiesen werden und führen somit zu einem „falsch-negativen“ Ergebnis. Die heute üblichen Tests können in der Regel zwölf Wochen nach der Ansteckung zuverlässig Antikörper nachweisen; 99 % der Infizierten weisen dann bereits Antikörper auf. In den meisten Fällen ist ein Kontakt mit HI-Viren bereits nach drei bis sechs Wochen feststellbar. In seltenen Fällen können aber noch Monate später falsche, auch negative Ergebnisse entstehen. Grundsätzlich gilt: Je länger der Zeitraum zwischen möglicher Ansteckung und Test, um so größer ist seine Aussagekraft. In Deutschland wird die Diagnose „HIV-positiv“ durch zwei Tests gestellt: einen Suchtest und einen Bestätigungstest. Als Suchtest wird meist ein kostengünstiger HIV-Elisa-Test durchgeführt. Dieser weist das p24-Antigen sowie Antikörper gegen HIV-1, HIV-2 und HIV-1 Subtyp 0 im Blut nach (sog. HIV-Test der vierten Generation). Für diesen Test werden von kommerziellen Herstellern Virusproteine in so genannten ElisaTestplatten vertrieben. Eine Testplatte besteht aus bis zu 96 kleinen Näpfen, in denen die HIV-Proteine auf dem Trägermaterial fixiert wurden. Von der zu testenden Blutprobe werden die Blutzellen abgetrennt und die verbleibende gelblich-klare Flüssigkeit, das so genannte Serum, in eines der Näpfchen der Testplatte gegeben. Wenn Antikörper im Serum vorliegen, die vom Immunsystem eines HIV-Infizierten gebildet wurden, heften diese sich an die HIV-Proteine. Nach weiteren Arbeitsschritten verbleibt in den Näpfen von HIVnegativen Personen eine glasklare Flüssigkeit und bei HIV-infizierten Menschen eine gefärbte Flüssigkeit. Der Test wird maschinell und immer im Vergleich zu HIV-positiven und HIV-negativen standardisierten Seren abgelesen. Der HIV-Suchtest ist auch in großen klinisch-chemischen Laborautomaten durchführbar. Es wird dann ein etwas abweichendes Verfahren eingesetzt, der Elektrochemilumineszenz-Immunoassay (ECLIA). Aussagekraft und Beschränkungen sind aber dem ELISA vergleichbar. Der Einsatz dieser Suchtests ist ab etwa zwei bis drei Wochen nach möglicher Exposition sinnvoll. Ein sehr zuverlässiges Testergebnis ist allerdings erst 3 Monate nach einem Risikokontakt zu erwarten. Die Tests arbeiten mit hoher Sensitivität, um auch sehr kleine Mengen vorhandene Antikörper zu entdecken. Allerdings sind die dergestalt gefundenen Antikörper keine eindeutige Bestätigung einer HIV-Infektion, so dass nach einem „reaktiven“ Testergebnis grundsätzlich ein so genannter Bestätigungstest durchgeführt wird. Als routinemäßiger Bestätigungstest dient die aufwändigere Western-BlotMethode (genauer gesagt Immunoblot), ebenfalls ein Antikörpertest. Hierzu wird eine Reihe unterschiedlicher HIV-Proteine auf einen Teststreifen als Trägermaterial nebeneinander aufgebracht. Der Streifen wird in eine weitere Serumprobe eingelegt. Wenn Antikörper gegen HIV vorhanden sind, heften sich diese an die Virusproteine. Nach weiteren Arbeitsschritten werden dunkle Striche auf dem Teststreifen sichtbar. Sie zeigen an, gegen welche Virusproteine der Mensch Antikörper gebildet hat. Nach WHO-Empfehlung wird die Diagnose 'HIV-positiv' auf Grund von Antikörpern gegen zwei verschiedene Virusproteine gestellt. Auf diese Weise wird der zuvor positive oder grenzwertige Suchtest widerlegt oder bestätigt. Zur Sicherung der Diagnose existieren weiterführende Tests, die nicht nur HIVAntikörper, sondern das HI-Virus selbst nachweisen können, etwa durch Nachweis viraler Nukleinsäuren. Über die HIV-RNA lässt sich die Virus-„Menge“ messen. Mittlerweile werden zunehmend auch solche Nachweismethoden zum diagnostischen Standard, welche Resistenzen in den Virusstämmen gegen antiretrovirale Therapien anzeigen. In der Frühphase der HIV-Infektion kann zudem der Nachweis des p24-Antigens durch einen ELISA hilfreich sein. Die Sensitivität des HIV-Test wird mit 99,9 % angegeben. Dies bedeutet, dass von 1000 HIV-positiven Patienten 999 als solche erkannt werden und einer ein falsch-negatives Ergebnis erhält. Die Spezifität beträgt 99,8 %. Dies bedeutet, dass von 1000 nicht HIV-Positiven 998 ein negatives Ergebnis erhalten und 2 ein falsch-positives Ergebnis . Der positive prädiktive Wert, also die Wahrscheinlichkeit, dass eine Person mit positivem Test wirklich infiziert ist, hängt von der Prävalenz in der getesteten Gruppe ab und kann somit nicht allgemein angegeben werden. Bei niedriger Prävalenz, wie z. B. bei Personen ohne Risikofaktoren liegt er deutlich unter der Spezifität, bei unter 50%. Liegen hingegen Risikofaktoren vor, steigt der Wert schnell an und erreicht Werte nahe der Spezifität. (zur Bewertung eines Testergebnisses siehe auch: Beurteilung eines Klassifikators). Direkt nachgewiesen werden HI-Viren bzw. die Virus-RNA durch das vergleichsweise kostenintensive RT-PCR-Verfahren. Diese Methode wird meist nach gestellter Diagnose zur Bestimmung der Viruslast angewandt. Bei Neugeborenen hat ein Antikörper-Test keine Aussagekraft, da die IgGAntikörper der Mutter durch die Plazenta in das Blut des Kindes gehen, und daher ein falsch positives Testergebnis entsteht. Kommerziell erhältliche Tests zum Nachweis von IgM- oder IgA-Antikörpern, welche vom Kind gebildet werden, sind noch nicht vorhanden. Daher ist die gängige Untersuchungsmethode bei Neugeborenen und Säuglingen die RT-PCR. Zur Diagnostik einer akuten HIV Infektion dient ein positiver HIV-RNA Test durch eine RT-PCR und ein negativer oder „grenzwertiger“ Bestätigungstest. Therapie Durch eine antiretrovirale Therapie (ART), d. h. die Einnahme von HIVunterdrückenden Medikamenten, und Behandlung von Sekundärinfektionen kann der Krankheitsverlauf verlangsamt werden. Da das Virus schnell Resistenzen gegenüber einzelnen Medikamenten entwickelt, hat sich die Therapie durch gleichzeitige Einnahme mehrerer Medikamente durchgesetzt, die sogenannte „Highly Active Antiretroviral Treatment“ (HAART). Antiretrovirale Therapie kann die Lebenserwartung HI-Infizierter deutlich verlängern, jedoch keine vollständige Eradikation des Virus – und damit eine Heilung – bewirken. Zudem können schwerwiegende Nebenwirkungen auftreten. Eine einmal begonnene ART sollte nicht mehr abgesetzt werden, um Resistenzbildung zu verhindern. Aus dem selben Grund ist eine regelmäßige Tabletteneinnahme unumgänglich (siehe Adherence). Daraus ergibt sich eine hohe Belastung für den Patienten. Zur Zeit werden drei Wirkstoffklassen angewandt: Nukleosid- und Nukleotidanaloga (NRTI), Nichtnukleosidische Reverse-Transkriptase-Inhibitoren (NNRTI) und Protease-Inhibitoren (PI). Eine weitere Wirkstoffklasse stellen Fusionsinhibitoren wie die Substanz T-20 dar. Nukleosidanaloga (NRTI) Nukleosidanaloga, auch Nukleosidische Reverse-Transkriptase-Inhibitoren (NRTI, umgangssprachlich „Nukes“) genannt, setzen an der reversen Transkriptase an, einem Enzym des HI-Virus, das das virale RNA-Genom in doppelsträngige DNA „übersetzt“. Anschließend baut ein weiteres virales Enzym, die Integrase, diese Virus-DNA in die DNA der Wirtzelle ein. Die NRTI stellen hierbei ein alternatives Substrat dar, die mit den physiologischen Nukleosiden konkurrieren, sich von diesen jedoch durch ein verändertes Zuckermolekül unterscheiden. Der Einbau der NRTI behindert die Struktur der Doppelstrangbindung und führt daher zu Kettenabbrüchen in der Virus-DNA. Hierbei entsprechen die Wirkstoffe Zidovudin (Azidothymidin, AZT) und Lamivudin (d4T) dem DNA-Baustein Thymidin, Zalcitabin (DDC) und Lamivudin (3TC) dem Cytidin, während Didanosin (DDI) analog zu Inosin und Abacavir ein Guanosin-Anologon ist. Eine Kombination von Analoga mit gleichem Ansatzpunkt (etwa AZT und d4T) ist nicht sinnvoll. Zahlreiche Nebenwirkungen können bei der Therapie mit NRTI auftreten. Häufig sind Kopfschmerzen, gastrointestinale Beschwerden, Völlegefühl oder Übelkeit, Erbrechen und Diarrhoeen, sowie allgemeine Müdigkeit. Als Folge längerer Anwendung kann es zur Laktatazidose, Myelotoxizität, Polyneuropathie und Pankreatiden kommen. Auch eine Lipodystrophie, eine auch bei Therapie mit Protease-Inhibitoren zu beobachtende eine Umlagerung von Körperfett, kann bei längerer Einnahme von NRTI auftreten. Viele dieser Nebenwirkungen sind eine Folge der mitochondralen Toxizität: Mitochondrien, die lebenswichtigen Kraftwerke der Zellen, benötigen ebenfalls Nukleoside. Durch den Einbau von NRTI statt Nukleosiden kommt es zu Stoffwechselstörungen und zur Degeneration der Mitochondrien. Bei der Toxizität der einzelnen Substrate gibt es erhebliche Unterschiede. NRTI werden unverändert in die Zelle aufgenommen und dort durch Phosphorylierung aktiviert. Sie werden überwiegend renal eliminiert und haben daher wenig Wechselwirkung mit Medikamenten, die in der Leber verstoffwechselt werden. PMID 10509516 Nicht-Nukleosidische Reverse-Transkriptase-Inhibitoren (NNRTI) Während NRTIs als „falsche“ Bausteine die reverse Transkriptase hemmen, binden NNRTIs direkt an dieses Enzym, nahe der Substratbindungsstelle für Nukleoside. Zurzeit gibt es drei NNRTis auf dem Markt: Neverapin, Delavirdin und Efavirenz. Während Nevirapin und Efavirenz etwa gleich effektiv sind, spielt Delaviridin in der Therapie kaum eine Rolle und ist in Deutschland (noch) nicht zugelassen. Als Einzelsubstanz zeigen NNRTIs nur eine begrenzte Wirkung, in Kombinationstherapie mit 2 NRTIs sind sie aus immunologisch-virologischer Sicht mit Proteaseinhibitoren gleichwertig. Jedoch gibt es bisher keine Studie, die den klinischen Effekt der NNRTIs – längeres und gesünderes Leben bei höherer Lebensqualität – nachweist. Zur Zulassung wurden ausschließlich Studien zu verbesserten CD4+ Zellzahlen und zur niedrigeren Viruslast benutzt (Surrogatmarker-Studien). Durch ihre gute Verträglichkeit und die geringere Pillenzahl werden sie häufig den Proteaseinhibitoren vorgezogen. NNRTIs sind recht empfindlich: Schon eine Punktmutation genügt, um eine Resistenz des Virus gegen den Wirkstoff zu erzeugen. Zudem bestehen Kreuzresistenzen: Zeigt ein Virus Resistenzen gegen einen NNRTI, so sind meist alle NNRTIs wirkungslos. NNRTIs werden in der Leber verstoffwechselt (Cytochrom P450System). Die Nebenwirkungsprofile der einzelnen Wirkstoffe unterscheiden sich erheblich. Bei der Therapie mit Nevirapin stehen vor allem allergische Reaktionen und Lebertoxizität im Vordergrund. Ein Exanthem tritt bei bis zu 20% der Patienten auf und führt bei 7 % zum Abbruch der Nevirapineinnahme. Um die Gefahr von Allergien zu mindern, sollte Nevirapin mit zunächst geringer Dosierung eingeschlichen werden. Lebertoxizität ist eine seltene, aber unter Umständen lebensbedrohliche Nebenwirkung von Nevirapin. Daher sollten zur Beginn der Therapie die Leberwerte (vor allem Transaminase) engmaschig kontrolliert werden. Die Nebenwirkungen von Efavirenz betreffen hingegen vor allem das zentrale Nervensystem. Sie treten meist zur Beginn der Therapie auf und schwächen sich danach ab. In den ersten vier Wochen in einer Studie traten bei 2/3 der Patienten Schwindel, nahezu der Hälfte Albträume und bei etwa einem Drittel der Patienten Benommenheit und Schlafstörungen auf. Diese nahmen aber meist nach einiger Zeit ab. Während Nevirapin zur Vorbeugung einer Mutter-zu-KindÜbertragung (PMTCT = Prevention of Mother to Child Transmission) eingesetzt wird, ist Efivarenz in der Schwangerschaft kontraindiziert. Angesichts der Wirkung auf das zentrale Nervensystem ist die Verkehrstauglichkeit fraglich. Ein Vorteil von Efavirenz gegenüber Nevirapin ist die geringere Lebertoxizität. Delavirdin ist wegen der hohen Pillenzahl und der dreimal täglichen Einnahme den anderen Wirkstoffen unterlegen. Zudem ist es zurzeit nicht auf dem deutschen Markt zugelassen. PMID 11590519 PMID 11873073 Proteaseinhibitoren (PI) Kann das HIV-Enzym Protease das virale Makromolekül gag-pol-Polyprotein nicht spalten, so werden nicht-infektiöse Viruspartikel produziert. Proteaseinhibitoren wurden mit dem Wissen über die molekulare Struktur des Enzyms so modelliert, dass sie direkt im aktiven Zentrum der Protease binden können. Die gute Wirksamkeit von Proteaseinhibitoren wurde anhand von klinischen Endpunkten nachgewiesen. Sie haben zu einer deutlichen Verbesserung der Therapie beigetragen. Bei der Langzeitbehandlung zeigen sich jedoch einige Probleme, die zu Störungen im Fettstoffwechsel führen und in Folge Lipodystrophie und Dyslipidämie auslösen können. Der Grund liegt wahrscheinlich in der mitochondrialen Toxizität, da Proteaseinhibitoren offenbar ähnlich den NRTI die Mitochondrien schädigen. Weitere Nebenwirkungen sind gastrointestinale Beschwerden. Proteaseinhibitoren haben relativ kurze Halbwertszeiten im Blutplasma. Schon nach acht Stunden ist die minimale Hemmkonzentration erreicht. Daher müssen die meisten Proteaseinhibitoren 3-mal täglich eingenommen werden. Der Abbau der Proteaseinhibitoren geschieht in der Leber durch das CytochromP450-Enzymsystem. Der Proteaseinhibitor Ritonavir hemmt dieses System. Man ging daher dazu über, andere Proteaseinhibitoren zusammen mit Ritonavir zu verabreichen, um den Abbau zu verlangsamen und die Plasma-Halbwertszeit zu verlängern. Dies wird als „Booster“ bezeichnet. Mittlerweile gibt es den Proteaseinhibitor Lopinavir kombiniert mit einer Boosterdosis Ritonavir (Kaletra). Dies führt zu einer fast 100-fach größeren Plasma-Konzentration von Lopinavir und zu einer größeren Barriere gegen Resistenzen. Daher wird Lopinavir/Ritonavir (Kaletra) zumeist nach Therapieversagen anderer Medikamente benutzt („Salvage-Bereich“). PMID 10860901 PMID 9287227 PMID 10202827 PMID 10509516 PMID 9835517 Fusionsinhibitoren Anfang 2003 wurde der erste Fusionsinhibitor T-20 auf den Markt gebracht. T-20 bindet an das für die Fusion des Virus mit der Zellmembran der T-Helferzellen wichtige Transmembranprotein gp41 und blockiert so den Eintritt des Virus in die Zelle. Besonders interessant wird die Substanz dadurch, dass sie keine mitochondriale Toxizität und damit kein Lipodystrophiesyndrom auslöst. T-20 ist mit seinen 36 Aminosäuren zu groß für eine orale Einnahme. In seiner jetzigen Form muss T-20 täglich subkutan gespritzt oder über eine „Insulinpumpe“ verabreicht werden. Als Nebenwirkung treten häufig Hautirritationen an der Einstichstelle auf. Erste Studien ergaben, dass die eine bloße Hinzugabe von T-20 zu einer klassischen antiretroviralen Therapie nur einen begrenzten Erfolg mit sich bringt. Zwei große Studien, die T-20 zu einer optimierten HAART gegen eine optimierte HAART ohne T-20 verglichen, zeigte jedoch signifikant bessere Werte im T-20-Arm der Studie. Das lässt darauf schließen, dass besonders diejenigen Patienten von T-20 profitieren, die gleichzeitig auch noch andere medikamentöse Optionen haben.[6] T-20 kann offenbar zu Interaktionen mit Granulozyten führen, die bei einigen Patienten zu vermehrten Infektionen führten. Eine rasche Resistenzbildung des Virus ist zudem recht wahrscheinlich. Jedoch scheint die virale Fitness der resistenten Stämme vermindert zu sein. Dennoch ermöglicht T-20 Patienten eine Option, die auf Grund von Nebenwirkungen oder Resistenzen ihre Therapie umstellen müssen. Erste Wahl zu Therapiebeginn ist T-20 derzeit jedoch nicht, und das nicht nur auf Grund der Studienlage. T-20 ist nach Aussage der Herstellerfirma Hoffmann-La Roche einer der am aufwändigsten zu produzierenden Substanzen der Firmengeschichte. Dies macht sich im Preis deutlich, der mit über €24.000 pro Jahr höher als einige Dreifachkombinationen herkömmlicher antiretroviraler Medikamente liegt. An anderen Fusionsinhibitoren und an einer wöchentlich zu verabreichenden T-20Injektion wird geforscht. Eine Sammlung mit übersichtlichen Beschreibungen aller zur Zeit angewandten antiretroviralen Therapeutika sowie einiger gängiger Medikamente zur Behandlungen opportunistischer Infektionen findet sich unter HIV.NET. Highly Active Antiretroviral Therapy (HAART) Mit highly active antiretroviral therapy wird die Kombinationstherapie aus mehreren antiretroviralen Medikamenten bezeichnet. Ziel der Therapie ist es, die Viruslast unter die Nachweisgrenze zu drücken und die CD4-Zellwerte zu erhöhen, um so das Immunsystem gegen opportunistische Infektionen und andere Aids-definierende Erkrankungen zu stärken. In der Regel besteht eine HAART aus 2 verschiedenen Nukleosidanaloga (NRTI, auch als „Nuke-Backbone“ der Therapie bezeichnet) plus entweder einem Nicht- nukleosidischen Reverse-Transkriptase-Hemmer (NNRTI), einem Proteaseinhibitor (PI) oder einem dritten Nukleosidanalogon. Welche Kombination die beste ist, lässt sich pauschal nicht beantworten, und wird individuell entschieden. Jede der Kombinationen hat Vor- und Nachteile: Die Kombination aus 2 NRTI und einem PI wurde dem größten Testspektrum ausgesetzt und es liegen Daten aus Langzeitstudien zum klinischen Effekt vor. Diese Kombination weist eine hohe Barriere gegen Resistenzen auf. Die hohe Pillenzahl stellt jedoch eine Belastung für den Patienten dar und wirkt sich negativ auf seine Adherence aus. Auch ist eine Langzeittoxizität zu befürchten. Eine Kombination aus 2 NRTI und einem NNRTI besitzt offenbar eine ähnlich virenhemmende Wirkung wie PIs, jedoch ist nicht der klinische Effekt, sondern lediglich der Effekt auf Laborparameter durch Studien belegt. Die geringe Pillenzahl (einmal am Tag für den NNRTI, zweimal am Tag die NRTI) stellt hierbei eine geringere Belastung für den Patienten dar. Zu Beginn der Therapie mit Nevirapin treten jedoch häufig Allergien auf. NNRTI sind resistenzanfälliger, und durch Kreuzresistenzen fällt eine ganze Wirkstoffklasse weg. 3 NTRI haben die geringste Pillenzahl und die einfachste Dosierung. Eine Kombination aus AZT, 3TC und Abacavir ist in einer Tablette (Trizivir) verfügbar, die 2-mal täglich eingenommen wird. Andere Kombinationen sind aus patentrechtlichen Gründen nicht in einer Tablette verfügbar. In Indien, Südafrika, Brasilien und Kenia werden auch Tabletten mit zwei NRTI und einem NNRTI als Generikum produziert. Es scheint wenige Interaktionen mit anderen Medikamenten zu geben, und sollte es zur Unverträglichkeit oder Resistenzen kommen, so stehen noch 2 andere Wirkstoffklassen zu Verfügung. Es liegen jedoch keine Langzeitdaten mit klinischen Endpunkten vor und die Kombination scheint auch etwas weniger wirksam in der Virusunterdrückung zu sein. Startzeitpunkt einer HAART Zum besten Startzeitpunkt einer HAART gibt es keinen Konsens, da die Gefahr an Aids zu erkranken gegen die Risiken der Langzeittoxizität und Resistenzbildung abgewägt werden müssen. Während Mitte der 1990er Jahre die Mutationsgeschwindigkeit des Virus und die Annahme einer möglichen Eradikation zu einer „Hit hard and early!“-Strategie bei der Behandlung verleiteten, führte die Entdeckung mitochondrialer Toxizität zur Zurückhaltung. Heute beginnt eine HAART erst bei deutlicher Schwächung des Immunsystems. Die Deutsch-Österreichische Empfehlung zum Therapiebeginn berücksichtigt drei Faktoren: Das klinische Bild des Patienten, seinen CD4-Wert und die Viruslast. Patienten, die bereits Aids-definierende Erkrankungen haben (CDC C), wird eine HAART dringend empfohlen. Auch beim Auftreten von Erkrankungen, die auf ein geschwächtes Immunsystem hindeuten, jedoch nicht Aids-definierend sind (CDC B), wird eine HAART empfohlen. Dies gilt auch für Patienten, die symptomfrei sind, aber einen CD4+ Wert unter 200 haben, da es dann meist eine Frage der Zeit ist, bis Aids auftritt. Als im Allgemeinen ratsam wird eine Therapie bei Patienten angesehen, die einen CD4+ Wert zwischen 200 und 350 haben. Ebenso angeraten ist der Beginn der HAART laut der Empfehlung bei Patienten mit einem CD4+ Wert zwischen 350 und 500, wenn eine hohe Viruslast vorliegt (>100.000). Aufgrund der für den Patienten weitreichenden Konsequenzen, wird die Entscheidung individuell getroffen, so dass der Patient zuvor über Risiken und Nebenwirkungen ausreichend informiert und psychisch auf diese Therapie eingestellt ist.