Myograph
Werbung

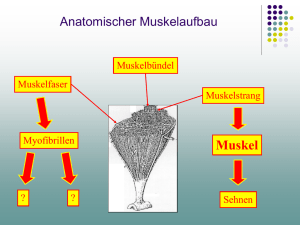
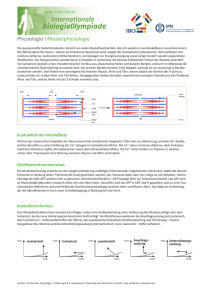
29.05.2006 Melanie Thompson Tierphysiologisches Praktikum Sommersemester 2006 - Versuch IX: Myograph, durchgeführt am 24.05.2006 Gruppe XII Mittwoch morgens Einleitung Das Nervensystem eines Organismus hat die Aufgabe elektrische Signale (oder auch Aktionspotentiale) zu verrechnen, fortzuleiten und zu übertragen, hierfür sind die Neuronen zuständig, die ihrer Aufgabe entsprechend charakteristische Strukturen besitzen: Dendriten – dienen der Aufnahme von Aktionspotentialen (kurz APs), Soma – enthält den Zellkern der Neurone, und verrichtet alle lebenswichtigen Aufgaben für das Neuron und das Axon – übernimmt die Fortleitung von Informationen über längere Strecken. Auch Muskelbewegungen werden im ganzen Tierreich, bis auf wenige Ausnahmen, durch Neurone kontrolliert. Diese Neurone nennt man Motoneurone, da ihre Axone Muskelfasern innervieren. Die Skelettmuskulatur der Wirbeltiere wird durch Motoneuronen des Rückenmarks gesteuert. Jede Muskelfaser wird von einem Motoneuron innerviert, wobei sich die Motoneuronen auf mehrere hundert Muskelfasern verzweigen, diese Aufspaltungen des Axons werden als Kolaterale bezeichnet. Die Gesamtheit aus Motoneuron und die von ihm innervierten Muskelfasern bezeichnet man als motorische Einheit. Skelettmuskeln bestehen aus mehreren hundert motorischen Einheiten, wobei alle Muskelfasern einer motorischen Einheit zum 1 selben Typus (entweder slow, fast-fatigable oder fast fatigue resistant) gehören und sich ein Skelettmuskel zu unterschiedlichen Anteilen aus allen drei Muskelfasertypen zusammensetzt. Möchte ein Organismus (hier ein Wirbeltier) eine Bewegung vollziehen, so beginnt diese im prämotorischen Cortex. Der dort entstandene Impuls wird über die Pyramidenbahnen an die im Dorsalganglion des Rückenmarks liegenden Motoneuronen weitergeleitet. Aktionspotentiale entstehen immer am Axonhügel, da dort die Summation der einkommenden postsynaptischen Potentiale stattfindet und hier die Schwelle zur Entstehung eines APs aus zwei Gründen am niedrigsten ist, zum einen, weil sich an dieser Stelle die ersten spannungsabhängigen Ionenkanäle befinden, und zum anderen, weil dort die Myelinscheide erst beginnt. Ein Aktionspotential wird typischer Weise durch eine elektrotonische Depolarisation ausgelöst, die in einem Dendriten oder im Soma aufgetreten und entlang der Membran zum Axon gelangt ist. Ein Muskel-AP entsteht immer nach dem „Alles oder Nichts“-Prinzip, hierbei muss ein bestimmter Schwellenwert überschritten werden, andernfalls entsteht kein Aktionspotential. Wird diese Schwelle jedoch überschritten, so ist es nahezu vollkommen egal, wie weit sie überschritten wurde, ein AP entsteht in jedem Fall, oder anders: Die Amplitude des Aktionspotentials wird nicht durch die Reizamplitude bestimmt. Das Axon ist für die Erregungsfortleitung verantwortlich, dabei wandert ein Aktionspotential nicht im eigentlichen Sinne, sondern wird immer wieder sequenziell entlang des Axons aufgebaut. Es gibt im Wesentlichen zwei Möglichkeiten die Geschwindigkeit der Erregungsfortleitung zu verbessern: 1. Durch Vergrößerung des Axon-Durchmessers (bspw. bei Riesenaxonen), dieser bewirkt eine Abnahme des Längenwiderstandes, was darin resultiert, dass der Schwellenwert zur Bildung eines APs auch noch in entfernteren Abschnitten überschritten wird, die Leitungsgeschwindigkeit wird erhöht. 2. Durch Abschnittsweise Myelinisierung, durch die Isolierung der Fasern durch Schwann’sche Zellen nimmt der Querwiderstand der Membran deutlich zu, Ströme quer zur Membran werden unterdrückt. An den Ranvier’schen Schnürringen wird das AP wieder aufgefrischt, was zu einer saltatorischen, schnelleren Erregungsleitung führt. 2 Die Höchstfrequenz und Ausbreitungsrichtung für aufeinander folgende APs wird durch die Refraktärzeit vorgegeben. Als Refraktärzeit bezeichnet man den Zeitraum nach einem AP, in dem kein weiteres Aktionspotential ausgelöst werden kann, da während dieser Zeit das Neuron nicht auf eine Depolarisation reagieren kann. Das Nervensystem hat trotz dem „Alles oder Nichts“-Prinzip und dem Vorhandensein von Refraktärzeiten die Möglichkeit zwischen starken und schwachen Reizen zu unterscheiden, dies über die Tatsache, dass starke Reize eine höhere Frequenz von APs bedingen als schwächere Reize. So generiert das Neuron auf einen starken Reiz also zahlreiche Aktionspotentiale, die maximal so schnell aufeinander folgen können, wie es die Refraktärzeit erlaubt. Die Reizstärke wird damit durch die Zahl der Impulse pro Sekunde – die Frequenz der APs – und nicht durch deren Amplitude codiert. Auch ein Muskel hat die Möglichkeit graduelle Abstufungen der Kontraktionskraft vorzunehmen, dies über zwei Möglichkeiten: Zum einen, wie eben erwähnt durch die Veränderung der Frequenz der nervenaktionspotentiale, zum anderen durch die Rekrutierung einer zunehmenden Anzahl von motorischen Einheiten, wobei sich durch das Ansprechen besonderer Muskelfasertypen die Kontraktionskraft auch qualitativ variieren lässt Bei der Rekrutierung „wählt“ das Nervensystem aus, wie viele motorische Einheiten zu jedem Zeitpunkt aktiviert werden und ob große oder kleine motorische Einheiten angesprochen werden. Außerdem ist es möglich, die Spannung eines Muskels sequenziell zu erhöhen, indem eine zunehmend größere Zahl von Motoneuronen aktiviert wird. Kommt ein Aktionspotential nun an das „Ende“ eines Neurons gelangt es zur Synapse. Im Falle einer motorischen Einheit wird der synaptische Kontakt zwischen Motoneuron und der Skelettmuskelfaser als motorische Endplatte bezeichnet. Ein Ankommendes Aktionspotential löst hierbei einen Ca2+ Einstrom aus, der nicht nur in Richtung seines elektrischen, sondern auch in Richtung seines chemischen Gradienten in die Zelle einfließt. Aufgrund dieses Ca2+-Einstroms verschmelzen die synaptischen Vesikel mit der präsynaptischen Membran und entleeren ihren Inhalt, den Neurotransmitter Acetylcholin, in den synaptischen Spalt. 3 Die subsynaptische Membran der Muskelfaser weißt querverlaufende Einfaltungen auf, in die rezeptorgesteuerte Ionenkanäle eingelagert sind. Bindet Acetylcholin an den Rezeptor verändert sich die Membranleitfähigkeit und es kommt zu einer Depolarisation der subsynaptischen Membran. Dieses lokale amplitudengraduierte postsynaptische Potential (PSP), wirkt hier erregend und wird Endplattenpotential (EPP) genannt. In der Regel ist es überschwellig und löst ein Muskelaktionspotential aus. Die Ausschüttungen von Acetylcholin, die durch Nervenaktionspotentiale bedingt waren, führen physiologisch stets genau zu einem Muskelaktionspotential. Das Muskelaktionspotential breitet sich von der motorischen Endplatte über das gesamte Sarkolemm bis zu den beiden Faserenden aus. Über Einstülpungen gelangt das AP in die Tiefe der Muskelfaser, wo es in Kontakt mit dem in Faserrichtung ausgerichteten sarkoplasmatischen Reticulum, dem Calciumspeicher der Muskelzelle, in Verbindung kommt. Das ankommende AP sorgt dafürt, dass aus dem sarkoplasmatischen Reticulum Ca2+ in das Sarkoplasma abgegeben wird, damit steigt die Ca2+-Konzentration von 10-7 auf 10-5m an und bedingt die eigentliche Muskelkontraktion. Wichtig zum Verständnis des Ablaufes einer Kontraktion ist zunächst der Aufbau eines Muskels. Ein Muskel ist aufgebaut aus mehreren Muskelfaserbündeln, welche wiederum zusammengesetzt sind aus einzelnen Muskelfasern. Eine Muskelfaser enthält viele Myofibrillen, die aus Aneinanderreihungen von Sarkomeren zusammengesetzt sind. 4 Ein Sarkomer wird eingegrenzt durch sog. Z-Scheiben, diese Verlaufen senkrecht zur Faserrichtung. Ein Sarkomer enthält dünne und dicke Filamente. Die dünnen Filamente sind aus Actin und Tropomyosin, die dicken aus Myosin aufgebaut. Den eigentlich kontraktilen Apparat in den Muskeln bilden die aus Aktin aufgebauten Mikrofilamente. In jeder Muskelzelle liegen Tausende von Actinfilamenten der Länge nach parallel nebeneinander, wobei sich in deren Zwischenräumen dickere Filamente aus dem Protein Myosin befinden. Zur Kontraktion kommt es, weil die Actin- und Myosinfilamente aneinander vorbeigeleiten, wodurch die Zelle kürzer wird. Verkürzt sich ein Muskel, so verkürzt sich dabei jedes Sarkomer, wobei sich damit auch der Abstand von einer Z-Scheibe zur nächsten verkleinert. Das Verhalten, welches Aktin und Myosin an den Tag legen wird durch die Gleitfilamenttheorie erklärt, diese besagt, dass bei einer Muskelkontraktion weder die Länge der dicken noch der dünnen Filamente verändert wird. Die Filamente gleiten vielmehr in Längsrichtung aneinander vorbei, wodurch sich die Überlappungsbereiche vergrößern. Das Gleiten der Filamente beruht auf einer Wechselwirkung zwischen Actin- und Myosinmolekülen. Das Myosinmolekül besteht aus einem langen, helikalen „Schwanz“ und einem globulären „Kopf“, welcher seitlich absteht. Das dicke Filament wird durch zahlreiche, an ihren „Schwanzenden“ aneinander liegenden Myosinmolekülen gebildet. Die Reaktion, die Energie liefert findet am Kopf des Myosinmoleküls statt, dieser ist nämlich in der Lage ATP zu binden und in ADP und anorganisches Phosphat zu hydrolysieren (ATPase-Aktivität des Myosins). 5 Ein Teil dieser Energie überträgt sich auf das Myosin, woraufhin es eine Konformationsänderung erfährt. Der gespannte Myosinkopf bindet an eine spezifische Stelle am Aktin und bildet so eine Querbrücke zwischen Aktin und Myosin („Actomyosin-Komplex“). Wird die gespeicherte Energie freigesetzt, so geht der Myosinkopf wieder in seine ursprünliche Konformation über, wodurch sich der Winkel verändert, unter dem der Kopf an den Schwanz gebunden ist. Bei dem Vorgang des Umklappens wird eine Kraft auf das Aktinfilament ausgeübt, und dieses in Richtung des Zentrums des Sarkomers gezogen. Die Bindung zwischen Myosin und Aktin wird wieder gelöst, wenn erneut ein Molekül ATP am Myosinkopf bindet und er Zyklus von neuem beginnt. Fehlt ATP gänzlich, so kann die Bindung zwischen Aktin und Myosin nicht gelöst werden, dieses Phänomen bezeichnet man als Totenstarre oder Rigor mortis. Neben diesen aktiven kontraktilen Komponenten hat ein Muskel auch passive mechanische Eigenschaften. Diese lassen sich zusammenfassen zu serienelastischen (bspw. Endsehnen) und parallelelastischen (bspw. Sarkolemma) Komponenten. Befindet sich der Muskel vor der Kontraktion in Ruhelage, so werden bei einer Kontraktion zunächst die serienelastischen Elemente vorgespannt, bis die Gewichtskraft der zu bewegenden Gließmaßen erreicht ist. Dieser Vorgang vollzieht sich nach einer auxotonischen Kontraktion, wobei sich der Muskel sowohl anspannt als auch verkürzt. Die serienelastischen Elemente werden erst in der Erschlaffungsphase der Kontraktion wieder entspannt. Kommt es jedoch zu einem zweiten Aktionspotential bevor die Erschlaffungsphase abgeschlossen ist, müssen sich die serienelastischen Elemente nicht mehr vordehnen, die Kontraktionen summieren sich zu tetanischen Kontraktionen. Als nächstes kommt es zu einer isotonischen Kontraktion, hierbei verkürzen sich die kontraktilen Elemente weiter, ohne dass sich der Spannungszustand des Muskels ändert. 6 Darauf folgt eine isometrische Kontraktion, hier kann sich der Muskel makroskopisch nicht mehr verkürzen, da die Muskelenden vollständig fixiert sind. Verkürzungen der kontraktilen Elemente auf molekularer Ebene setzen die Kontraktion über Anspannung der serienelastischen Elemente in Kraft um. Oder anders ausgedrückt, der Spannungszustand des Muskels ändert sich, ohne, dass sich der Muskel selbst verkürzt. Material und Methoden In diesem Versuch sollen Informationen über den Ablauf neuromuskulärer Vorgänge gewonnen werden, wobei der Daumen eines Probanden in eine spezielle Apparatur eingespannt wird, die diesen Test ohne Tierverbrauch möglich macht. Der Daumen wird dann einer Reihe von Test ausgesetzt, die sich wie folgt zusammensetzen: 1. Ein Einzelreiz von 10mA, der den zeitlichen Verlauf einer Einzelzuckung wiedergeben soll 2. steigende Reize mit einer Ausgangsamplitude von 8mA und einer Endamplitude von 16mA, die die Rekrutierung von Motoneuronen verdeutlichen sollen 3. Doppelreize von 9mA, die in immer kürzeren Abständen zueinander kommen und den Weg zum Tetanus verdeutlichen sollen 4. Tetanus, mehrere Reize von 8,5mA die einen glatten Tetanus provozieren sollen 5. Isotonische Maxima, bei einer Amplitude von 10,5mA wird die Kontraktion unter unterschiedlichen Dehnungszuständen gemessen 6. Isometrische Maxima, der Kraftanstieg zum Zeitpunkt einer Dehnung wird bei einer Amplitude von 10,5mA gemessen Die Hebellänge der Probandin betrug 8,8cm, der Muskelradius 6,3cm. Gereizt wird kathodisch. Die Vorgänge werden dann im Computer aufgezeichnet und weitestgehend ausgewertet. Ergebnisse Siehe Graphen im Anhang 1. Versuch – Seite 1 2. Versuch – Seite 2+3 3. Versuch – Seite 4+5 4. Versuch – Seite 6+7 7 5. Versuch – Seite 8+9 6. Versuch – Seite 10+11 Auswertung 1. Versuch Seite 1 zeigt die drei, vom Myographen aufgezeichneten Kurven Die erste gibt den zeitlichen Verlauf einer Einzelzuckung wider, wobei die y-Achse die Kraft, und die x-Achse die Zeit darstellt. Der zweite Graph zeigt den zeitlichen Verlauf des EMG (Summenaktionspotential vom Muskel) und der dritte den zeitlichen Verlauf des PMG (Phonomyogramm). Zu erkennen ist, dass die Einzelzuckung bei ca. 0,025ms beginnt, etwa 0,208ms anhält und nach knapp 0,250ms abflacht. Zieht man den Vergleich zum EMG, so ist schon mit dem bloßen Auge zu erkennen, dass das Summenaktionspotential etwas zeitverzögert zur Einzelzuckung einsetzt. Die Verzögerung beträgt hierbei etwa 0,01ms. Diese zeitliche Differenz lässt sich über die Latenzzeit erklären. Die Latenz- oder Totzeit umfasst die Zeit, die vergeht nachdem ein Reiz auftrifft bis zur Auslösung eines hieraus resultierenden Aktionspotentials. 2. Versuch In diesem Versuch wurden steigende Reize mit einer Anfangsamplitude von 8mA und einer Endamplitude von 16mA induziert. Seite 2 (Anhang) zeigt erneut drei Kurven. Die erste Kurve stellt erneut den zeitlichen Verlauf einer Einzelzuckung dar, jedoch überlagert durch die Einzelzuckungen je nach Amplitudenhöhe. Zu erkennen ist, dass weder die Kontraktionsdauer noch die Lage der Amplitude Reizstärkeabhängig ist. Die Kontraktionsamplitude wächst, die Kraft nimmt zu und auch das Summenpotential erhöht sich, dennoch verändert sich die Lage der Amplitude über alle Reizstärken nicht, genau wie die Dauer der Einzelzuckung und auch die Lage des EMG, was man wunderbar an der dichten Überlagerung der einzelnen Spitzen erkennen kann. Das Maximum bewegt sich hier in einem Bereich von ca. 2,75 Kraft/N bis 8,2 Kraft/N. 8 Das EMG zeigt ein fortwährend gleiches Ergebnis, dies spricht für das „Alles oder Nichts“Prinzip, dass das Überschreiten einer Schwelle ein AP auslöst, es jedoch vollkommen irrelevant ist, wie stark diese Schwelle überschritten wurde. Seite 3 des Anhangs zeigt die Auftragung der Kontraktionen bei veränderter Reizstärke. Zu erkennen ist, dass diese Auftragung der Kontraktionen nahezu linear verläuft, gegen Ende jedoch langsam in eine Stagnation übergeht, also keine stärkere Kontraktion erzielt werden konnte. Dieser Versuch zeigt recht anschaulich, wie durch Rekrutierung von weiteren Motoneuronen und Anstieg der Frequenz von Dauerkontraktionen eine größere Kraft erzielt werden kann. 3. Versuch In diesem Versuchsteil wird die Probandin einem Doppelreiz von jeweils 9mA Amplitudenhöhe ausgesetzt. Hierbei ist die Reizamplitude von großer Bedeutung, da sich, wie auf Seite 4 im Anhang zu erkennen, die Reize, je näher sie einander zeitlich kommen, überlagern, empfindet die Probandin zwei Reize, die sehr nah nacheinander kommen stärker, als sie sie empfinden würde, wenn der Abstand größer wäre. Die Reizfrequenz betrug in diesem Fall zunächst 2Hz, was zwei Ereignissen pro Sekunde, bzw. pro 1000ms entspricht. Die zwei Ereignisse liegen damit 500ms auseinander. Bei dieser Frequenz waren die zwei Reize noch als Einzelreize durch die Probandin zu erkennen. Ab einer Reizfrequenz von 500Hz konnte die Probandin subjektiv keine zwei Reize, sondern nur noch einen erfühlen. Ab diesem Zeitpunkt war auch nur noch ein EMG zu erkennen, da die Refratärzeit des Motoneurons erreicht war. Seite 5 des Anhangs zeigt diesen Umstand recht deutlich. Das Maximum gibt den letzten Zeitpunkt an, an dem noch zwei Reize spürbar und die Kontraktion damit sehr stark war. Ab ca. 500Hz fällt die Kurve, da, wie gesagt, die Refraktärzeit des Motoneurons erreicht war und die Kontraktion des Muskels nicht mehr so stark ausfiel, da quasi nur noch ein verhältnismäßig schwacher Reiz von 9mA auf ihn einwirkte. 9 4. Versuch In diesem Teilversuch werden mehrere Reize von 8,5mA Amplitude hintereinander gegeben um einen Tetanus zu provozieren. Ein Tetanus ist die Summation von Kontraktionen. Dies ist beim Skelettmuskel möglich, da die Kontraktionsdauer 100 Mal länger ist als das AP und die Refraktärzeit zusammen. Da das AP also relativ kurz ausfällt, ist auch die anschließende Refraktärzeit relativ kurz, und ein neues AP kann eintreffen, ohne, dass die vorangegangene Kontraktion schon in ihre Erschlaffungsphase übergegangen ist. Wie auf Seite 6 im Anhang zu erkennen, kommen die Reize zunächst im Abstand von 35ms, ab einer Reizfrequenz von 30Hz (also 30 Ereignissen pro 1000ms) ist ein glatter Tetanus zu erkennen, der Muskel hat keine Zeit zu erschlaffen, bevor das nächste Aktionspotential eintrifft, es kommt zu Dauerkontraktionen. Auch hier ist auf Seite 7 im Anhang zu erkennen, dass die Kontraktionen relativ linear ansteigen und ihr Maximum im Tetanus erlangen. 5. Versuch Dieser Versuchsteil beschäftigt sich mit Kontraktionen unter unterschiedlichen Dehnungszuständen. Bei einer Dehnung wird die Anzahl der Myosinköpfchen, die mit dem Aktin wechselwirken und damit Kraft erzeugen können geringer. Die Amplitude betrug in diesem Fall 10,5mA, der Anfangswert der Dehnung betrug 5N der Endwert 17N. Die obere Kurve auf Seite 8 im Anhang zeigt die Kraft, die auf den Daumen ausgeübt wird, die untere die Länge, die er durch die Kraftausübung annimmt. Dieser Versuch zeigt also, die Muskelverkürzung, ohne, dass eine Spannungsänderung stattgefunden hat. Sehr gut ist dies auch auf Seite 9 im Anhang zu erkennen, wo die Ruhedehnungen, und die isotonischen Maxima recht dicht beieinander liegen. 6. Versuch In diesem Versuchsteil bleibt die Länge des Muskels Konstant, jedoch wird die angelegte Spannung erhöht. Es wird der Kraftanstieg zum Zeitpunkt der Dehnung gemessen. 10 Die Amplitude betrug in diesem Fall erneut 10,5mA. Wie auf Seite 10 im Anhang zu erkennen ist, bleibt die Länge (untere Graphik) je Versuchsdurchlauf konstant. Die Kraft, die auf den Muskel einwirkt, steigt bei jedem Versuchsdurchlauf an(obere Graphik). Auch Seite 11 zeigt recht deutlich, wie der Kraftanstieg im Verhältnis zur Ruhedehnung verläuft. Der hier aufgezeichnete Kraftanstieg verdeutlicht die Dehnung der elastischen Elemente. Diese elastischen Elemente dehnen sich, wenn der Muskel keine weitere Dehnung mehr ausführen kann, und dies ist der hier registrierte Kraftanstieg. Literaturhinweise Praktikumsskript Tierphysiologischer Kurs, Institut für Ökologie, Evolution und Diversität, Johann-Wolfgang-Goethe Universität Frankfurt am Main, 2006 Neil A. Campbell, Jane B. Reece, Biologie, 6. Auflage, Spektrum Akademischer Verlag, Heidelberg – Berlin, 2003 Heldmaier, Neuweiler, Vergleichende Tierphysiologie, 1. Auflage, Springer Verlag, Berlin – Heidelberg – New York, 2003 Wikipedia (http://de.wikipedia.org/wiki/Hauptseite) Bestätigung Hiermit bestätige ich, dass ich dieses Protokoll selbstständig verfasst habe und keine anderen als die angegebenen Quellen und Hilfsmittel verwendet habe. Melanie Thompson, Gruppe XII 11