Trametinib
Werbung

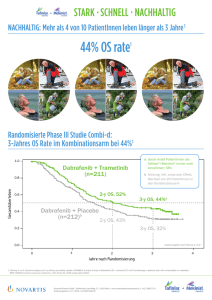
Haben Sie externe Hilfestellungen in Anspruch genommen ? Wenn ja, bitte geben Sie an, welche Hilfestellung Sie in Anspruch genommen haben ? Der Antrag beruht auf einer Vorlage der Arbeitsgemeinschaft Dermatologische Onkologie (ADO) in der Deutschen Krebsgesellschaft und der Deutschen Dermatologischen Gesellschaft basierend auf dem Stand der wissenschaftlichen Erkenntnis sowie Angaben der Herstellers. 1.1 Angefragte Untersuchungs- und Behandlungsmethode (Kurzbezeichnung max. 200 Z.) Trametinib (Mekinist®) zur Behandlung des metastasierten malignen Melanoms. 1.2 Alternative Bezeichnung(en) der Methode MEK-Inhibitor GSK1120212 1.3 Beschreibung der neuen Methode Trametinib ist ein oral verfügbarer MEK-Inhibitor, der selektiv die MEK1- und MEK2-Aktivierung und Kinaseaktivität hemmt. MEK ist ein Target im RAS/RAF/MEK/ERK-Signalweg. Dieser ist bei ca. 50% der Melanome durch das Vorhandensein einer BRAF V600-Mutation konstitutiv aktiviert und kann zu unregulierter Zellproliferation führen. Durch die Inhibition von MEK durch Trametinib kann das Tumorwachstum gehemmt und durch Apoptose eine Regression des Tumors erzielt werden. Durch die gleichzeitige Hemmung von BRAF und MEK mit der Kombinationstherapie von Trametinib und Dabrafenib kann die hemmende Wirkung auf das Tumorwachstum verstärkt und die Resistenzentwicklung verzögert werden. Trametinib wird als Monotherapie oder in Kombination mit Dabrafenib gezielt zur Behandlung von Patienten mit fortgeschrittenem oder metastasiertem Melanom mit BRAF V600-Mutation eingesetzt. Bei Trametinib handelt es sich um eine orale Therapie, die in Form von Tabletten einmal täglich eingenommen wird. Monotherapie: In einer Phase III Studie wurden 322 Patienten mit fortgeschrittenem/metastasiertem Melanom und nachgewiesener BRAF-V600-Mutation im Verhältnis 2:1 randomisiert und mit Trametinib bzw. Chemotherapie (Dacarbazin oder Paclitaxel), behandelt. Patienten, bei denen unter Chemotherapie eine Tumorprogression auftrat, hatten die Möglichkeit Trametinib zu erhalten. Das progressionsfreie Überleben bei Patienten mit BRAF V600E-Mutation, der primäre Endpunkt der Studie, war unter Trametinib gegenüber der Chemotherapie statistisch signifikant verlängert (HR = 0,45; p < 0,0001; medianes PFS 4,8 vs. 1,5 Monate); das Gesamtüberleben war mit Trametinib gegenüber der Chemotherapie ebenfalls statistisch signifikant verlängert (HR 0,54; p=0.01; 6-MonatsÜberlebensrate 81% vs. 67%). Kombinationstherapie: Die Kombinationstherapie aus Dabrafenib und Trametinib wurde in einer Phase II-Studie bei Patienten mit fortgeschrittenem/metastasiertem Melanom und nachgewiesener BRAFV600-Mutation untersucht. Dabei wurden 162 Patienten mit Dabrafenib Monotherapie bzw. in Kombination mit Trametinib behandelt. Das progressionsfreie Überleben, der primäre Endpunkt der Studie, war mit der Kombinationstherapie aus Trametinib (2mg QD) und Dabrafenib (150 mg BID) gegenüber Dabrafenib allein statistisch signifikant verlängert (HR = 0,39; p < 0,001; medianes PFS 9,4 vs. 5,8 Monate). Die Ansprechrate betrug 76% für die Kombinationstherapie, verglichen mit 54% für Dabrafenib allein (p=0.03). Mutationstest: Für eine Behandlung mit Trametinib ist der Nachweis einer BRAF-V600-Mutation mithilfe einer validierten Testmethode (PCR, Sequenzierung) erforderlich. 1. Flaherty KT, Robert C, Hersey P, et al. Improved survival with MEK inhibition in BRAF-mutated melanoma. N Engl J Med 2012;367:107-14. 2. Flaherty KT, Infante JR, Daud A, et al. Combined BRAF and MEK inhibition in melanoma with BRAF V600 mutations. N Engl J Med 2012;367:1694-703. 1.4 Mit welchem OPS wird die Methode verschlüsselt? Ein spezifischer OPS Code für diese Methode ist bisher nicht definiert worden. Der BRAF-V600Mutationstest ist derzeit als Genmutationsanalyse in OPS 1-992.0 verschlüsselt. 2.1 Bei welchen Patienten wird die Methode angewandt (Indikation)? Trametinib ist angezeigt als Monotherapie oder in Kombination mit Dabrafenib zur Behandlung von erwachsenen Patienten mit BRAF V600-mutiertem nicht resezierbarem oder metastasiertem Melanom 2.2 Welche bestehende Methode wird durch die neue Methode abgelöst oder ergänzt? In 2011, 2012 und 2013 wurden erstmals seit über 20 Jahren neue Wirkstoffe zur Behandlung des fortgeschrittenen/metastasierten Melanoms zugelassen: Ipilimumab (Yervoy®), Vemurafenib (Zelboraf®) und Dabrafenib (Tafinlar®). Trametinib ist ein MEK-Inhibitor, der selektiv bei Patienten mit aktivierenden Mutationen des BRAFProteins zum Einsatz kommt. Für Patienten mit BRAF-mutiertem fortgeschrittenem/metastasiertem Melanom kommt als zielgerichtete Therapie somit wahlweise die Kombinationstherapie mit Trametinib und Dabrafenib oder eine Monotherapie mit einem BRAF-Inhibitor (Dabrafenib oder Vemurafenib) oder mit dem MEK-Inhibitor Trametinib in Frage. Neben der zielgerichteten Therapie mit selektiven BRAFund/oder MEK-Inhibitoren besteht – unabhängig vom Vorliegen der BRAF-Mutation – die Möglichkeit einer Therapie mit Ipilimumab oder einer Chemo- oder Immuntherapie. Die verfügbaren Studiendaten deuten auf eine signifikante und klinisch relevante Überlegenheit der Kombinationstherapie von Trametinib und Dabrafenib gegenüber einer Monotherapie mit einem BRAF-Inhibitor hinsichtlich der Effektivität hin. Es ist absehbar, dass die Kombinationstherapie mit Trametinib und Dabrafenib zum Teil die Monotherapie mit einem BRAF-Inhibitor (Dabrafenib oder Vemurafenib) ablösen wird. Trametinib wird überwiegend in Kombination mit Dabrafenib eingesetzt werden; die Monotherapie mit Trametinib wird voraussichtlich eine untergeordnete Rolle spielen. 2.3 Ist die Methode vollständig oder in Teilen neu und warum handelt es sich um eine neue Untersuchungs- und Behandlungsmethode ? Trametinib ist ein neues Medikament, das im Februar 2013 zur Zulassung bei der European Medicines Agency (EMA) eingereicht wurde. Trametinib ist der erste selektive MEK-Inhibitor („first-in-class“) und stellt damit einen vollständig neuartigen Therapieansatz dar. In klinischen Studien beim BRAF-mutierten Melanom wurde die klinische Wirksamkeit von Trametinib als Monotherapie und in Kombination mit Dabrafenib und ein akzeptables Sicherheitsprofil gezeigt. 2.4 Welche Auswirkungen hat die Methode auf die Verweildauer im Krankenhaus? Zum jetzigen Zeitpunkt liegen zu dieser Frage noch keine validen Erkenntnisse vor. Wegen der prinzipiell ambulant durchführbaren oralen Therapie wird die Verabreichung von Trametinib unter stationären Bedingungen wird im Wesentlichen bei Patienten erfolgen, die aus anderen Gründen stationärer Behandlung bedürfen. 3.1 Wann wurde diese Methode in Deutschland eingeführt? Das Medikament wurde seit 2010 im Rahmen klinischer Prüfungen eingesetzt. 3.2 Bei Medikamenten: Wann wurde dieses Medikament zugelassen? Die Zulassung von Trametinib wird im ersten Quartal 2014 erwartet. 3.3 Wann wurde bzw. wird die Methode in Ihrem Krankenhaus eingeführt? ??? 3.4 In wie vielen Kliniken wird diese Methode derzeit eingesetzt (Schätzung)? Trametinib wurde bisher in schätzungsweise 30 Kliniken in Deutschland im Rahmen von Studien eingesetzt. 3.5 Wie viele Patienten wurden in Ihrem Krankenhaus in 2012 oder in 2013 mit dieser Methode behandelt? In 2012 ??? In 2013 ??? 3.6 Wieviele Patienten planen Sie im Jahr 2014 mit dieser Methode zu behandeln? ca. ??? Patienten 4.1 Entstehen durch die neue Methode Mehrkosten gegenüber dem bisher üblichen Verfahren? Wenn ja, wodurch? In welcher Höhe (möglichst aufgetrennt nach Personal- und Sachkosten)? Sachkosten: Trametinib wird einmal täglich oral eingenommen. Die zur Zulassung eingereichte Tagesdosis beträgt 2 mg und wird in Form einer Tablette eingenommen. Eine Packung Trametinib enthält voraussichtlich 30 Kapseln und wird etwa 11.000,00 € brutto kosten. Bei der empfohlenen Tagesdosierung von 2 mg = 1 Tablette betragen die Tagestherapiekosten etwa 367,00 € brutto. Bei der Behandlung mit Trametinib können einmalig Kosten für die Diagnostik der BRAF-Mutation anfallen. Da diese Diagnostik gleichermaßen bei der Anwendung von Vemurafenib oder Dabrafenib erforderlich ist, fallen diese Kosten nur einmalig bei Therapiebeginn mit einer (oder in Kombination) der aufgeführten Substanzen an. Für den Test, der mit einem validierten System durchzuführen ist, ist mit Kosten in Höhe von 100,00 – 120,00 € brutto zu rechnen. Dagegenzusetzen wären einzusparende Kosten für eine konventionelle Chemotherapie (z.B. Dacarbazin 250 mg/m² Tag 1-5 mit Gesamtkosten von ca. 400 Euro) oder auch höhere Kosten z.B. im Rahmen einer Immuntherapie mit Ipilimumab (NUB-Status 1 in 2012). Personalkosten: Keine relevanten Kosten bei Personal auf Station und Apotheke, da orale Einnahme. Bei einem mehrtägigen stationären Aufenthalt, der bei Patienten mit fortgeschrittenem/metastasiertem Melanom üblich ist, ist folglich mit erheblichen Mehrkosten zu rechnen, die über den DRG-Erlös nicht finanziert werden können. Da Patienten im fortgeschrittenen Stadium einer Melanomerkrankung häufig wegen unterschiedlicher Gründe stationär behandelt werden und Trametinib eine orale Dauertherapie ist, ist eine Erstattung auch im stationären Bereich erforderlich. 4.2 Welche DRG(s) ist/sind am häufigsten von dieser Methode betroffen? Bei einer Aufnahme mit der Hauptdiagnose malignes Melanom (C43.-) und konservativer Therapie sind dies in der Regel die DRG J68A oder J61C. Daneben sind auch stationäre Behandlungen unter anderen DRGs mit laufender oraler Dauertherapie denkbar. 4.3 Warum ist diese Methode aus Ihrer Sicht derzeit im G-DRG-System nicht sachgerecht abgebildet? Trametinib wurde noch nicht in der EU zugelassen. Die Kosten für das Medikament sind daher noch nicht sachgerecht in der DRG-Systematik abgebildet. Mit zusätzlichen Arzneimittelkosten von etwa 367,00 € pro Verweiltag während eines stationären Aufenthalts wird die Trametinib-Therapie mit der Fallpauschale allein nicht ausreichend abgebildet. Wie bei anderen innovativen onkologischen Behandlungsoptionen ist die Vergütung als NUB und später als ZE zu prüfen. 4.4 Wurde für diese Methode bereits eine Anfrage gemäß § 6 Abs. 2 KHEntgG beim InEK gestellt?