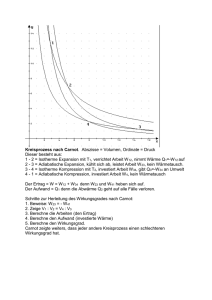
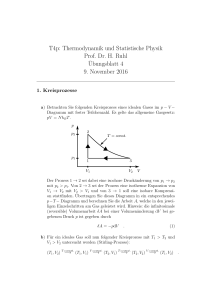
Kreisprozesse
Werbung

Fachschaft Physik / KSL Kreisprozesse Sadi Carnot: 1796-1832 "Réflexions sur la puissance motrice du feu" Verfasst von Werner Fuchsberger James Watt 1736-1819 Erfinder der Dampfmaschine Thermodynamik Physikpraktikum Grundlagenfach Einleitung Der 2. Hauptsatz der Wärmelehre entstand erst im 19. Jahrhundert vor allem auf Grund von Arbeiten des Physikers Ludwig Boltzmann (Wien). Dieser Satz ist Grundlage dafür, dass periodisch arbeitende Wärmekraftmaschinen nie die gesamte zugeführte Wärme in Arbeit umwandeln können, sondern nur immer einen Teil davon. Dies ist nicht ein technisches Gebrechen, sondern die Wirkung des 2. Hauptsatzes der Wärmelehre, eines grundlegenden Naturgesetzes. Eine erste solche Wärmekraftmaschine war die Dampfmaschine von James Watt. Diese Maschine war Ausgangspunkt einer revolutionären Wandlung der Gesellschaft von einer Agrargesellschaft in die Industriegesellschaft. Knapp 50 Jahre später hat Sadi Carnot (Frankreich) die theoretischen Grundlagen der Energieumsetzungen in Wärmekraftmaschinen erarbeitet. Er fand und untersuchte den theoretisch effizientesten Kreisprozess. (Jede Wärmekraftmaschine kehrt nach einem Zyklus von Vorgängen in die Ausgangsposition zurück, deshalb Kreisprozess). Er entdeckte damit die Obergrenze für den Wirkungsgrad aller Wärmekraftmaschinen, die zwischen den Temperaturniveaux T 1 und T2 (T1 > T2, Angabe in Kelvin) arbeiten. T T T 1 2 1 2 T1 T1 Fachschaft Physik / KSL Versuchsziele Internet-Recherche zu Sadi Carnot, James Watt, Ludwig Boltzmann Vorstellen der Ergebnisse der Recherche Selbständiges Erarbeiten einer physikalischen Grundlage der Technik unter Benutzung von Unterlagen Diskussion von Problemen zur Thematik Studium der Modelle eines Viertakt- und Zweitaktmotors Übungsaufgaben als Hausaufgabe Vorbereitung Vorausgesetzt wird die Kenntnis der Zustandsgleichung idealer Gase, die Kenntnis der "Isoprozesse": isobar, isochor, istherm, isentropisch (=adiabatisch) 1. Hauptsatz der Wärmelehre: quantitativ 2. Hauptsatz der Wärmelehre: qualitativ Grundlegendes Vorgehen zur Bestimmung der Wärme Grundlegendes Vorgehen zur Bestimmung der Arbeit Material 1 PC / Notebook je Gruppe; Internetzugang Modell Viertaktmoter, Modell Zweitaktmotor, evtl. Modell Dampfmaschine Durchführung und Auswertung 1. 2. 3. 4. 5. Internet-Recherche: 10 min Je eine Gruppe recherchiert im Internet zu den biographischen Themen (siehe Versuchsziele) mit folgenden Fragestellungen: - Umfeld der Person (Familie, soziales Umfeld) - Ausbildung / Beruf der Person - Thematik der wichtigsten Arbeit - Auswirkungen der Ergebnisse und Aussagen der Person für Physik und Gesellschaft. Mitteilung der Ergebnisse der Internet-Recherche, Diskussion: 10 min Am gemeinsamen Tisch werden die Ergebnisse mitgeteilt und kurz diskutiert. Arbeit und Wärme der Iso-Prozesse eines idealen Gases: 20 min An Hand der im Anhang 1 beigefügten Inhalte zu Wärme und Arbeit der Iso-Prozesse sind diese zu erarbeiten. Verständnisprobleme sind mit der Lehrperson zu klären. Der Carnot'sche Kreisprozess: 20 min An Hand der im Anhang 2 beigefügten Inhalte über den Carnot'schen Kreisprozess sind die Schritte der Entwicklung nachzuvollziehen. Dabei werden sich wahrscheinlich Verständnisprobleme ergeben. Diese sind mit der Lehrperson zu besprechen. Am Ende steht die eingangs geschilderte Idealformel für den thermodynamischen Wirkungsgrad einer Wärmekraftmaschine. Beachte, dass Carnot zusätzlich gezeigt hat, dass kein anderer Kreisprozess einen besseren Wirkungsgrad haben kann. In einer gemeinsamen Diskussionsrunde sollen die Erkenntnisse nochmals gefestigt werden. Die Modelle des Viertaktmotors und des Zweitaktmotors: 15 min Je 2 Gruppen schliessen sich zusammen und studieren die Modelle, sodass der Ablauf verstanden wird. Das Lehrbuch mit seinen Abbildungen ist sicher hilfreich dafür. Zusatzaufgaben Es sind Übungsaufgaben nach Vorgabe der Lehrperson zur Thematik zu lösen. S 180 / 31 - 34 PS-Praktikum GF Seite 2/5 Kreisprozesse / Version 1 Fachschaft Physik / KSL Anhang 1: Arbeit und Wärme der "Iso-Prozesse" eines idealen Gases Überlege zu den einzelnen Prozessen, welche besonderen Bedingungen der Zustandsgrössen gelten. Z. B. Isobarer Prozess: Gay-Lussac Gesetz. Überlege weiter, wie diese Prozesse grafisch in den Diagrammen Vp, TV, Tp darzustellen sind. Die Richtung (z.B. Kompression oder Expansion) ist von Bedeutung. Vorzeichen: Dieses ist positiv, wenn die Transportenergie (Q oder W) dem Gas zugeführt wird, negativ, wenn sie abgeführt wird. n = Molzahl, CV, Cp sind spezifische Molwärmen, Temperaturen immer in Kelvin, Drücke immer in Pascal, Volumen immer in m3. Q = Wärme, W = Arbeit. Cp R = universelle Gaskonstante = 8.31 J/(Mol K). Cp CV R , CV p const T Q nCV T2 T1 ; keine Arbeit, weil V = const, also keine Kolbenbewegung 1. Isochorer Prozess: V = const; Amontons Gesetz: Sofern T2 > T1 ist es eine Erwärmung. Q > 0. V const T Q nCp T2 T1 , es gilt dabei: Cp CV R ; Vorzeichen wie bei 1. 2. Isobarer Prozess: p = const, Gay Lussac Gesetz: W p V2 V1 , Die Arbeit ist negativ, wenn V2 > V1 (Expansion). 3. Isothermer Prozess: T = const, U = const, Boile-Mariotte Gesetz: pV const W V2 V2 V1 V1 p dV V nRT dV nRT ln 2 Vorzeichen ist negativ bei Expansion V V1 V Weil U = 0 gilt: Q W nRT ln 2 Vorzeichen ist positiv bei Expansion V1 Die zugeführte Wärme wird vollständig in Arbeit umgewandelt. In umgekehrter Richtung wird die zugeführte Arbeit vollständig als Wärme abgeführt (Umgebungsspeicher) 4. Isentropischer oder adiabatischer Prozess: Q = 0, S = 0. Poisson Gleichung(en): pV const , TV k 1 const , T p1 const , Cp CV Q=0 (Definition), damit wird U = W (1. Hauptsatz) W nCV T2 T1 Das Vorzeichen ist positiv bei Kompression (Temp.-erhöhung) PS-Praktikum GF Seite 3/5 Kreisprozesse / Version 1 Fachschaft Physik / KSL Anhang 2: Kreisprozess nach Carnot. Abszisse = Volumen, Ordinate = Druck Der Prozess besteht aus: 1 - 2 = Isotherme Expansion mit T1, verrichtet Arbeit W 12, nimmt Wärme Q1=-W 12 auf 2 - 3 = Adiabatische Expansion, kühlt sich ab, leistet Arbeit W 23, kein Wärmetausch. 3 - 4 = Isotherme Kompression mit T2, investiert Arbeit W 34, gibt Q3=-W 34 an Umwelt 4 - 1 = Adiabatische Kompression, investiert Arbeit W 4, kein Wärmetausch Der Ertrag = W = W 12 + W 34 denn W 23 und W41 heben sich auf. Der Aufwand = Q1 denn die Abwärme Q2 geht auf alle Fälle verloren. Schritte zur Herleitung des Wirkungsgrades nach Carnot: 1. Beweise: W 23 = - W 41 2. Zeige V1 : V2 = V4 : V3 3. Berechne die Arbeiten (den Ertrag) 4. Berechne den Aufwand (investierte Wärme) 5. Berechne den Wirkungsgrad. Carnot zeigte weiters, dass jeder andere Kreisprozess einen schlechteren Wirkungsgrad hat. PS-Praktikum GF Seite 4/5 Kreisprozesse / Version 1 Fachschaft Physik / KSL 1. Behauptung: W 23 = -W41 beides sind adiabatische Prozesse, Q = 0 J; U = W W23 = Cv (T2- T1) W41 = Cv (T1- T2) Somit stimmt die Behauptung 2. isotherm sind: p1V1 p2 V2 ; p4 V4 p3V3 adiabatisch sind: p 2 V2 p3 V3 ; p1V1 p 4 V4 V1 V2 V V 4 3 V2 V1 V3 V4 1 1 V V2 3 1 1 V1 V4 V1 V4 V2 V3 3. V2 V2 dV V nRT1 ln 2 V V1 V1 W12 p dV nRT1 V1 W34 nRT2 ln W nR ln V3 V nRT2 ln 4 V4 V3 V2 (T1 T2 ) V1 4. Q1 W12 nRT1 ln V2 V1 5. W Q PS-Praktikum GF V2 (T1 T2 ) T T T V1 1 2 1 2 V2 T1 T1 nR ln T1 V1 nR ln Seite 5/5 Kreisprozesse / Version 1