270150 VO Allgemeine Chemie
Werbung

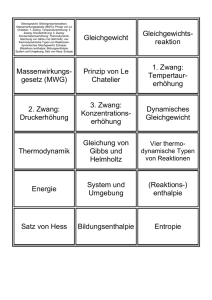
270150 VO Allgemeine Chemie Bernhard Keppler, Vladimir Arion, Herbert Ipser, Regina Krachler Dienstag, 9.30 – 11.00 Uhr Mittwoch, 11.15 - 12.00 Uhr Donnerstag, 9.30 – 11.00 Uhr ------------------------------------------ Prüfungen • Vorlesungs-Prüfung: schriftlich, 15 Fragen/ 100 Punkte maximal erreichbar. Für diese Prüfung erhält man ein Zeugnis. • Termine der Vorlesungs-Prüfung: 1. Anfang Februar, 2. Ende Februar, 3. Anfang März, 4.nach den Osterferien, 5. Ende Juni, 6. Ende September • Zwischenprüfung: Ende November oder Anfang Dezember. Die Teilnahme an der Zwischenprüfung ist freiwillig, sie kann nicht wiederholt werden. Falls man die Vorlesungs-Prüfung zum 1., 2. oder 3. Termin absolviert, ist das (positive) Ergebnis der Zwischenprüfung anrechenbar, und es sind dann statt 15 nur 6 Fragen zu beantworten. Ab dem 4. Termin ist das Ergebnis der Zwischenprüfung nicht mehr anrechenbar. Literatur C. MORTIMER, U. MÜLLER CHEMIE (Paperback) Georg Thieme Verlag 9. Aufl., 2007 E. RIEDL ALLGEMEINE UND ANORGANISCHE CHEMIE (Paperback) de Gruyter 9. Aufl., 2008 18 Teilreaktionen mit 21 beteiligten Species !! Phen=Phenanthrolin Redox-Indikator rot blau Ein mechanisches System kann um seine Gleichgewichtslage schwingen. Ein chemisches System kann das nicht tun. Schwingende chemische Systeme befinden sich stets fernab vom Gleichgewicht. Sie streben dem Gleichgewicht zu, wobei die Konzentrationen von Zwischenverbindungen oszillieren. Oszillierende Reaktion Wenn nicht gerührt wird, entstehen auch räumliche Muster Belousov-Zhabotinsky-Reaktion Quelle: A. Schunk, Universität Ulm + Reaktionskinetik = Lehre von der Geschwindigkeit chemischer Reaktionen • Altgriechisch kinetikos = die Bewegung betreffend, zur Bewegung gehörend • Während einer Reaktion werden Ausgangsstoffe (Edukte) verbraucht, ihre Konzentrationen im Reaktionsgemisch nehmen daher mit der Zeit ab, während gleichzeitig Reaktionsprodukte entstehen, d.h. die Konzentrationen der Produkte nehmen mit der Zeit zu. • Definition der Reaktionsgeschwindigkeit v: z.B. für die Reaktion aA bB cC P 1 d A 1 d B 1 d C d P v a dt b dt c dt dt Reaktionsgeschwindigkeitsgesetz v k A B C x y z • Das Geschwindigkeitsgesetz einer chemischen Reaktion beschreibt die Abhängigkeit der Reaktionsgeschwindigkeit von den Konzentrationen der Reaktanden. • Für jede Reaktion kann eine Differentialgleichung angegeben werden = das Geschwindigkeitsgesetz der betreffenden Reaktion. • Die Reaktionsordnung=Summe der Hochzahlen x+y+z • Die Konstante k = Reaktionsgeschwindigkeitskonstante (=für eine bestimmte Reaktion eine charakteristische Größe) Reaktionsordnung • Das Geschwindigkeitsgesetz und damit auch die Reaktionsordnung muss experimentell bestimmt werden. • Man kann die Reaktionsordnung nicht aus der Brutto-Reaktionsgleichung ableiten, außer es handelt sich um eine Elementarreaktion. • Die Reaktionsordnung muss nicht ganzzahlig sein. Reaktionen nullter Ordnung A B Pr odukte d A d B v k dt dt Beispiel: Die Reaktion wird durch ein Enzym katalysiert, welches pro Zeiteinheit nur eine ganz bestimmte Menge an Reaktionsumsatz katalysieren kann. Die Edukte A und B stehen hierzu in einem sehr großen Überschuss. Daraus folgt: Die Reaktionsgeschwindigkeit ist unabhängig von den Konzentrationen der Edukte. Reaktionen erster Ordnung A Pr odukte d A v k A dt d A k dt A ln A k t ln At 0 At At 0 e k t Beispiel: N2O ½ O2 + N2 Reaktionen zweiter Ordnung A A Pr odukte d A 2 v k A dt 1 1 k t A At 0 Beispiele: 2 HI (g) H2 (g) + I2 (g) NO (g) + O3 (g) NO2 (g) + O2 (g) Einstufige Reaktionen (Elementarreaktionen) und mehrstufige Reaktionen • Aus der stöchiometrischen Reaktionsgleichung ist nicht zu erkennen, ob die Reaktion in einer Stufe (einem Schritt, einem molekularen Prozess) abläuft (Elementarreaktion), • oder ob eine Kaskade von Elementarreaktionen zeitlich hintereinander mit unterschiedlicher Geschwindigkeit ablaufen. • Erfolgt die Reaktion über zwei oder mehrere Stufen, so treten kurzlebige Zwischenprodukte auf, die in der Reaktionsgleichung nicht aufscheinen. • Der geschwindigkeitsbestimmende Schritt für die Gesamtreaktion ist immer die am langsamsten verlaufende Teilreaktion. Geschwindigkeitsbestimmender Schritt A+B+C Produkte Langsam: A+B Zwischenstufe X Schnell: X+C Produkte v k A B Reaktion 2. Ordnung Aus der Stöchiometrie einer Reaktionsgleichung kann nie unmittelbar auf die Reaktionsordnung geschlossen werden, man muss die geschwindigkeitsbestimmenden Schritte kennen. Molekularität einer Elementarreaktion: Wie viele Teilchen treten zum Übergangszustand (aktivierten Komplex) zusammen? • Beispiel: Einer der beiden monomolekularen Schritte muss also der langsamste und damit derjenige sein, der die Reaktionsgeschwindigkeit und damit die Reaktionsordnung der Gesamtreaktion bestimmt. Reaktionsordnung und Molekularität von Elementarreaktionen A Produkte v = k [A] Monomolekulare Reaktion, Reaktion 1. Ordnung A+B Produkte v= k [A] [B] Bimolekulare Reaktion, Reaktion 2. Ordnung 2A+B Produkte v = k [A]2 [B] Trimolekulare Reaktion, Reaktion 3. Ordnung (sehr selten) Beispiel einer monomolekularen Reaktion Aus: E. Riedl, Allgemeine und Anorganische Chemie Aktivierungsenergie • Damit zwei Teilchen zum aktivierten Komplex zusammentreten und zu den Produkten reagieren, müssen sie zunächst kollidieren. • Im Allgemeinen führt nur ein kleiner Bruchteil der stattfindenden Kollisionen tatsächlich zur Reaktion. • Für eine effektive Kollision muss die Summe der kinetischen Energien der zusammentreffenden Moleküle einen Mindestwert übersteigen. Dieser Mindestwert heißt Aktivierungsenergie. • Temperaturabhängigkeit der Reaktionsgeschwindigkeit Die Geschwindigkeitskonstante k ändert sich mit der Temperatur gemäß der Arrhenius-Gleichung (Svante Arrhenius 1889) ------------------------------------------------------Ea Arrhenius‘sche Aktivierungsenergie R Ideale Gaskonstante T absolute Temperatur A Faktor, berücksichtigt die geometrische Ausrichtung der Moleküle beim Zusammenstoß k Ae Ea RT Energieprofil einer chemischen Reaktion, die über zwei Übergangszustände und eine Zwischenstufe abläuft, wobei der 1. Reaktionsschritt geschwindigkeitsbestimmend ist. Wilhelm Ostwald 1853-1932 Foto aus Wikipedia Der Autoabgas-Katalysator CH 4 2 NO2 CO2 N 2 2 H 2O 4 CO 2 NO2 4 CO2 N 2 2 CO O2 2 CO2 Gleichgewicht im Apfelkrieg, aus: Dickerson/Geis, Chemie eine lebendige und anschauliche Einführung, Verlag Chemie, Basel 1983. Chemisches Gleichgewicht Es findet (wenn die Reaktionsprodukte nicht laufend entfernt werden) im Reaktionsgemisch stets eine Hinreaktion und eine Rückreaktion statt. Nach einer gewissen Zeit hat sich ein Gleichgewicht ausgebildet, bei dem Hin und Rückreaktion gleich schnell ablaufen. Die Gesamtreaktionsgeschwindigkeit ist dann gleich Null. Für diesen Fall gilt das Massenwirkungsgesetz. Das MWG wurde 1867 von Cato Maximilian Guldberg und Peter Waage (Norwegen) experimentell entdeckt und kinetisch abgeleitet. Eine chemische Reaktion kommt bei gegebener Temperatur dann zum Stillstand, wenn der Massenwirkungsquotient Q einen für die Reaktion charakteristischen Zahlenwert K erreicht hat. Foto: Wikpedia C D Q a b A B c aA bB cC dD d Allgemeine Reaktion aA + bB cC + dD Im Gleichgewicht gilt: Q=K Massenwirkungsquotient =Gleichgewichtskonstante C D K a b A B c d Es gibt unendlich viele mögliche Gemische der Reaktanden, die dem MWG genügen und daher nach außen hin nicht reagieren!! :iiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiii Gekoppelte Reaktionen im Gleichgewicht Es können z.B. zwei Reaktionen über einen gemeinsamen Reaktanden D miteinander gekoppelt sein: aA bB cC D D eE fF gG C D K1 A a Bb c F G K2 D E e f g Die Gleichgewichtskonstante der Gesamtreaktion ist gleich dem Produkt der Gleichgewichtskonstanten der Einzelreaktionen: aA bB eE cC fF gG c f g c f g C D F G C F G K K1 K 2 a b e a b e A B D E A B E Kinetische Ableitung des MWG Das MWG lässt sich aus der stöchiometrischen Reaktionsgleichung kinetisch ableiten, auch dann, wenn die Reaktion aus beliebig vielen Reaktionsschritten (Elementarreaktionen) besteht, weil sich für jede der im Gleichgewicht vorhandenen Elementarreaktionen Gleichgewicht einstellt (Hin- und Rückreaktion gleich schnell). aA bB cC dD v hin k hin A B a b v rück k rück C D c v hin v rück K k hin k rück d Cc Dd a b A B