klinische studien
Werbung

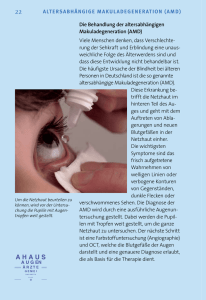
Die AMD ist die häufigste Erblindungsursache in den Industrienationen. Es handelt sich dabei um eine Erkrankung mit multifaktorieller Pathogenese, die sich in zwei Verlaufsformen manifestiert, die atrophische und die exsudative Form. Um der stetigen Zunahme der AMD Herr zu werden, greifen Netzhautspezialisten auf drei Strategien zurück: Primärprävention, Patientenmanagement in der klinischen Praxis sowie medizinische Vorlaufforschung im Dienste neuer Behandlungsmöglichkeiten. D Dr. Henrik Sagnières Facharzt für Augenheilkunde, Netzhautspezialist, Hyères, Frankreich Dr. Henrik Sagnières; privat praktizierender Arzt; Augenarztpraxis Hyères Var; Privatklinik Saint Michel Toulon Var; Studium der Augenmedizin Paris; ehemaliger leitender Oberarzt SCHLÜSSELWÖRTER AMD, Makula, Makulopathie, Pigmentepithel, Lipofuszin, Fotorezeptoren, A2E, oxidativer Stress, Phototoxizität, blaues Licht, in vitro, Fotorezeptoren, Anti-VEGF, Drusen, Prävention, Antioxidanzien, Lichtschutz, Crizal ® Prevencia ® www.pointsdevue.net ie altersbedingte Makula degeneration (AMD) ist eine chronische degenerative Erkrankung der Netzhaut. Sie betrifft ausschließlich den zentralen Netzhautbereich, die sogenannte Makula, und bewirkt eine Degeneration der retinalen Sehzellen. Die AMD ist die häufigste Erblin dungsursache in den Industrie nationen. Die Erkrankung befällt Personen über 50 Jahre und führt zu einem fortschreitenden Verlust des zentralen Sehens, welches für das Detailsehen im Alltag, z. B. zum Lesen, Erkennen von Gesichtern und Autofahren, unverzichtbar ist.. Die physiopathologischen Mechanismen Die genauen physiopathologischen Mechanismen der AMD sind zurzeit noch ungeklärt, jedoch wurde in den letzten Jahren die Beteiligung von toxischen Prozessen festgestellt, die zu einem Absterben der Pigmen tepithelzellen führen. Mit zunehmendem Alter kann es in diesen Zellen zu funktionellen Störungen kommen, die mit einer Ansammlung von Proteolipidkomplexen, den sogenannten Lipofuszinablagerungen, in Lysosomen zusammenhängen. KLINISCHE STUDIEN AMD: KLINISCHES PROTOKOLL, PRÄVENTION UND PERSPEKTIVEN Diese Körner bilden sich vermehrt durch eine Ansammlung nicht abgebauter Proteine und Lipide aus den Fotorezeptor-Außensegmenten, die vom Pigmentepithel phagozytiert werden1 (Finneman et al., 2002). Zudem enthält Lipofuszin zytotoxische Derivate wie A2E aus dem visuellen Zyklus. Unter der Einwirkung von blauem Licht oxidiert A2E und induziert Oxidationen von Proteinen, Lipiden und DNA, was wiederum zu einem hohen oxidativen Stress in den alternden Pigmentepithelzellen führt und diese schließlich absterben (Kim et al., 2006).2 Die Pathogenese Der altersbedingten Makuladegeneration (AMD) liegt eine multifaktorielle Pathogenese zugrunde. Der Hauptfaktor ist vor allem das Alter, denn die Erkrankung tritt ab dem 50. Lebensjahr auf und ihre Prävalenz steigt ab dem 75. Lebensjahr. Für die Erkrankung besteht eine genetische Prädisposition: Das Risiko, eine AMD zu entwickeln, ist viermal höher, wenn ein Elternteil oder Geschwister erkrankt ist. Es wurden mehrere genetische Polymor phismen nachgewiesen, die mit der Points de Vue - nummer 71 - Herbst 2014 33 KLINISCHE STUDIEN ABB. 1 B eispiel der Entwicklung einer Patientin mit serösen Drusen hin zu einer exsudativen AMD mit Neovaskularisation vom Typ chorioretinale Anastomose 1.a - Farbfotos des Augenhintergrunds 1.b - Fluoreszenzangiographie der Netzhaut AF 30° ART [HR] IR 30° ART [HR] FA 1:21.15 30° (9.0 mm) ART (11) Q: 27 [HR] Erkrankung in Zusammenhang stehen. Dabei sind Varianten des Gens beteiligt, welches für den Komplementfaktor H kodiert, oder auch des Gens, welches für HTRA1 (eine Protease) kodiert. Seit 2005 wurden insgesamt 19 Stellen identifiziert, die mit der AMD in Zusam menhang stehen3 (The AMD Gene Consortium Nature Genetics, 3. März 2012). Sie sind an einer Vielzahl biologischer Funktionen beteiligt, einschließlich der Regulierung des angeborenen Immunsystems, dem Erhalt der Zellstruktur, dem Wachstum und der Permeabilität der Blutgefäße, dem Fettstoffwechsel und der Atherosklerose. Bei gleichzeitigem Vorhandensein dreier Varianten (Faktor H, HTRA1 und CC2-FB) bei derselben Person kann das Risiko, eine AMD zu entwickeln, um bis zu 250 Mal höher sein. Rauchen wird besonders häufig mit der AMD in Verbindung gebracht: Es erhöht das Risiko einer Erkrankung um das Dreifache4 (Thornton). Zahlreiche Forschungsarbeiten haben 34 Points de Vue - nummer 71 - Herbst 2014 FA 0:30.29 30° ART [HR] FA 1:03.70 30° ART [HR] FA 2:33.68 30° ART [HR] belegt, dass eine Ernährung, die arm an Vitaminen, Spurenelementen und Antioxidanzien ist, die Erkrankung begünstigen kann 5 (Cohen 2008). Retinale Phototoxizität in Verbindung mit blauem Licht ist ebenso an der AMD-Pathogenese beteiligt. Vor kurzem wurden die für diese Toxizität verantwortlichen Wellenlängen bei Vorhandensein von Lipofuszin in vitro dargestellt, wobei ein blau/violett- Lichtspektrum von 415 nm bis 455 nm mit einem extrem toxischen Höchstwert bei 435 nm aufgezeigt wurde6 (Arnault et al., 2013). Diese Toxizität erhöht sich proportional zur Menge des retinal abgelagerten Lipofuszin, bleibt aber selbst bei Nichtvorhandensein von Lipofuszin in geringerem Umfang bestehen. Diese Wellenlängen sind in erster Linie im Sonnenlichtspektrum vorhanden, können aber in der Strahlung von bestimmten LEDs nachgewiesen werden. Darüber hinaus verdoppelt starkes Übergewicht das AMD-Risiko. Bluthochdruck, kardiovaskuläre Erkrankungen und der Cholesterinspiegel werden ebenso verantwortlich gemacht - welche Rolle sie dabei spielen, ist indes noch nicht geklärt Erscheinungsformen der AMD Bei der AMD wird zwischen der atrophischen und exsudativen Form unterschieden. Die atrophische oder „trockene“ Form hängt mit der Atrophie der Makula zusammen, die durch die progressive Degeneration des retinalen Pigmentepithels und der neurosensorischen Netzhaut kennzeichnet ist. Diese langsam voranschreitende Form der Erkrankung kann nicht geheilt werden. Die exsudative oder „feuchte“ Form manifestiert sich in der anormalen Entwicklung der Blutgefäße unter der Makula. Diese Neoangiogenese ist auch unter der Bezeichnung choroidale bzw. subretinale Neovaskularisation bekannt, daher wird diese Form auch als neovaskuläre AMD bezeichnet. Diese missgebildeten, neuen Blutgefäße sind Makulad eg ener atio n ( AM D) lieg t eine multifakto r ielle P atho g enes e z ug r und e. “ empfindlich und porös und weisen daher eine sehr hohe Hyperpermeabilität auf. Sie zerstören gleichzeitig den physiologischen Aufbau der Netzhaut und somit deren Funktionalität. Es existieren verschiedene Unterarten der neovaskulären Form, je nach Typ und Lage der neugebildeten Gefäße in Bezug auf das Pigmentepithel. Die Fotorezeptoren werden geschädigt, was letztlich zur Bildung von Narbengewebe führt, welches die Makula endgültig zerstört. Sie stellt die aggressivste Form der Erkrankung dar und macht 2/3 der AMD-Formen aus 7 (Eureye). Die choroidale Neovaskularisation wird durch Angiogenese verursacht, bei dem der vaskuläre endotheliale Wachstum sfaktor oder VEGF („Vascular Endothelial Growth Factor“) eine wichtige Rolle spielt. Somit steht er im Zentrum neuer therapeutischer Verfahren, die in den letzten Jahren entwickelt wurden, wodurch die Entwicklung von Anti-VEGFTherapien neue Impulse erfuhr. Diese Behandlungen entwickelten sich mittlerweile zur Standardtherapie, die über intravitreale Injektionen (intraokular) in einem Abstand von durchschnittlich 2 Monaten wiederholt angewandt wird. In den Frühstadien der AMD zeigen sich kleine weiß-gelbliche Ablagerungen am Augenhintergrund im Bereich der Makula, die sogenannten Drusen und/oder Veränderungen des Pigmentepithels. Dieses Merkmal dient zur Bestimmung altersbedingter Makula degeneration oder beginnender AMD. scher und therapeutischer Dringlichkeit dar. Ein Netzhautspezialist, der Patienten mit AMD behandelt, muss imstande sein, einen Patienten innerhalb kürzester Zeit (max. 1 Woche) zur Sprechstunde zu empfangen, wenn dieser ein Skotom (schwarze Punkte beim zentralen Sehen) oder ein Makula-Syndrom aufweist: • verminderte Sehschärfe, Schwierigkeiten beim Lesen • Metamorphopsien (verzerrte Wahrnehmung von Bildern und geraden Linien). Vor dem Hintergrund dieser Symptomatik sind schnellstmöglich ophthalmologische Untersuchungen durchzuführen, einschließlich Sehtest mit EDTRS-Buchstabentafel, Untersuchung des Augenhintergrunds mittels Biomikroskop, Fluoreszeinund/oder IndocyaningrünAngiographie der Netzhaut sowie optische Kohärenztomographie (OCT). Im Falle einer exsudativen subfovealen AMD, deren Diagnose durch diese Untersuchungen gesichert wird, empfiehlt es sich, so früh wie möglich eine Anti-VEGF-Therapie unabhängig von der anfänglichen Sehschärfe zu beginnen. Die AntiVEGF-Therapie erfolgt über intravitreale Injektion. Die neu gebildeten choroidalen extra- und juxtafovealen Blutgefäße mit subfovealen exsudativen Manifes tationen sind als eine subfoveale Lokalisation der AMD zu betrachten. Nach derzeitigem wissenschaftlichen Stand wird in der Regel folgendes Behandlungsprotokoll angewandt. Eine Anti-VEGF-Injektion im Monat während drei aufeinanderfolgender Monate (der Zeitraum zwischen zwei Injektionen muss mindestens vier Wochen betragen) mit abschließender Beobachtungsphase. Während dieser Phase sind die Patienten alle vier Wochen folgendermaßen zu untersuchen: • Sehtest mit ETDRS-Buchstabentafel • Untersuchung des Augenhintergrunds und/oder Elektroretinogramm • optisches Kohärenztomogramm KLINISCHE STUDIEN „Der alter s b ed ing ten ABB. 2 Fluoreszenzangiographie der Netzhaut bei atrophischer AMD IR 30° ART [HR] BAF 30° ART [HR] BAF 30° ART [HR] BAF 30° ART [HR] BAF 30° ART [HR] Die exsudative AMD: Behandlungsprotokoll Aufgrund der Schwere und Verlaufsgeschwindigkeit der exsudativen Form der AMD sowie der Effizienz und Kosten der bisher entwickelten Therapien stellt sie eine echte Herausforderung aufgrund diagnosti- www.pointsdevue.net Points de Vue - nummer 71 - Herbst 2014 35 KLINISCHE STUDIEN ABB. 3 Exsudative AMD mit subfoveal sichtbaren Blutgefäßneubildungen 3.a Fluorescein ICGA 0:42.78 30° ART [HR] IR AF 30° ART [HR] 3.b Angiographie der Netzhaut mit Fluorescein und Indocyaningrün IR 30° ART [HR] AF 30° ART [HR] FA 3:24.75 30° ART [HR] FA 3:20.92 30° ART + OCT 30° (9.0 mm) ART (11) Q: 36 [HR] Erforderlichenfalls kann eine Fluoreszenzangiografie durchgeführt werden. Im Falle eines Rezidivs oder anhaltender Anzeichen einer neovaskulären Läsion, die klinisch am Augenhintergrund und/oder durch eine optische Kohärenztomografie nachgewiesen wurde, ist die Verabreichung einer weiteren Injektion nach den drei ersten Injektionen erforderlich. Durch schnittlich erhalten Patienten 6 bis 7 Injektionen im Jahr. Die AMD ist eine bilaterale Erkrankung. Nach Befall des ersten Auges besteht ein erhöhtes Risiko, dass auch das zweite Auge erkrankt (ca. 10 % pro Jahr). Bei Vorhandensein funktioneller Symptome (Sehbeeinträchtigung, Metamor phopsie, Skotom) am zweiten Auge während der Verlaufskontrolle ist eine Notfallbehandlung indiziert. Es wird empfohlen, AMD-Kontrolluntersuchungen an beiden Augen 36 ICGA 1:46.37 30° ART [HR] Points de Vue - nummer 71 - Herbst 2014 FA 0:34.15 30° ART [HR] durchzuführen, um mögliche anfängliche asymptomatische Läsionen am anderen Auge erkennen zu können. Atrophische AMD: Patientenmanagement Patienten mit atrophischer AMD profitieren leider nicht von den bei Patienten mit exsudativer AMD erzielten therapeutischen Fortschritte. Auch wenn sie langsamer voranschreitet, ist ihre Langzeitprognose ungünstig und es können Kompli kationen in Form von Neovaskula risationen auftreten, weshalb eine FA 1:07.76 30° ART [HR] regelmäßige Kontrolle unverzichtbar ist (Selbstkontrolle mittels AmslerGitter, die bei einer Veränderung der funktionellen Symptome eine rasche ärztliche Beratung notwendig macht). Führt die Visusminderung zu Invalidität, macht die Behandlung der Patienten mit fortgeschrittener AMD den Einsatz rehabilitativer Massnahmen bzw. vergrößernder Low Vision-Sehhilfen erforderlich, die eine Mobilisierung der nicht betroffenen Netzhautbereiche zur Verbesserung des Sehens ermöglichen. Patienten mit altersbedingter Makuladegeneration müssen über die „Der So nnens chutz d ur ch Lichts chutz g l ä se r im Fr eien b leib t eine No twend ig keit vo m fr ühen Kind es alter an, d a d ie Aug enlinse b e i Kind er n tr ans p ar ent is t. “ Kontroll-OCT nach 3 intravitrealen Anti-VEGF-Injektionen Methoden der Eigenkontrolle, namentlich das Amsler-Gitter, aufgeklärt werden. Hochrisiko patienten mit großflächigen konfluierenden Drusen sowie Veränderungen des Pigmentepithels müssen häufig Kontrolluntersuchungen im Hinblick auf ein mögliches Auftreten einer Neovaskularisation unterzogen werden, die dann behandelt werden kann. Es ist unbedingt erforderlich, dass Patienten eine klare Diagnose gestellt wird. Es muss sichergestellt werden, dass die Patienten den Namen der zu Visusverlust führenden Krankheit kennen und Klarheit darüber erhalten, ob es sich um ein Früh- oder Spätstadium der altersbedingten Makuladegeneration bzw. um eine atrophische oder exsudative Form handelt. Den Patienten muss erklärt werden, dass ihre Erkrankung chronischer Natur ist, die behandelt, aber nicht geheilt werden kann und nicht zur www.pointsdevue.net völligen Erblindung führt (Erhalt des peripheren Sehens). Regelmäßige Kontrolluntersuchungen sind unumgänglich. Die Patienten müssen über die Prognose, das Risiko der Erkrankung des zweiten Auges sowie über das Risiko des Übergangs der atrophischen AMD in eine exsudative AMD aufgeklärt werden. Die Primärprävention Die stetig zunehmende Inzidenz der AMD rechtfertigt voll und ganz eine konsequente Primärprävention zur Bekämpfung dieser Erkrankung. Die Primärprävention zielt darauf ab, die Risikofaktoren der Erkrankung zu reduzieren. So können jedem Patienten einfache präventive Maßnahmen hinsichtlich Lebensstil und Ernährung empfohlen werden, z. B.: - Einstellung des Tabakkonsums - Reduzierung von Übergewicht, Behandlung von Störungen des Fettstoffwechsels und Bluthochdruck - Regelmäßige Bewegung - Umstellung auf eine Ernährung, die reich an Makulapigmenten, Lutein und Zeaxanthin (in Obst und Gemüse enthalten) und Omega-3-Fettsäuren (fettreiche Fische wie Lachs, Thunfisch usw.) ist Aufgrund der Ergebnisse einer Studie, die die Toxizität von blau-violetter Strahlung belegt, hat eine Partnerschaft mit einem BrillenglasHersteller die Entwicklung von Gläsern (Crizal® Prevencia®) ermöglicht, die einen Teil dieser schädlichen Strahlung reflektieren und dadurch ihr Eindringen in die Augen verhindern. Folglich sollte das Tragen eines solchen selektiven Schutzes möglichst vielen Menschen empfohlen werden, vor allem Personen mit genetischen Risikofaktoren. Der Sonnenschutz durch Lichtschutzgläser im Freien bleibt eine Notwendigkeit vom frühen Kindesalter an, da die Augenlinse bei Kindern transparent ist. Die Prävention von Komplikationen bei Patienten mit vorausgehenden Läsionen ist heute in gleichem Maße erforderlich. Diese umfasst seit der Veröffentlichung umfangreicher epidemiologischer Studien primär die Verschreibung von Nahrungse rgänzungsmitteln. So soll eine Nahrungsergänzung mit Anti oxidanzien (Zink, Vitamin C und E) das Risiko eines Fortschreitens und einer Verschlechterung der AMD bei Risikopatienten um 25 % mindern8 ( AREDS 1). Eine Nahrungser gänzung mit 10 mg Lutein und 2 mg Zeaxanthin zusätzlich zu den Antioxidanzien soll die Progredienz einer fortgeschrittenen AMD um 18 % verringern9 (AREDS 2). Die Wirkung von Omega-3-Fettsäuren ist nicht so eindeutig, jedoch haben Studien belegt, dass die Aufnahme von DHA in hohen Dosen das Risiko, eine neovaskuläre AMD zu entwickeln, bei Hochrisikopatienten reduziert10 (Nat 2). Points de Vue - nummer 71 - Herbst 2014 KLINISCHE STUDIEN 3.c 37 KLINISCHE STUDIEN ABB.4 B eispiel eines Hochrisikopatienten und unbehandelter fortgeschrittener AMD an einem Auge sowie Drusen und Pigmentveränderungen am anderen „Die s tetig z unehmend e I nz id enz d er AM D r echtfer t i g t vo ll und g anz eine ko ns eq uente P r imär p r även t i o n z ur Bekämp fung d ies er E r kr ankung . “ Die Verschreibung von Nahrungser gänzungsmitteln, deren Zusam mensetzung den besagten Studien daten entspricht, ist daher bei Risikopatienten sowie Patienten mit diagnostizierter AMD zu empfehlen. Neue Therapieansätze Gegenwärtig werden zahlreiche neue Therapieansätze zur AMD erforscht. Sehr bald dürften neue Substanzen im Rahmen der Anti-VEGF-Therapien für die exsudative AMD einschließlich neuer intraokular verabreichter AntiPDGF-Wirkstoffe (Platelet derived growth factor) verfügbar sein. Außerdem werden zahlreiche andere Substanzen getestet, einschließlich Komplementfaktorinhibitoren und Anti-TNF-Wirkstoffe (Tumor necrosis factor) Im Bereich der exsudativen AMD werden gleichzeitig gentherapeutische Untersuchungen mit dem Ziel durchgeführt, einen Anti-VEGF-Wirkstoff direkt in der Netzhaut zu erzeugen, und zwar durch Einbringen eines Gens über einen viralen Vektor direkt in die Netzhautzellen. Dadurch wür- den aus Patientensicht- die mit den wiederholten Injektionen verbundenen Risiken wegfallen. Die Zelltherapie ist ein neuer, in Erprobung befindlicher Ansatz für die atrophische AMD. Das Prinzip besteht darin, Stammzellen oder autologe Pigmentepithelzellen in die Netzhaut zu implantieren, um den Stamm funktioneller Zellen zu erneuern und den Degenerationsprozess zu stoppen. Und last but not least wird für Patienten mit weit fortgeschrittener Sehbehinderung an der Entwicklung einer künstlichen Netzhaut gearbeitet. Dabei wird ein Implantat in die Netzhaut eingesetzt, die die Bildinformationen über eine Brillenkamera empfängt.• DIE KERNPUNKTE Die multifaktorielle Pathogenese der AMD: • Alter • Genetische Prädisposition • Rauchen • vitamin-, spurenelement- und antioxidanzienarme Ernährung • Retinale Phototoxizität (blaues Licht) • Übergewicht • Bluthochdruck LITERATURHINWEISE 1. Finnemann S.C., Leung L.W., Rodriguez-Boulan E. The lipofuscin component A2E selectively inhibits phagolysosomal degradation of photoreceptor phospholipid by the retinal pigment epithelium. Proc Natl Acad Sci U S A. 2002 Mar 19;99(6):3842-7. 2. Kim S.R., Nakanishi K., Itagaki Y., Sparrow J.R. 2006. Photooxidation of A2-PE, a photoreceptor outer segment fluorophore, and protection by lutein and zeaxanthin. Exp. Eye Res. 82, 828-839. 3. The AMD Gene Consortium. Seven new loci associated with age-related macular degeneration. Nat Genet. 2013 Apr;45(4):433-9, 439e1-2. doi: 38 Points de Vue - nummer 71 - Herbst 2014 10.1038/ng.2578. Epub 2013 Mar 3. 4. Thornton J., Edwards R., Mitchell P. Smoking and age-related macular degeneration: a review of association. Eye 2005; 19: 935-44. 5. Cohen S.Y., Desmettre T. La DMLA est-elle due à mon alimentation ? DMLA – Dégénérescence liée à l’âge, Bash 2008, p 70. 6. Arnault E., Barrau C., Nanteau C., Gondouin P., Bigot K, et al. Phototoxic Action Spectrum on a Retinal Pigment Epithelium Model of Age-Related Macular Degeneration Exposed to Sunlight Normalized Conditions. PloS One, 23 August 2013, 8(8) 7. Augood C., Fletcher A., Bentham G. et al. Methods for a population-based study of the prevalence of and risk factors for age-related maculopathy and macular degeneration in elderly European populations: the EUREYE Study. Ophthalmic Epidemiol 2004, 11: 117-129. 8. AREDS Group. A Randomized, Placebo-Controlled Clinical Trial of High-Dose Supplementation With Vitamins C and E, Beta Carotene, and Zinc for AgeRelated Macular Degeneration and Vision Loss. Report no. 8. Arch Ophthalmo, 2001, 119: 1417-1436. 9. Age-Related Eye Disease Study 2 (AREDS2) Research Group Secondary analyses of the effects of lutein/zeaxanthin on age-related macular degeneration progression: AREDS2 report No. 3. JAMA Ophthalmol. 2014 Feb;,132(2):142-9. doi:10.1001/jamaophthalmol.2013.7376. 10. Eric H. Souied, Cécile Delcourt, Giuseppe Querques, Ana Bassols, MD, Bénédicte Merle, Alain Zourdani, Theodore Smith, Pascale Benlian, for the Nutritional AMD Treatment 2 Study Group. (NAT2 study, submitted)