Das maligne Pleuramesotheliom
Werbung

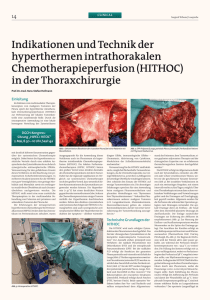
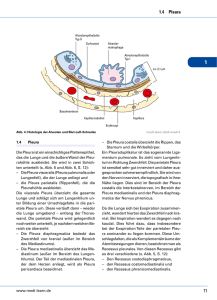
M E D I Z I N Das maligne Pleuramesotheliom Sebastian Sohrab1, Marc Hinterthaner2, Georgios Stamatis2, Klaus Rödelsperger3, Hans-Joachim Woitowitz3, Nikolaus Konietzko1 Zusammenfassung Die Inzidenz und Mortalität des malignen Pleuramesothelioms (MPM) wird in den kommenden Jahren deutlich steigen und aufgrund der langen Latenzzeit nach Asbestexposition erst im Jahre 2017 ihren Gipfel in Deutschland erreichen. Derzeit gilt die Diagnose des MPM als schwierig und die Therapie als wenig erfolgreich. Dieser Artikel gibt einen Überblick über den aktuellen Stand der diagnostischen Verfahren und therapeutischen Möglichkeiten. Im Rahmen der Diagnostik kommt den bildgebenden Verfahren und der Thorakoskopie besondere Bedeutung zu. Therapeutisch werden derzeit multimodale Therapieansätze neben innovativen Verfahren, basierend auf Gentechnik und Immuntherapie, angewandt. Nur eine zunehmende Sensibilisierung für diesen Tumor, die daraus resultierende frühe Diagnose sowie die konsequente Umsetzung klinischer und experimenteller Forschungsergebnisse wird die Prognose des MPM in Zukunft entscheidend verbessern. D as maligne Pleuramesotheliom (MPM) ist ein bösartiger Pleuratumor, der sich bei Asbestexponierten 1 000-mal häufiger als in der Allgemeinbevölkerung findet (39), sodass man von einem „Signaltumor bei Asbestexposition“ spricht. Man unterscheidet zwei Asbestfaserformen, zum einen die speerförmigen Amphibole, zu denen das Krokydolith (Blauasbest) gehört zum anderen die dünneren gebogenen Serpentine, zu denen das weit ver- Schlüsselwörter: Pleuramesotheliom, Asbestexposition, Diagnostik, multimodale Therapie Summary Treatment of Mesothelioma Due to a long latency period after asbestos exposure there will be a considerable increase in the incidence and mortality of malignant mesotheliomas in the next years culminating in 2017 in Germany. At present, diagnosis is considered difficult and therapy seems to be more or less unsuccessful. This article gives an overview about current diagnostic and therapeutic options. Concerning diagnosis, imaging procedures and thoracoscopy are of special importance. Besides multimodal therapy gene therapy and immunotherapy are new treatment options. To improve the prognosis of malignant mesotheliomas firstly we have to become aware of the disease itself which then may lead to an early diagnosis and secondly we have to apply new research results consequently to the clinical routine. Key words: mesothelioma, asbestosis, diagnosis, multimodal therapy Abbildung 1: Großer Rezidivtumor bei Zustand nach extrapleuraler Pleurektomie wegen Pleuramesotheliom rechts mit Durchwachsen der Thorakotomienarbe durch den Tumor. breitete Chrysotil (Weißasbest) gehört. Wenngleich bei nahezu allen kommerziellen Asbestexponierten eine Mischung von Fasertypen vorkommt, ist der Unterschied bedeutsam, da die Serpentine teilweise abbaubar sind und somit biologisch weniger gefährlich. Zu den benignen durch Asbest verursachten Veränderungen gehören Pleuraplaques, bindegewebige Verdickungen der parietalen Pleura, die nach Jahrzehnten verkalken können, daneben die Asbestpleuritis, 1 Abteilung Pneumologie (Direktor: Prof. Dr. med. Nikolaus Konietzko) der Ruhrlandklinik-Universitätsklinik, Essen 2 Abteilung Thoraxchirurgie und Thoraxendoskopie (Direktor: Priv.-Doz. Dr. med. Georgios Stamatis) der Ruhrlandklinik, Essen 3 Institut und Poliklinik für Arbeits- und Sozialmedizin (Direktor: Prof. Dr. med. Hans-Joachim Woitowitz), JustusLiebig-Universität, Gießen Deutsches Ärzteblatt½ Jg. 97 ½ Heft 48½ 1. Dezember 2000 welche als benigner asbestbedingter Pleuraerguss verstanden wird und zu einer diffusen Pleurafibrose führen kann sowie die Lungenasbestose, eine generalisierte, basal betonte Fibrosierung der Lunge. Die histologische Diagnose des MPM ist trotz differenzierter histochemischer Verfahren nicht einfach und die Abgrenzung gegenüber dem metastasierenden Adenokarzinom gelingt in bis zu 15 Prozent der Fälle nicht. Nach heutigem Verständnis stellt die Diagnose Pleuramesotheliom eine Synopsis aus Klinik – hier insbesondere bildgebender und endoskopischer Verfahren – und pathologisch-anatomischen Befunden dar (7, 19). Schleichender Beginn und späte Diagnose im Stadium der Inoperabilität und die relative Resistenz gegenüber Strahlen und Zytostatika machen das MPM zu einem besonders schwer behandelbaren Tumor mit ungünstiger Prognose. Unserer relativen Hilflosigkeit in der Behandlung dieser Tumoren steht eine rasante Zunahme der Fallzahl in den nächsten Jahrzehnten gegenüber. Ziel der vorliegenden Arbeit ist es, den derzeitigen Stand der Epidemiologie, Diagnostik und Therapie darzulegen und Ansatzpunkte für eine Verbesserung des uns derzeit zur Verfügung stehenden Armentariums aufzuzeigen. Epidemiologie Bei gut 70 Prozent aller Mesotheliomerkrankten – und zwar bei Männern häufiger als bei Frauen (12, 38) – findet sich anamnestisch ein beruflicher Asbestkontakt. Man wird jedoch bei Einbeziehung auch von Gefährdungen in der Umwelt und durch Haushaltskontakte nicht fehl gehen in der Annahme, dass nahezu 100 Prozent aller Mesotheliome durch Asbest und andere biobeständige Fasern kritischer Abmessungen verursacht sind (24, 38). So zeigen Faseranalysen im menschlichen Lungengewebe, dass praktisch bei allen Verstorbenen, auch solchen ohne anamnestische Hinweise auf A 3257 M E D I Z I N eine Asbestgefährdung, Asbestfasern theliom können auch Mesothelzellen und in geringerer Menge auch andere des Peritoneums und des Perikards bei Mineralfasern nachzuweisen sind (24, 26, Asbestexponierten maligne transfor27). Überraschend können dabei hohe mieren und zum Perikard- oder PeritoAsbestfaserkonzentrationen immer wie- nealmesotheliom führen. Derzeit werder bei MPM-Patienten ohne klare den in der Bundesrepublik Deutschland anamnestische Hinweise auf eine Ge- jährlich circa 600 Fälle mit MPM von fährdung durch Asbest festgestellt wer- den Berufsgenossenschaften anerkannt, den (25). Ein eindeutiger Zusammenhang zwischen dieser Faserbelastung und dem Mesotheliomrisiko wird bisher allerdings nur für die besonders biobeständigen Amphibolfasern beobachtet (27). Hierbei werden allerdings die anderen Faserspezies nicht exkulpiert, da das jahrzehntelange Verweilen der Fasern bis zum Ausbruch der Erkrankung nicht als Voraussetzung für die Verursa- Abbildung 2: Malignes, knotig die parietale Pleura in ihrer chung des Mesothelioms ange- Gesamtheit bedeckendes malignes Pleuramesotheliom sehen werden kann. (Operationssitus). Außer für das Mesotheliom Grafik 1 ist auch für den Lungen- und Kehlkopfkrebs Asbest als UrAnzahl sache erwiesen (3, 32). Für die 1 200 beiden letzteren Tumorlokali1 000 sationen sind aber neben einer Asbestexposition auch mehre800 re andere Faktoren – insbe1988 sondere das Zigarettenrau600 Entschädigte chen – als Ursache in Betracht Erkrankungen zu ziehen. Daher kann nur das 400 Schätzung gemäß nach heutiger Kenntnis naheBerufskrank200 zu monokausal verursachte heitendokumentation Mesotheliom als Signaltumor 0 einer Asbestexposition gelten. 1960 1980 2000 2020 2040 Auch unter den nichtmalignen Asbestinhalationsfolgen ste- Beobachtete und erwartete Mesotheliomfälle nach Coenen hen heute neben der erst nach et al. (10) in Westdeutschland. Zum Zeitpunkt der Prognose einer starken Exposition be- waren lediglich die bis 1988 aufgetretenen und als Berufskrankheit entschädigten Erkrankungen nach Nr. 4105 BKV obachteten Asbestose insbe- „Durch Asbest verursachtes Mesotheliom des Rippenfelles, sondere die bei niedriger Do- des Bauchfelles oder des Perikards“ bekannt. sis in Erscheinung tretenden Pleuraveränderungen im Vordergrund (32). insgesamt muss mit etwa 1 000 Fällen Für das MPM liegt die Latenzzeit zwi- jährlich gerechnet werden. Aufgrund schen dem Beginn der Exposition ge- der langen Latenzzeit und des Anstiegs genüber Asbest und der Tumormanife- des Asbestverbrauchs in Deutschland station im Mittel bei 35 Jahren, mit einer bis Mitte der siebziger Jahre ist in den Schwankungsbreite von 10 bis 60 Jahren. nächsten Jahren mit einer steigenden InDie Dauer der Asbestgefährdung be- zidenz und Mortalität des Pleuramesoträgt im Mittel 15 Jahre, im Extremfall thelioms zu rechnen. Für Westeuropa auch nur wenige Wochen. Das Manife- muss nach Berechnung von Peto et al. stationsalter des malignen Pleurameso- (22) mit einer Verdoppelung der Mesothelioms liegt in Deutschland bei 65 ± 10 theliomtoten für die nächsten 20 Jahre Jahren. Ähnlich wie beim Pleurameso- von derzeit 5 000 auf gut 9 000 gerechnet A 3258 werden. Der Gipfel wird in den Ländern Westeuropas erst nach 2020 erwartet. In den USA hingegen kulminiert die Inzidenz um die Jahrtausendwende, da dort bereits während des zweiten Weltkrieges ein hoher Asbestverbrauch bestand und verhältnismäßig früh Arbeitsschutzmaßnahmen praktisch durchgeführt worden sind. Die Zahl der männlichen Mesotheliomtoten wird von Peto für Westeuropa in den nächsten 30 Jahren auf circa 250 000 prognostiziert (22). Für Deutschland rechnet Coenen vom Hauptverband der gewerblichen Berufsgenossenschaften in St. Augustin mit dem Gipfel der Mesotheliomtodesfälle um das Jahr 2017 (10). Die tatsächlich beobachteten Zahlen der letzten zehn Jahre folgen der errechneten Kurve relativ gut, sodass die Hochrechnungen als realistisch anzusehen sind (Grafik 1). Diagnostik Die Diagnose des MPM bleibt eine Herausforderung für den Kliniker und den Pathologen. Nur in enger Zusammenarbeit zwischen Beiden ist die manchmal schwierige Diagnose als Synopsis klinischer, röntgenologischer, endoskopischer und histologischer Befunde zu stellen. Anamnese Der Berufsanamnese bei klinischem Verdacht auf ein MPM kommt besondere Bedeutung zu. Bei der langen Latenz zwischen Exposition und Tumormanifestation – im Mittel 35 Jahre – muss der Arzt manchmal detektivische Fähigkeiten entwickeln. Die Fülle asbesthaltiger Produkte der Industrie ist kaum zu überblicken, Kennzeichnungspflicht besteht erst seit Ende der 70erJahre. Mit Abstand der wichtigste Bereich der Arbeitsgefährdung ist im Umgang mit Asbestzement und „schwach gebundenen Asbestfasern“, wie sie zur Isolierung von Lüftungsrohren und Stahlkonstruktionen bis zur Mitte der 70er-Jahre noch verbindlich vorgeschrieben waren, zu suchen. Vernachlässigt wurde in der Vergangenheit auch das Problem der Asbestbelastung bei Arbeiten in der Umgebung von asbest- Deutsches Ärzteblatt½ Jg. 97 ½ Heft 48½ 1. Dezember 2000 M E D I Z I N emittierenden Arbeitsplätzen und die indirekte Asbestbelastung durch asbeststaubverunreinigte Kleidungsstücke, welche von den Ehefrauen von Asbestarbeitern gereinigt wurden. Dagegen wurden die Gefahren einer nicht berufsbedingten Gefährdung der Allgemeinbevölkerung durch Asbest in der Vergangenheit überGrafik 2 schätzt (14). Bildgebende Verfahren Sonographie Ein Pleuraerguss ist bei 80 Prozent der Patienten bei der Erstvorstellung vorhanden. Die Sonographie erlaubt – neben der Darstellung von Pleuraergüs- Klinik Die klinische Symptomatik ist uncharakteristisch und trägt nur wenig zur Diagnosestellung bei. In frühen Stadien der Erkrankung sind typische Tumorsymptome wie Müdigkeit, Abgeschlagenheit und Gewichtsverlust mit 15 Prozent selten (4). Zu den am häufigsten angegebenen Symptomen gehören die Dyspnoe mit kaum merklichem Beginn in drei Viertel der Fälle und zunehmender schlecht lokalisierbarer Thoraxschmerz. Er verschwindet im Gegensatz zur benignen Asbestpleuritis nicht bei Auftreten von Pleuraerguss. In gut einem Drittel der Fälle wird trockener Reizhusten angegeben. Labor 2 4 3 1 4 Schematische Darstellung einer Pleuraverdickung sowie Schrumpfung des Hemithorax in der Röntgenthoraxaufnahme. (1) Pleuraerguss, (2) „knollige“, von der Brustwand ausgehende Tumormassen, (3) perikardiale tumoröse Infiltration und (4) kontralaterale Pleuraplaques Grafik 3 4 3 der Fälle ist der Erguss rechtsseitig lokalisiert. Ebenso können mittels der konventionellen Aufnahme eine diffuse oder noduläre Pleuraverdickung sowie eine Schrumpfung des Hemithorax aufgedeckt werden (Grafik 2). Computertomographie Die Computertomographie hat in der Diagnose und Stadieneinteilung des MPM einen zentralen Stellenwert (Grafik 3). Insbesondere eine Infiltration der Brustwand, die Beteiligung der Lunge sowie ein Befall des Perikards, der mediastinalen Lymphknoten und der kontralateralen Lunge lassen sich mit dieser Methode beurteilen. Darüber hinaus können Pleuraplaques oft besser als mit der konventionellen Röntgenaufnahme nachgewiesen werden. Magnetresonanztomographie und Positronenemissionstomographie Die Magnetresonanztomographie und die Positronenemissionstomographie können bei besonderen Fragestellungen wie zum Beispiel der Beurteilung der Infiltration brustwandnaher Strukturen und eines Tumorrezidivs als ergänzende Maßnahmen in Betracht kommen (2, 13). 2 Invasive Verfahren 2 1 4 In der klinischen Laborroutine gibt es keine auf das MPM hinweisende Parameter. Häufig finden sich nur wenig ausgeprägte Entzündungszei- Schematische Darstellung typischer Veränderungen beim malignen Pleuramesotheliom in der Computertomographie. chen mit erhöhten Leuko- (1) Freier Pleuraerguss, (2) tumorige Infiltration der Pleura, zyten- und Thrombozyten- (3) knotige Tumorinfiltration des Perikards und (4) kontralazahlen sowie Anstieg der Lak- terale Pleuraplaques tatdehydrogenase und alkalischen Phosphatase. Auch die derzeit sen – die Beurteilung des Tumorausgängigen Tumormarker aus dem Serum maßes und die Invasion benachbarter erlauben keine Diagnose: karzinoem- Strukturen (Zwerchfell, Abdomen). bryonales Antigen (CEA) wird nahezu regelhaft in niedriger Konzentration Röntgenbild des Thorax gefunden, während TPS (Tissue Polypeptide Specific Antigen) und CYFRA In der Mehrzahl findet sich im Rönt21-1 (Cytokeratin-Fragment 21-1) in er- genbild des Thorax als Ausgangsbefund höhter Konzentration gefunden wer- ein einseitiger Pleuraerguss meist ohne Mediastinalverlagerung. In zwei Drittel den können. Deutsches Ärzteblatt½ Jg. 97 ½ Heft 48½ 1. Dezember 2000 Pleurapunktion Ein durch Punktion gewonnener Pleuraerguss ist in jeweils der Hälfte der Fälle serös oder hämorrhagisch. Die Analyse gewonnener Exsudate ergibt bei zunehmender Tumorlast erniedrigte pHund Glucosewerte sowie erhöhte Hyaluronsäurewerte. Dagegen ist das CEA in der Regel im Erguss nicht oder nur gering erhöht nachweisbar (16). Pleurabiopsie Die blinde Pleurabiopsie hat eine Sensitivität von unter 50 Prozent, da das MPM häufig in den distalen Teilen der parietalen/diaphragmalen Pleura auftritt, die für eine blinde Biopsie schlecht erreichbar sind (17). A 3259 M E D I Z I N ´ Tabelle 1 C C ´ Stadieneinteilung des malignen Pleuramesothelioms in Anlehnung an die UICC/AJCC 1997 (Asbestkörperchen!), trägt aber zur Diagnostik des malignen Pleuramesothelioms nicht bei. Stadium IA T1a N0 M0 Mediastinoskopie/Laparoskopie Stadium IB T1b N0 M0 Stadium II T2 N0 M0 Stadium III T1,2 T1,2 T3 N1 N2 N0-2 M0 M0 M0 Stadium IV T4 T1–4 T1–4 N0 N3 N0-3 M0 M0 M1 Im Rahmen der Stadieneinteilung, vor allem vor geplanten operativen Eingriffen, ist die Mediastinoskopie empfehlenswert, in bis zu 50 Prozent lassen sich dabei, trotz unauffälligem CTThorax tumorbefallene Lymphknoten ipsilateral (N2) finden. Während die Spezifität der Mediastinoskopie 100 Prozent beträgt, liegt die Sensitivität zwischen 80 bis 95 Prozent, da nicht alle Lymphknotenstationen erreichbar sind (18). Präoperativ sollte ebenfalls eine Laparaskopie zum Ausschluss eines fortgeschrittenen Tumors durchgeführt werden. Thorakoskopie Bei der Thorakoskopie handelt es sich um eine endoskopische Technik, die sich in der Hand erfahrener Pneumologen und Thoraxchirurgen zunehmender Beliebtheit erfreut und deren diagnostische Ausbeute zwischen 90 und 95 Prozent liegt. Sie kann in lokaler Anästhesie mit leichter Sedierung oder besser zur Vermeidung einer Tumorkontamination in Vollnarkose mit einem doppelläufigen Tubus zur getrennten Lungenventilation durchgeführt werden (6). Während der Thorakoskopie ist eine komplette Betrachtung des betroffenen Hemithorax und somit die direkte Beurteilung des Tumorausmaßes möglich (4). Die Biopsieentnahme makroskopisch suspekter Areale erfolgt unter direkter Sicht. Zur Beurteilung der Tumorinfiltration in umgebende anatomische Strukturen und der damit exakten prätherapeutischen Stadieneinteilung ist auch im Hinblick auf eine radikale Operation die gezielte Entnahme von Biopsien nötig. Für die Thorakoskopie als diagnostische Maßnahme spricht neben der guten Verträglichkeit und günstigen Kosten-Nutzen-Relation die hohe Sensitivität von 90 Prozent (17). Bronchoskopie Die Bronchoskopie wird zum Ausschluss eines Bronchialkarzinoms mit Pleuritis carcinomatosa (Adenokarzinom?) durchgeführt, gelegentlich auch zum Nachweis der Asbestbelastung durch bronchoalveoläre Lavage A 3260 Zytologie/Histologie Die zytologische Untersuchung gewonnener Exsudate erbringt in 50 Prozent positive Ergebnisse. Da die Differenzierung gegenüber reaktiv veränderten Mesotheliomzellen schwierig ist, kommen auch falsch-negative Befunde vor. Die Sensitivität beim epithelialen Typ liegt deutlich höher als beim biphasischen Typ. Die Typisierung der Tumorzelle, insbesondere die Unterscheidung zwischen Adenokarzinom und Pleuramesotheliom, kann ähnliche Schwierigkeiten wie die histologische Beurteilung bereiten. Mit der Entwicklung immunhistochemischer Methoden wurde die Diagnose in den letzten Jahren jedoch einfacher. Beim Verdacht auf ein MPM gilt heute der positive Nachweis von Cytokeratin und Vimentin bei fehlendem Nachweis von CEA als richtungsweisend. Darüber hinaus kann der beim MPM fehlende Nachweis des monoklonalen Antikörpers Leu-M1 (CD15) zur Differenzialdiagnose gegenüber dem Adenokarzinom herangezogen werden (20). In circa zehn Prozent der Fälle ist eine eindeutige Aussage MPM oder Adenokarzinom nicht möglich. Derzeit werden ein epithelialer Typ in circa 50 Prozent, ein sarkomatöser oder mesenchymaler Typ in circa 15 Prozent und ein Mischtyp in circa 35 Prozent der Fälle unterschieden. Makroskopisch umscheidet der Tumor die Lunge als breite, schwartige fischfleischartige Verdickung und geht mit einem hämorrhagischen fibrosierenden Exsudat einher. Histologisch findet sich ein mesenchymales Grundgerüst aus spindeligen Zellen und kollagenen Fasern in welches plumpe epithelähnliche Zellen eingeschlossen sind. Im weiteren Verlauf können auch Metastasen in den Lymphknoten, der Leber, dem Skelettsystem und den Nieren auftreten. Funktionsuntersuchungen Die Funktionsuntersuchungen haben vor allem im Hinblick auf das weitere therapeutische Vorgehen beim MPM Bedeutung. Neben der Spirometrie und der arteriellen Blutgasanalyse als Basisuntersuchungen sind EKG und Echokardiographie obligat. Bei einer geplanten Operation ist zur Berechnung der postoperativen Funktionsreserve die Durchführung einer Lungenperfusionsszintigraphie mit Seitenquantifizierung notwendig. Darüber hinaus können in bestimmten Fällen weitere Belastungsuntersuchungen wie beispielsweise Rechtsherzkatheter und Ergospirometrie notwendig werden. Differenzialdiagnose Im Rahmen der Differenzialdiagnose müssen zunächst benigne Pleuraergüsse, hierbei insbesondere der benigne Asbesterguss sowie alle anderen malignen Pleuraergüsse abgegrenzt werden. Bei infiltrativem Wachstum müssen eine Pleurakarzinose, Metastasen eines Adenokarzinoms oder ein peripheres Bronchialkarzinom ausgeschlossen werden. Stadieneinteilung Seit den 70er-Jahren wurden verschiedene Stadieneinteilungen des malignen Pleuramesothelioms entwickelt. Gegenwärtig wird das vom American Deutsches Ärzteblatt½ Jg. 97 ½ Heft 48½ 1. Dezember 2000 M E D I Z I N Joint Committee on Cancer (AJCC) vorgeschlagene TNM-System verwendet. Dieses ist zuletzt durch die International Mesothelioma Interest Group (IMIG) unter Berücksichtigung der Prognose bei Tumorausbreitung (T-Status) des nichtkleinzelligen Bronchialkarzinoms angelehnt und bedarf unter Berücksichtigung der Tumorausbreitung per continuitatem und Befall ungewöhnlicher Lymphknotenstationen weiterer Validierung (Textkasten und Tabelle 1). Therapie Das maligne Pleuramesotheliom hat trotz des sicher malignen Verhaltens mit lokaler Invasion, Destruktion, Bildung von Lymphknoten- (50 Prozent) (30) und Fernmetastasen (33 Prozent bis 49 Prozent) (28) einen vergleichsweise langsamen Spontanverlauf. Es werden mediane Überlebenszeiten von 4 bis 18 Monaten ohne Therapie angegeben (15, 28). Bis vor wenigen Jahren gab es kein therapeutisches Konzept das zu einer deutlichen Verbesserung dieser Überlebensraten führte. In historischen und aktuellen Kollektiven werden bei unselektionierten Patienten mediane Überlebensraten von 4 bis 38 Monaten nach resezierenden Verfahren mit und ohne adjuvante Behandlung angegeben (9, 11, 21, 29, 30, 36). Vergesellschaftet mit diesen eher bescheidenen Ergebnissen in der Resektion war eine hohe Morbidität und Mortalität: Bei dem Versuch der kompletten Tumorexstirpation durch extrapleurale Pleuropneumonektomie verstarben zwischen 5,5 Prozent und 31 Prozent in den 70er- und 80er-Jahren (9, 29, 35). Seit Beginn der 90er-Jahre bekommt jedoch die Therapie des malignen Pleuramesothelioms neue Impulse durch multimodale Therapiekonzepte, sorgfältigere Selektion der Patienten und durch neue Behandlungsmethoden wie die Gen- oder fotodynamische Therapie. Im Folgenden wird eine kurze Zusammenfassung der Modalitäten und der derzeit sinnvollen Konzepte und Aussichten gegeben. Strahlentherapie Die transkutane Radiatio konnte keinen lebensverlängernden Effekt zeigen, wenn auch eine Tumorreduktion beschrieben wird. Da die Lunge im Bestrahlungfeld liegt und radiosensible Organe wie das Knochenmark, der Ösophagus und das Herz direkt benachbart sind und zudem für adäquate Effekte einer Dosis von über 50 Gy erforderlich ist, werden häufig Strahlenpneumonitis, Lungenfibrose, Ösophagitis und Perikarderguss beobachtet. Die Überlebenszeiten werden mit einem Median zwischen 6 und 13 Monaten angegeben (31, 34). Bei multimodalen Konzepten hat die Strahlentherapie einen festen Stellenwert. Ihr wird die entscheidende Rolle in der lokalen Kontrolle nach resezierenden Verfahren zugeschrieben. Nach unveröffentlichten Daten soll eine Reduktion von Lokalrezidiven nach extrapleuraler Pleuropneumonektomie von zehn Prozent auf 3,3 Prozent durch die adjuvante Radiatio von 54 Gy erzielt werden können (31). Als Standard muss die prophylaktische, lokale Radiatio nach diagnostischen und therapeutischen Eingriffen wie Punktionen oder Thorakoskopien angesehen werden (6). Chemotherapie Alle Untersuchungen bezüglich der Monochemotherapie sind enttäuschend. Partielle Remissionen, über sechs bis acht Monate anhaltend, können bei 15 Prozent durch 5-Fluorouracil, bei 20 bis 25 Prozent durch Doxorubicin, Methotrexat oder Ifosfamid erwartet werden. Vinca-Alkaloide und Paclitaxel haben keine Wirkung, platinhaltige Therapeutika nur eine geringe. Neuere Medikamente wie Gemcitabin können noch nicht abschließend beurteilt werden. Auch Polychemotherapien führen kaum zu besseren Ansprechraten. Am positivsten wird die Kombination mit Cisplatin und Gemcitabin mit einer Ansprechrate über 50 Prozent und einer Verbesserung der Symptome in 90 Prozent bewertet (34). Deutsches Ärzteblatt½ Jg. 97 ½ Heft 48½ 1. Dezember 2000 Textkasten TNM-Klassifizierung des malignen Pleuramesothelioms (MPM) T-Primärtumor T1a Tumor begrenzt auf die ipsilaterale parietale und/oder mediastinale und/oder diaphragmatische Pleura. Keine Beteiligung der viszeralen Pleura. T1b Tumor begrenzt auf die ipsilaterale parietale und/oder mediastinale diaphragmatische Pleura. Befall der viszeralen Pleura durch einzelne Tumorherde. T2 Tumorbefall aller ipsilateraler Oberflächen (parietale, mediastinale, diaphragmatische und viszerale Pleura) mit zusätzlicher Beteiligung einer der folgenden Strukturen: ❃ Zwerchfell ❃ ipsilaterale Lunge (ausgehend von viszeraler Pleura) T3 Tumor lokal fortgeschritten, aber noch potenziell resektabel. Tumorbefall aller ipsilateralen Oberflächen (parietale, mediastinale, diaphragmatische und viszerale Pleura) mit zusätzlicher Beteiligung einer der folgenden Strukturen: ❃ thorakale Faszie ❃ mediastinales Fettgewebe ❃ nichttransmuraler Perikardbefall ❃ ipsilateraler Brustwandbefall in Form einzelner komplett resezierbarer Herde T4 Tumor lokal fortgeschritten und technisch inoperabel. Tumorbefall aller ipsilateraler Oberflächen (parietale, mediastinale, diaphragmatische und viszerale Pleura) mit zusätzlicher Beteiligung einer der folgenden Strukturen: ❃ diffuse Ausbreitung oder multifokale Tumormassen in der Brustwand ❃ direkte Ausbreitung des Tumors durch das Zwerchfell in das Peritoneum ❃ direkte Ausbreitung des Tumors in die kontralaterale Pleura ❃ direkte Ausbreitung des Tumors in ein oder mehrere mediastinale Organe ❃ direkte Ausbreitung des Tumors in die Wirbelsäule N-Lymphknoten N0 keine regionären Lymphknoten N1 Lymphknotenmetastase(n) in ipsilateralen, peribronchialen und/oder ipsilateralen Hiluslymphknoten (einschließlich Befall durch direkte Ausbreitung des Primärtumors) N2 Metastasen in ipsilateralen, mediastinalen und/oder subkarinalen Lymphknoten N3 Metastasen in kontralateralen mediastinalen, kontralateralen Hilus-, ipsi- oder kontralateralen Skalenus- oder supraklavikulären Lymphknoten M-Fernmetastasen M0 keine Fernmetastasen M1 Fernmetastasen A 3261 M E D I Z I N Operation Von chirurgischer Seite kommen die Pleurektomie als palliative Resektion und die extrapleurale Pleuropneumonektomie als Resektion mit kurativer Intention zum Einsatz. Die Indikationsstellung zur Pleurektomie erfolgt bei therapierefraktärem Erguss und bei beabsichtigter Tumorreduktion als Vorbereitung zur Durchführung anderer Therapieoptionen. Liegt ein niedriges Tumorstadium vor (begrenzter Pleurabefall), stellt sich die Indikation zur extrapleuralen Pleuropneumonektomie mit Resektion des Zwerchfells und des Perikards und plastischem Ersatz dieser Strukturen. Durch Standardisierung dieses Eingriffs und ein verbessertes perioperatives Management konnte die Mortalität in spezialisierten Zentren auf sechs Prozent und die Morbidität auf 25 Prozent gesenkt werden (31, 36). Multimodaler Ansatz Bei der Kombination der Pleuropneumonektomie mit postoperativer Radiatio und Chemotherapie konnte erstmals bei einem auf die Prognosefaktoren hin selektionierten Patien- Referiert Innovative Verfahren Therapiekonzept nach derzeitigem Erkenntnisstand Im Frühstadium der Erkrankung ist in kurativer Intention die extrapleurale Pleuropneumonektomie mit adjuvanter Radiatio anzustreben. Sollte sich intraoperativ der Tumor als nicht resektabel erweisen, kann die parietale Pleurektomie zur Vermeidung rezidivierender Pleuraergüsse palliativ vorgenommen werden. Bei rezidivierenden Ergüssen sollte eine thorakoskopische Talkumpleurodese und die Radiatio der Zugangsbereiche erfolgen. Bei allen anderen Konstellationen ist ein individuelles palliatives Vorgehen und bei innovativen Verfahren die Anbindung an Studien zu empfehlen. ❚ Zitierweise dieses Beitrags: Gentherapie, fotodynamische Therapie und Immuntherapie Dt Ärztebl 2000; 97: A 3257–3262 [Heft 48] Die Gentherapie, die fotodynamische Therapie sowie die Immuntherapie gehören zu den neueren Therapieverfahren, welche Gegenstand klinischer Forschung sind. Für alle drei Verfahren liegen positive Ergebnisse bei selektionierten Patienten vor; eine abschließende Beurteilung ist derzeit noch nicht möglich (1, 5, 23, 33, 34). Die Zahlen in Klammern beziehen sich auf das Literaturverzeichnis, das über den Sonderdruck beim Verfasser und über das Internet (www.aerzteblatt.de) erhältlich ist. Anschrift für die Verfasser: Prof. Dr. med. Nikolaus Konietzko Abteilung Pneumologie – Universitätsklinik Ruhlandklinik Tüschener Weg 40 45239 Essen bestehen. Hierbei wurde sogar deutlich, dass die gehäufte Extrasystolie ein gleich hohes Langzeitrisiko aufwies wie belastungsinduzierte Ischacc ämiezeichen. Erhöhtes KHK-Risiko bei ventrikulären Extrasystolen im EKG bei asymptomatischen Männern Das Belastungs-EKG findet breite Anwendung im Rahmen der Abklärung einer koronaren Herzerkrankung. Die Signifikanz hierbei auftretender ventrikulärer Extrasystolen bei ansonsten asymptomatischen Personen ist jedoch umstritten. Eine französische Arbeitsgruppe untersuchte bei betroffenen Patienten den Langzeitverlauf im Hinblick auf eine eventuell erhöhte kardiovaskuläre Mortalität. 6 101 asymptomatische Männer, bei denen in den Jahren 1967 bis 1972 Ergometrien durchgeführt wurden und A 3262 tenkollektiv ein deutlicher Überlebensvorteil gesichert werden. Etwa 17 Prozent der Patienten ohne Lymphknotenmetastasen mit einem epithelialen Zelltyp wurden ohne mikroskopisch nachweisbaren Tumorrest reseziert. Bei dieser Gruppe wurde ein medianes Überleben von 51 Monaten und eine Fünf-Jahres-Überlebensrate von 46 Prozent beschrieben. Auch wenn nur ein „Selektionsvorteil“ vorlag, profitierten die Patienten nachweislich mit verlängerten medianen Überlebensraten zwischen 21 und 26 Monaten und Fünf-Jahrs-Überlebensraten von 17 bis 25 Prozent (36). bei denen ventrikuläre Extrasystolen aufgetreten waren, wurden in diese Studie eingeschlossen. Dabei galt eine Extrasystolierate von mehr als zehn Prozent aller ventrikulärer Depolarisationen sowie paarweise oder in Salven auftretende Extrasystolen als gehäufte Extrasystolie. Diese Kriterien wurden von 138 der Untersuchten erfüllt. Nach 23 Jahren hatte diese Gruppe ein um den Faktor 2,67 erhöhtes Risiko für einen Tod mit kardiovaskulärer Ursache. Dies blieb auch nach Multivarianzanalyse bekannter Risikofaktoren für die KHK Jouven X et al.: Long-term outcome in asymptomatic men with exercise-induced premature ventricular depolarizations. N Eng J Med 2000; 343: 826–833. Dr. Jouven, Service de Cardiologie, Hopital Europeen Georges Pompidou, 20 rue Le Blanc, 75015 Paris, Frankreich. Deutsches Ärzteblatt½ Jg. 97 ½ Heft 48½ 1. Dezember 2000