n=1: 2(1) - nadirpoint.de
Werbung

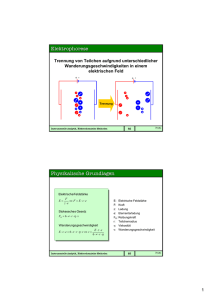
Umweltforschungszentrum Leipzig-Halle; Department Analytik Grundlagen der Atomspektrometrie Atombau und theoretische Betrachtungen 1 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Ursache von Spektren Wechselwirkung zwischen Strahlung und Materie 2 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Ursache von Spektren Wechselwirkung zwischen Strahlung und Materie 3 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik 4 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Wellenlänge und Energie hc E 2 E 1 h : Frequenz : Wellenlänge c: Lichtgeschwindigkeit h: Planck'sche Konstante h = 6.626 1034 J s 5 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik 6 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik 7 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik 8 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik 9 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Grundlage für Atomspektroskopie – freie Atome Atom: Kern und Hülle Elektron : Masse (Ruhemasse) me = 9.11 x 10-28 g Ladung (Elementarladung) e = 1. 602… x 10-19 C (As) Elektronenradius (klassisch) potentielle Energie re = 2.8 x 10-15 m Epot = - e² / 4πє0 r je weiter Elektron von Atomkern entfernt, umso größer ist potentielle Energie kinetische Energie Gesamtenergie E = Epot + Ekin Ekin= e² / 8πє0 r E = e4me / n² 8 h² є0² (auf n-ter Bahn) 10 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Atomemissionsspektrometrie 2 - Stufenprozess »Abklingen » Anregung h Energie Niedrigeres Niveau (E1) Höheres Niveau (E2) 11 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Energie – Übergang Elektron von mehr angeregtem Zustand n2 zu weniger angeregten Zustand n1 → Freisetzung von Energie Em – En = e4 me / n² 8 h² є0² [1/n1² - 1/n2²] = h Em – En = R [1/n1² - 1/n2²] = ’ = 1 / λ ’ Wellenzahl R (RH) RYDBERG –Konstante Einfachster Fall : Wasserstoffatom (Ein Elektron) Absorption eh Emission r + ω h 12 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Wasserstoffspektrum Basierend auf Erkenntnis des Seriencharakters der Spektren ’ = 1/λ = R [1/2² - 1/n2²] BALMER (1885) n2 = 3,4,5,…. der Termfomel = T2 - T1 = RH / 2² - RH / n² RYDBERG RYDBERG –Konstante RH = 109677 cm-1 der Bohr’schen Frequenzbedingung E a - Ee = h folgt: = Ea / hc - Ec / hc BOHR = R ( 1/ne2 - 1/na2 ) Serienformel 13 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Wasserstoff - Einelektronenspektrum 14 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle;Department Analytik für Balmer Serie na = 2 ne = 3 ’ = R (1 / 2² - 1/ 3²) ne = 4 ne = 5 ne = 6 ne = 7 ne = 8 → λ = 656 nm ’ = R (1 / 2² - 1/ 4²) → λ = 486 nm ’ = R (1 / 2² - 1/ 5²) → λ = 434 nm ’ = R (1 / 2² - 1/ 6²) → λ = 410 nm ’ = R (1 / 2² - 1/ 7²) → λ = 397 nm ’ = R (1 / 2² - 1/ 8²) → λ = 389 nm 15 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Wasserstoffähnliche Spektren z.B. He+ Li2+ Spektren ähnlicher Aufbau wie H = Z2 Ea / hc - Ec / hc = Z2 R ( 1/ne2 - 1/na2 ) Z : Kernladungszahl Spektroskopischer Verschiebungssatz SOMMERFELD und KOSSEL 16 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Spektren von Atomen mit mehreren Elektronen Grundlage für Beschreibung: Kenntnis des Atombaus, Elektronenkonfiguration (Orbitale) Basis: Quantenzahlen Hauptquantenzahl n ( n = 1,2,3,... ) definiert maximale Zahl der Elektronen, die sich in definiertem Abstand der „Schale“ vom Kern befinden (max. 2 n²) n=1: 2(1)²; n=2: 2(2)²=8; n=3: 2(3)²=18; n=4: 2(4)²=32; …. Bahndreh-Impuls (Neben-) Quantenzahl l ( l = 0,1,2,.., n-1 ) zu jeder Hauptquantenzahl n gehören einschließlich der Kreisbahn n Ellipsen unterschiedlicher Exzentrizität (Symmetrie der Orbitale, Knotenflächen eines Orbitals durch den Atom“Mittelpunkt“) SOMMERFELD Den l - Werten werden Buchstaben zugeordnet l=0 s sharp l=1 p principal l=2 d diffuse l=3 f fundamental Spin (Orientierungs-) Quantenzahl s ( + ½ und - ½ ) innere Quantenzahl j (j=l±s) Kopplung aus Bahndrehimpuls- und Spin-Quantenzahl zur Beschreibung des Gesamtdrehimpulses magnetische Quantenzahl m (m = + l ... - l) 17 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Aufbau der Elektronenniveaus (Terme) Basis: Die Energieniveaus werden in der Reihenfolge Elemente im Periodensystem mit Elektronen belegt. Diese Belegung erfolgt unter energetischem Aspekt. Jedes Energieniveau kann nur mit einem Elektron besetzt werden. Je 2 beliebige Elektronen eines Atoms müssen sich in mindestens einer Quantenzahl unterscheiden ! PAULI 18 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik In Atomspektroskopie wird der Elektronenzustand (Term) hauptsächlich durch n ; l und s bzw. j charakterisiert. Bahn - Impulsquantenzahl l (l = 0;1;2;…n-1) Eigendreh(Spin)- Impulsquantenzahl s (s = +½ und - ½) l und s koppeln zu j Gesamtdrehimpulsquantenzahl (innere Quantenzahl) j=│l+s│ RUSSEL - SAUNDERS Symbolik der Energieniveaus ergibt sich aus Nummer der Hauptquantenzahl und Kopplung zwischen den Impulsquantenzahlen der Valenzelektronen, sog. Termsymbole nm lj n: Hauptquantenzahl m: Multiplizität der Terme (m = 2 s + 1) l: Nebenquantenzahl in Großbuchstaben (historisch), S, P, D, F 19 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Elektronenkonfiguration für Mg 3d 4s 3p 3s e Mg 1s 2s2p e Nach Konvention: E = 0 für niedrigstes E-Niveau, 3s, i.e. Grundzustand 20 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Beispiele: Na im Grundzustand - Elektronenzahl = 11 n=1 2s Elektronen [He] n=2 2 s Elektronen + 6 p Elektronen n=3 1 s Elektron mit spin [1/2] [Ne] m = 2 s+1 = 2* (1/2) + 1 =2 I = 0 (da nur s Elektronen) S j = l ± s= 0 ± (1/2) = ½ nm lj 3 2S1/2 Mg im Grundzustand - Elektronenzahl = 12 [Ne] n= 3 2 s Elektronen mit spin s1 -1/2 und s2 + 1/2 m = 2 s+1 = 2* (0) + 1 =1 l = 0 (da nur s Elektronen) S j = l ± s= 0 ± 0 = 0 Σ (s1+s2) = 0 3 2S0 nm lj Al im Grundzustand - Elektronenzahl = 13 [Ne] n= 3 2 s Elektronen mit spin s1 -1/2 und s2 + 1/2 1 p Elektron mit s = [1/2] m = 2 s+1 = 2* (1/2) + 1 =2 l = 1 (da s und p Elektronen) P j = l ± s= 1 ± 1/2 = ½; 3/2 nm lj Σ (s1+s2) = 0 3 2P1/2, 3/2 21 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Elektronenbesetzung der Elemente Z Element Elektronenkonfig. Nm Term T0 2 He 1s2 3 Li [He] 2S1 2 2 2S1/2 4 Be [He] 2s2 1 2 1S0 5 B [He] 2s22p1 6 2 2P1/2 11 Na [Ne] 3s1 2 3 2S1/2 12 Mg [Ne] 3s2 1 3 1S0 13 Al [Ne] 3s23p1 6 3 2P1/2 20 Ca [Ar] 4s2 1 4 1S0 21 Sc [Ar] 3d14s2 10 4 5D4 22 Ti [Ar] 3d24s2 45 4 3F3 24 Cr [Ar] 3d54s1 504 4 7S3 25 Mn [Ar] 3d54s2 252 4 3S5/2 26 Fe [Ar] 3d64s2 210 4 5D3 64 Gd [Xe] 4f75d16s2 34320 5 9D2 (1s22s1) Nm Zahl der Mikrozustände; 22 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Beispiel: Na (Elektronenzahl 11) Grundzustand - angeregter Zustand → Spektrum Grundzustand [Ne] n=3 1 s – Elektron [s = ½] I=0 →S n m lj 3 2S1/2 angeregter Zustand [Ne] n=3 1 s – Elektron wurde auf 3 p – Niveau angehoben [Ne] n=3 1 p – Elektron [s = ½] m=2s+1 I=1 → P ….. m = 2 * ½ + 1 = 2 j = │l ± s │ ………. j = │1 ± ½ │ = 1 /2; 3 /2 Übergang 3 2S1/2 3 2P1/2 , 3/2 → 3 2P3/2 λ = 588.9950 nm 3 2S1/2 → 3 2P1/2 λ = 589.5924 nm 23 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Termschema für Na Kein „freier“ Übergang zwischen den Energie - Niveaus 24 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Absorptions- & Emissionsspektrum des Na 25 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Atomspektren : Elektronenübergang zwischen Energie-Niveaus Auswahlregeln allgemeine Auswahl-Regel für Entstehen einer Spektrallinie für Ein-Elektronensysteme n = 1, 2, 3 bei Mehrelektronensystemen n = 0, 1, 2, 3 bei Alkalispektren und mit (vielen Einschränkungen) bei allen anderen Mehrelektronensystemen gilt weiterhin l=1 bedingt durch Elektronenspin (line fine structure) Aufspaltung der Spektrallinien in eng beeinander liegende Energieniveaus Multiplizität Auswahl-Regel J = 0, 1 Na-Dublett Übergang vom 3 s- Niveau Grundzustand Na [Ne] 2S1/2 mit n = 0 nach 3 p - Niveau mit l = 1 und mit s = + ½ bzw. s = - ½ [Ne] 2P 3/2 [Ne] 2P 1/2 26 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Termschema des K - Atoms 27 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Emissionsspektrum des K – Atoms (350 – 435 nm) 28 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Departmen Analytik Emissionsspektrum des Sm – Atoms (350 – 435 nm) 29 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Spektren der Alkali - Elemente Na K Rb CsCs 30 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Mg Anregung Mg Mg* e M Mg K L e 31 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Mg ionization e M Mg K L e Mg Mg+ 32 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Mg+ excitation • Mg: 1s2 2s2 2p6 3s2 3p0 4s0 3d0 4p0… • Mg+: optical electron 1s2 2s2 2p6 3s1 3p0 4s0 3d0 4p0… • Mg+*: 1s2 2s2 2p6 3s0 3p1 4s0 3d0 4p0… 1s2 2s2 2p6 3s0 3p0 4s0 3d1 4p0… 33 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle; Department Analytik Atomspektren : Linienbreite Theoretische Linienbreite : „Null“ Spektrallinie ist genau definierter Elektronen – Übergang zwischen zwei energetischen Zuständen 34 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren : Linienbreite Natürliche Linienbreite Ursache : Unschärfe – Relationen Heissenberg Δχ Δ pχ „Über den anschaulichen Wert der quantentheoretischen Kinematik und Dynamik“ Z. Phys. (1927) 43, 172 ≥ h / 2π ≡ ħ Δχ Ungenauigkeit der Ortsbestimmung Δ pχ Ungenauigkeit des Impulses m v χ Ort und Impuls können nicht gleichzeitig exakt gemessen werden. Es besteht folglich auch Ungenauigkeit der Geschwindigkeit und Energie. Aus Energie (Δ E) – Zeit (Δ t) – Unschärfe ergeben sich Ausdrücke für spektroskopische Linienbreite, d.h. Unschärfe der Frequenz eines Elektronenüberganges ΔE Δt ≥ ħ ≡ h / 2π 35 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren : Linienbreite Natürliche Linienbreite Beispiel Übergang 4 2S1/2 → 4 2P3/2 Cu 324.755 nm ΔE* Δt ≥ ħ ≡ h / 2π Postulat: Atom bleibt für 10-8 s im angeregten Zustand ΔE* Δt E=h*ν = h / 2π h * Δ ν *Δ t = h / 2π Δ ν *Δ t = 1 / 2π Δ ν = 1/ 2π *10-8 s-1 = 1.59 *10 c= λ*ν nach Näherung ΔE=h*Δν 7 Δ t = 10-8 s s-1 Differenzieren → d ν = -1 c * λ² *Δ λ1/2 Δ λ1/2 = (Δ ν * λ² ) /c Δ λ1/2 = (1.59 * 107 s-1) (324 *10-9 m )² / 3 * 108 m s-1 = 5.6 *10-14 m = 0.0055 pm 36 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren : Linienbreite Linienverbreiterungen: Doppler - Verbreiterung 37 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren : Linienbreite Linienverbreiterungen: Doppler - Verbreiterung 38 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren : Linienbreite Linienverbreiterungen: Doppler - Verbreiterung Einflussgrößen: (Atom, Ionen) - Masse, Temperatur Geschwindigkeit eines Teilchens nimmt mit Quadratwurzel der Temperatur [T] zu Boltzmann Geschwindigkeit ist indirekt proportional zur Atommasse [m] ΔλD = ν / c (2RT / m)1/2 = 7.162 * 10-7 *λ0 (T/m)1/2 Beispiele: ΔλD *103 nm rel. Atommasse Cs Na Cu 133 23 63.6 λ0 852.1 589.0 324.8 T = 2000 K 2.4 3.9 1.3 T = 3000 K 2.9 4.8 1.6 39 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren : Linienbreite Linienverbreiterung : Doppler - Verbreiterung 40 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren : Linienbreite Linienverbreiterungen: Stoß- oder Druck- (Linien) Verbreiterung Druckerhöhung führt zu verstärkter Kollision ► elastische Stöße dabei wird keine Energie auf den Stoßpartner übertragen, es ändert sich aber die kinetische Energie, zusätzlich wird potentielle Energie (bei Annäherung des Partners) verändert → Linienverbreiterung abhängig von Druck, Temperatur, Masse der Stoßpartner Druckerhöhung führt zu verstärkter Kollision von Atomen mit gleichen Atomen Holtzmark elektrisch geladenen Teilchen Stark ungeladenen Teilchen van der Waals andersgearteten Spezies Lorentz ΔνStoß = Zahl der Stöße pro Sekunde / π ΔνStoß ≈ ΔνDoppler ► unelastische Stöße ca. 1 pm Anregungsenergie eines Atoms wird teilweise oder ganz auf Stoßpartner übertragen → Deaktivierung (angeregter Zustände ) oder strahlungsloser Übergang 41 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren : Linienbreite (historisch) Linienverbreiterungen: im elektrischen Feld Stark elektrisches Feld polarisiert Atom, dabei entsteht ein dem Feld proportionales Dipolmoment Beeinflussung des Eigendrehimpulses der Elektronen 42 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren : Linienbreite (historisch) Linienverbreiterungen: → im magnetischen Feld Zeeman Einfluss eines Magnetfeldes auf den Eletronenspin Richtunsquantelung des Elektronenspins im Magnetfeld Aufspaltung der Spektrallinie im Magnetfeld in 3 Komponenten Orientierung der resultierenden Komponenten mittlere Komponente hat andere Polarisierung als äußere Komponenten (diese sind gleich polarisiert) Abstand der Linien (Aufspaltung) ist direkt proportional der Magnetfeldstärke Es ergeben sich für Gesamtdrehimpulsquantenzahl J im Magnetfeld (2J + 1) Zustände 43 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren : Linienbreite (historisch) Linienverbreiterungen: im magnetischen Feld Zeeman normaler Zeeman – Effekt 44 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren : Linienbreite (historisch) Linienverbreiterungen: im magnetischen Feld Zeeman normaler Zeeman – Effekt Voraussetzung Singulett – System Gesamtspin S=0 L=J sog. „three-line pattern“ of normal Zeeman effect 45 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren : Linienbreite (historisch) Linienverbreiterungen: im magnetischen Feld Zeeman anormaler Zeeman – Effekt Na: 2S1/2 → 2P1/2 Na: 2S1/2 → 2P3/2 46 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren : Linienbreite Selbstabsorption - Linienumkehr Plasma ist nicht homogen → Temperaturgradient In „kalten“ Randzonen liegen Atome z.T. im „weniger angeregten“ Zustand vor z.B. im Grundzustand; bzw. sind weniger ionisiert → freie Atome (Ionen) können die aus den inneren Bereichen des Plasmas von angeregten Atomen (Ionen) emittierten Photonen absorbieren 47 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren : Linienbreite Selbstabsorption - Linienumkehr 48 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren : Linienbreite Selbstabsorption - Linienumkehr Konzentrationsabhängige Selbstumkehr der Emissionslinien Selbstumkehr kann zu separaten Linien führen Ursache: Die Emissionslinien haben größere Breite als Absorptionslinien; die freien Atome in „kalter Zone“ absorbieren vorwiegend Licht, dass ihrem Anregungspotential, d.h. der Mitte der Emissionslinie entspricht 49 →scharfe Absorptionslinie auf Untergrund verbreiteter Emissionslinie Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren : Linienbreite (historisch) Linienverbreiterungen: weitere Effekte extrem starke Magnetfelder ► Entkopplung von L und S von J anormaler Zeeman-Effekt wird aufgehoben und in normale Zeeman –Aufspaltung gewandelt Einfluss des a) Kernspins b) Isotopie (besonders „leichte Elemente“, z.B. Li, Ne auf Linienspektrum ► Hyperfeinstruktur der Linien 50 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik Atomspektren Literatur: theoretische Grundlagen: P.F.Bernath Spectra of Atoms and Molecules Oxford University Press, Oxford, 1995, ISBN 0-19-507598-6 H.Lindner Grundriß der Atom- und Kernphysik Fachbuchverlag Leipzig, 1988, ISBN 3-343-00449-9 G.Herzberg Atomic Spectra and Atomic Structure Dover Publications, New York, 1944. A. Sommerfeld Atombau und Spektrallinien Friedrich Vieweg & Sohn, Braunschweig, 1944 W.R.Hindmarsh Atomspektren Akademie-Verlag, Berlin, 1972 Lehrbücher der theoretischen Physik 51 Aufbaustudium "Analytik und Spektroskopie“ Umweltforschungszentrum Leipzig-Halle ; Department Analytik 52 Aufbaustudium "Analytik und Spektroskopie“