Nr.3 Liste Atommodelle 1 - FST
Werbung

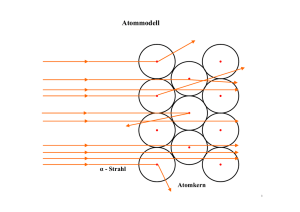
Fachschule für Technik Dipl.FL. D.Strache FST UH Fachschule für Technik Ein Atommodell ist eine Vorstellung von den kleinsten Teilen der Stoffe. Lange Zeit gab es keine experimentellen Hinweise für die Existenz kleinster Teilchen, sondern lediglich die intuitive Ablehnung unendlich fortsetzbarer Teilbarkeit, sowie die Möglichkeit, die vielfältigen Eigenschaften von Materialien und Substanzen auf kleinste Teilchen geringerer Zahl zurückzuführen. Grundlage der Modelle der Neuzeit sind beobachtbare Eigenschaften der Materie und experimentell ermittelte Daten. Auf die Frage, wie man sich denn ein Atom nun vorzustellen habe, antwortete der Physiker Werner Heisenberg: „Versuchen Sie es gar nicht erst!“ Die Formulierung der gängigen Atommodelle der Quantenmechanik bestehen vorrangig aus mathematischen Aussagen. Die folgende, chronologisch geordnete Liste gibt einen Überblick. Wichtige Modelle haben Hauptartikel. Aktuell gebräuchliche sind auch im Artikel Atom im Zusammenhang dargestellt. Dipl.FL D.Strache FST UH. Fachschule für Technik •Das Teilchenmodell von Demokrit (etwa 400 v. Chr.), •dieser postulierte die Existenz von verschiedenartigen festen, unteilbaren Teilchen, •die unterschiedlich kombiniert die bekannten Substanzen bilden. •Das Dalton-Modell (1803) geht von kleinsten, nicht weiter teilbaren Teilchen aus, die sich in ihrer •Masse unterscheiden und bei chemischen Reaktionen neu angeordnet und in •bestimmten Anzahlverhältnissen • miteinander verknüpft werden. •Im Dynamidenmodell (1903) von Philipp Lenard bestehen Atome zum größten Teil aus leerem Raum • zwischen kleinen, rotierenden elektrischen Dipolen, den Dynamiden. •Nach dem thomsonschen Atommodell (1903) besteht das Atom aus einer gleichmäßig verteilten •positiven Ladung und negativ geladenen Elektronen, die sich darin bewegen. • Dieses Modell wird auch als Plumpudding-Modell oder zu deutsch Dipl.FL Rosinenkuchenmodell bezeichnet. D.Strache FST UH. Fachschule für Technik • Im planetarischen Modell bzw. Saturnmodell von Nagaoka Hantarō (1904) ist das Atom eine große, positiv geladene Kugel, die von den negativ geladenen Elektronen umkreist wird. In Analogie zur Stabilität der Ringe des Saturns sagte das Modell einen sehr massereichen Kern voraus, sowie eine (nicht beobachtete) Energieabstrahlung durch die Bewegung der Elektronen. • Nach dem rutherfordschen Atommodell (1911) besteht das Atom aus einem positiv geladenen Atomkern, der nahezu die gesamte Masse des Atoms beinhaltet, und einer Atomhülle aus Elektronen. • Nach dem bohrschen Atommodell (1913) besteht das Atom aus einem positiv geladenen, massetragenden Kern und Elektronen, die diesen auf diskreten, als stabil postulierten Bahnen umkreisen. • Das bohr- sommerfeldsche Atommodell (1916) ist eine Erweiterung des bohrschen Atommodells, in dem auch bestimmte Ellipsenbahnen um den Atomkern zugelassen sind. • Nach dem Orbitalmodell (1928) besteht das Atom aus einem Kern, der von Orbitalen umgeben ist. Die Form der Orbitale ist durch die räumliche Aufenthaltswahrscheinlichkeit der Elektronen gegeben. Im strengen Sinn ist ein Orbital eine Lösung der Schrödingergleichung. Dipl.FL D.Strache Fachschule für Technik • Das Schalenmodell (Atomphysik) vereinfacht das Atom so, dass ein positiv geladener Atomkern von Kugelschalen umgeben ist, in denen sich die Elektronen befinden. Nur die jeweils äußerste Schale ist für die chemischen Eigenschaften des Elements verantwortlich. Über die Bewegung der Elektronen wird keine Aussage gemacht. • Das Kugelwolkenmodell (kimballsches Atommodell, Tetraedermodell) ist ein in der Schule häufig verwendetes Atommodell, welches eine Erweiterung des Schalenmodells darstellt. • In einigen Fällen können Atome als Punkte ohne Ausdehnung genähert werden, etwa beim Modell des idealen Gases, in anderen als Kugeln mit bestimmtem Volumen, etwa beim Van-der-Waals-Gas, das entsprechende Modell heißt auch Punktteilchen-Modell bzw. inkompressible KugelnModell. Dipl.FL D.Strache FST UH. Fachschule für Technik Es gibt auch Modelle, die sich ausschließlich mit dem Atomkern beschäftigen: • Das Tröpfchenmodell (1936) beschreibt den Atomkern als Tröpfchen einer geladenen Flüssigkeit. • Das Schalenmodell (1949) führt den Aufbau der Atomkerne auf quantenmechanische Gesetzmäßigkeiten (Pauli-Prinzip) zurück, hier wird den Nukleonen eine relative Bewegungsunabhängigkeit zugestanden Dipl.FL D.Strache 7 Fachschule für Technik Dipl.FL D.Strache FST UH. Fachschule für Technik Dipl.FL D.Strache FST UH.