Genmutationen sichern Therapieerfolg
Werbung

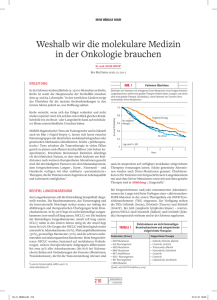
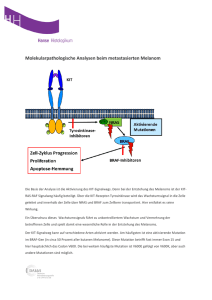
MOLEKULARE MEDIZIN Individualisierte Krebstherapie Genmutationen sichern Therapieerfolg Eigentlich gelten unkontrollierte Genmutationen als Krebsauslöser, aber beim nicht-kleinzelligen Bronchialkarzinom sind bestimmte Mutationen für das Therapieansprechen verantwortlich. Das Lungenkarzinom ist die dritthäu- therapie im Rahmen einer multimodalen im EGF-Rezeptor-Gen mit der Wirksam- figste Krebserkrankung und die häufigste Therapie Aussicht auf Heilung. Bei fort- keit eines speziellen Inhibitors (Gefitinib) Krebstodesursache in Deutschland. An geschrittenen Tumoren im Stadium IIIB korrelieren. Diese Mutationen sind bei nur der hohen Mortalität von etwa 50.000 pro und IV ist bislang die Chemotherapie die 5-20% der nicht-kleinzelligen Bronchial- Jahr bzw. 30% aller Krebssterbefälle hat Therapie der Wahl, doch lässt sich damit karzinome (NSCLC) nachweisbar, aber sich trotz hochspezialisierter chirurgischer meist keine wesentliche Verlängerung der immerhin sprechen ca. 70-75% der NS- Methoden und adaptierter Chemotherapie- Überlebenszeit erreichen. CLC-Tumoren mit einer EGFR-Mutation auf das neue Medikament an. Protokolle seit 1950 nichts Wesentliches Die Hoffnungen der Medizin liegen der- geändert. Doch neuerdings steht das nicht- zeit in zielgerichteten Therapien, die sich Erwartungsgemäß ist in unselektierten kleinzellige Bronchialkarzinom (NSCLC) gegen Wachstumsrezeptoren in der Tumor- Patientenkollektiven kein signifikanter im Fokus des therapeutischen Interesses. zellmembran richten. Man unterscheidet Vorteil einer TKI-Therapie nachweisbar, Mit einer Inzidenz von 40 pro 100.000 hochmolekulare blockierende Antikörper aber eine Subgruppe von Patienten, ins- Einwohner und Jahr macht es rund 70% al- gegen die extrazelluläre Domäne und klei- besondere Asiaten und Niemals-Raucher ne inhibierende sowie ein Teil der Patienten, bei denen eine Moleküle, die Platin-basierte Behandlung wirkungslos ins Innere der war, profitieren davon. Tu m o r z e l l e n eindringen kön- Gastkommentar nen und dort die TyrosinkinaseAktivität der intrazellulären Domäne hemmen. In beiden TMR = Transmembranregion Fällen kommt es zur Blocka- Abb. 1: Das nicht-kleinzellige Bronchialkarzinom (NSCLC) ist durch Mutationen de von wachs- des Wachstumsrezeptors EGFR gekennzeichnet. Es besteht eine Häufung tumsfördernden in zwei Abschnitten, nämlich in Exon 19 und Exon 21. Ein wichtiger Ansatz- Signalwegen. punkt für die individualisierte Therapie mit dem neuen Tyrosinkinasehemmstoff Gefitinib (Iressa) ist die L858R-Mutation im Exon 21. Man kennt heute etwa 500 ve r s c h i e d e n e ler Lungenkarzinome aus und umfasst die Tyrosinkinasen und über 100 potenzielle drei Untergruppen der Plattenepithelkarzi- Inhibitoren (TKI), die folglich nicht alle nome, Adenokarzinome und großzelligen streng spezifisch sein können. Im Fall des Karzinome. Nur in frühen Stadien besteht Lungenkrebses hat sich jedoch gezeigt, durch Operation, Bestrahlung und Chemo- dass spezielle aktivierende Mutationen 42 Trillium-Report 2010 8(1):42 Das Lungenkarzinom stellt trotz gewisser Therapiefortschritte im letzten Jahrzehnt mit einer Fünf-Jahres-Überlebensrate von nur 15% weiterhin eine ernste Prognose dar. Insbesondere zytotoxische Chemotherapeutika, die mittlerweile seit sechs Dekaden weiterentwickelt wurden, scheinen mit ihren begrenzten Therapieerfolgen eine Plateau-Phase zu erreichen. Vor dem Hintergrund dieser Erfahrungen weist die Individualisierung der Therapieauswahl anhand von klinischen, histologischen und molekularbiologischen Kriterien in die richtige Richtung. Sie hat mit dem gezielten Einsatz von Gefitinib bei aktivierenden EGFR-Mutationen das erste und bisher einzige Systemtherapeutikum in die klinische Anwendung gebracht, das in der Zulassung für die Therapie des nicht-kleinzelligen Lungenkarzinoms (NSCLC) mit einem positiven Biomarkernachweis verknüpft ist. Zwar betrifft die therapierelevante Mutation nur etwa 10% der NSCLC-Patienten, zumeist Nichtraucher mit Adenokarzinom, doch wird damit MOLEKULARE MEDIZIN Abb. 2: Der diagnostische Weg vom Primärtumor der Lunge (links) bis zum spezifischen Mutationsnachweis (rechts) führt über die histopathologische Charakterisierung. In der HE-Färbung erkennt man ein typisches Adenokarzinom mit weitgehender Verdrängung der Lungenbläschen durch zellreiches Tumorgewebe. Zum Immunphänotyp primär pulmonaler Adenokarzinome gehört u.a. die Expression von TTF1 (braune Granula). Am 24. Juni 2009 erhielt AstraZeneca die Zur Auswahl (Stratifizierung) geeig- Zulassung von Gefitinib (Iressa) für die ge- neter Patienten ist vor Behandlungsbe- samte Europäische Union zur Behandlung ginn eine gezielte Diagnostik durch den Für die Zukunft wird es wichtig sein, nicht-kleinzelliger Bronchialkarzinome Pathologen erforderlich. Sie beginnt mit sowohl primäre als auch sekundäre thera- mit aktivierenden EGFR-Mutationen. der Identifizierung und Mikrodissektion pierelevante Mutationen zur Stratifizierung Über 90% dieser Mutationen betreffen des Tumorgewebes nach adäquater histo- von Patientengruppen zu identifizieren, um einen kleinen Abschnitt des Gens, insbe- pathologischer Subtypisierung des Bron- mit der zielgerichteten individualisierten sondere in der ATP-bindenden Domäne chialkarzinoms. Anschließend erfolgt Therapie Erfolge zu erzielen sowie unnö- des Rezeptors (Abb. 1). eine DNA-Isolierung und Sequenzierung tige Nebenwirkungen und Kosten zu ver- (Abb. 2). meiden. Die molekularpathologischen Me- die Suche nach weiteren Biomarkern beflügelt. Hoffnungsvolle Kandidaten wie das eml/alkFusionsgen oder diverse Resistenzmarker für Chemotherapeutika und Tyrosinkinase-Inhibitoren werden derzeit in klinischen Studien auf ihre Anwendbarkeit überprüft. Der Befund des (Molekular-)Pathologen wird also künftig nicht nur für die Diagnosesicherung, sondern in zunehmendem Maß auch für die Therapieauswahl entscheidend sein. Das erfordert die interdisziplinäre Zusammenarbeit von Pneumologen, Radiologen, Onkologen, Strahlentherapeuten und Chirurgen. Hier steckt die Forschung noch in den Anfängen. Neben Mutationen, die die Wirksam- thoden dafür sind heute in ausreichendem keit der TKI-Behandlung erhöhen, wur- Maße vorhanden, und Ringversuche unter den im Krebsgenom auch Veränderungen dem Dach der Qualitätssicherungs-Initiati- entdeckt, die eine primäre oder sekundäre ve Pathologie (QuIP) stellen die für solche Therapie-Resistenz verursachen. Dazu Untersuchungen nötige hohe Qualifikation gehören zum Beispiel KRAS-Mutationen, der zertifizierten Pathologischen Institute die vorwiegend bei Rauchern, aber so gut sicher. wie nie in Kombination mit EGFR-Mutationen auftreten. Nach initial erfolgreicher Therapie können auch sekundäre Mutationen auftreten, die entweder das EGFR-Gen oder andere Signalkaskaden betreffen. Einige scheinen Resistenzen für Chemo- Priv.-Doz. Dr. med. Dipl.-Med. Mike Otto therapeutika zu vermitteln; Kandidaten Prof. Dr. med. Christopher Poremba hierfür sind zum Beispiel bei Taxanen Prof. Dr. med. Dr. phil. Jörg Kriegsmann das Klasse III Beta-Tubulin (TUBB3), Priv.-Doz. Dr. Martin Steins Prof. Dr. Michael Thomas Thoraxklinik Heidelberg bei platinhaltiger Chemotherapie ein Zentrum für Histologie, Zytologie und ERCC1-Polymorphismus und bei Gem- Molekulare Diagnostik ZHZMD Trier citabin eine RRM1-Überexpression. www.patho-trier.de Trillium-Report 2010 8(1):43 43