Übungen 10 zur Vorlesung Organische Chemie
Werbung
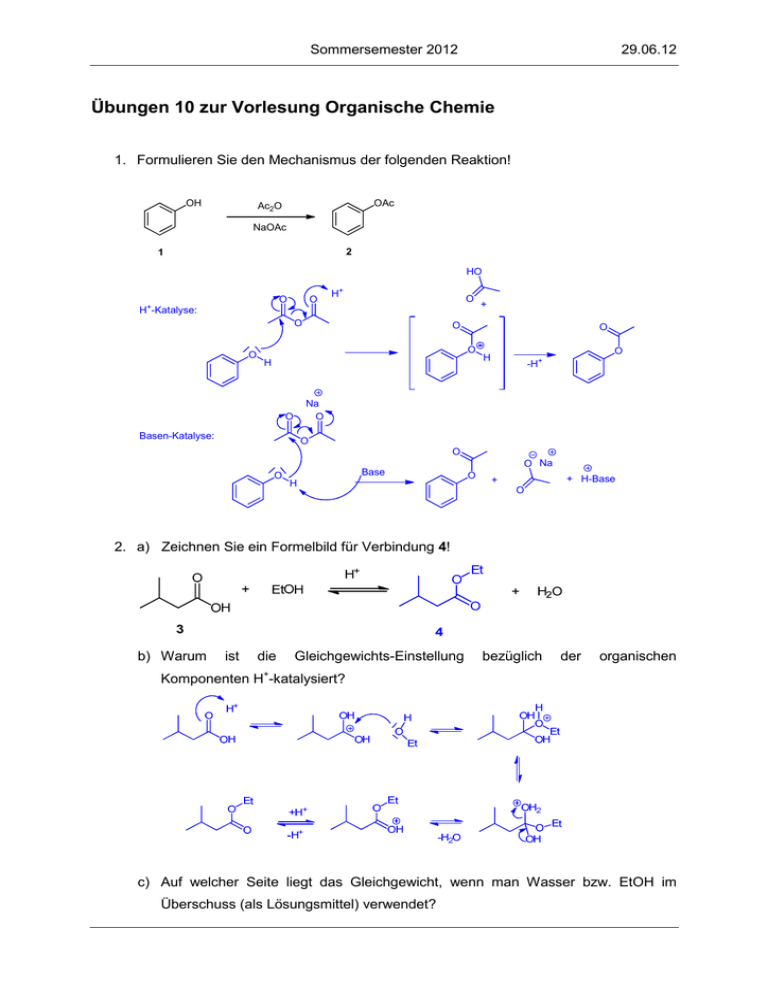
Sommersemester 2012 29.06.12 Übungen 10 zur Vorlesung Organische Chemie 1. Formulieren Sie den Mechanismus der folgenden Reaktion! OH OAc Ac2O NaOAc 2 1 HO O + O H+ O H -Katalyse: O O + O O O H O H -H+ Na O O Basen-Katalyse: O O O Base H O Na O + H-Base + O 2. a) Zeichnen Sie ein Formelbild für Verbindung 4! b) Warum ist die Gleichgewichts-Einstellung bezüglich der organischen Komponenten H+-katalysiert? c) Auf welcher Seite liegt das Gleichgewicht, wenn man Wasser bzw. EtOH im Überschuss (als Lösungsmittel) verwendet? Sommersemester 2012 29.06.12 EtOH als Lösungsmittel: Gleichgewicht auf Produktseite (Ester) Wasser als Lösungsmittel: Gleichgewicht auf Eduktseite (Säure) 3. An welchen Positionen kann Methylamin den Acrylsäureester 5 angreifen? Welche Produkte ergeben sich daraus? 4. Erklären Sie die folgende Umsetzung mechanistisch! Um was für eine Reaktion handelt es sich? O O MeO O H + 6 O MeO O OMe milde Base OMe O 7 8 O H Base MeO OMe O O O O milde Base O AldolAddition O OMe H OMe MeO MeO O OMe H H MeO O hohe Acidität mesomeriestabilisiertes Anion Base O Aldol-Kondensation bzw. Knoevenagel-Kondensation O OH MeO OMe AldolKondensation -H-Base/OH- 8 H OMe O MeO O