Ligandnamenstamm()
Werbung

ohne Anspruch auf Vollständigkeit,
dafür konsultiere man das „Red Book“ der IUPAC:
Connelly, Neil G.; Damhus Ture; Nomenclature of Inorganic Chemistry,
RSC Publishing IUPAC, Cambridge
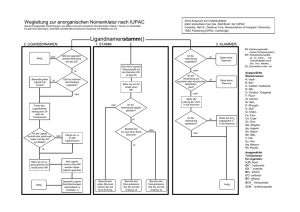
Wegleitung zur anorganischen Nomenklatur nach IUPAC
Zusammengesetzte Verbindungen wie Salze sind nach einzelnen Komponenten (Kation / Anion) zu behandeln.
Es gibt eine alternative, ebenfalls korrekte Benennung für Komplexe mit Metallen als ZA.
Ligandnamenstamm()
2. LIGANDENNAMEN:
fertig
nein
1. STAMM:
Gibt es Liganden?
(andere Elemente
als das ZA)
Ist die
Verbindung
ungeladen?
Das Atom (ausser
Wasserstoff) mit
der kleinsten EN
ist das ZA
ja
Behandle jeden
Ligand-Typ
einzeln
ja
3. KLAMMER:
Gibt es mehrere
verschiedene
Liganden?
Ist die
Verbindung ein
neutraler oder anionischer
Metallkomplex?
Ist der Ligand
neutral oder positiv geladen und das ZA
ein Metall?
ja
nein
Hänge ein -o
an den
Ligandnamen
Setze keine
Klammer
Setze die
Ladung der Verb.
in die Klammer
Ist die
Verbindung negativ
geladen?
Besteht das
Ion aus einer Sorte
Element?
ja
nein
nein
Finde den
Ligandnamen
analog zum ZA
oder als
Trivialnamen
Setze keine
Klammer
nein
Mehr als ein ZA
erhält einen
MP
nein
ja
Ist die
Verbindung
radikalisch?
ja
Setze die Anz.
ungepaarter e¯
in die Klammer
nein
nein
ja
ja
Mehr als ein Ligand gleicher Art
erhält einen MP
Alle Ligandnamen ohne MP
werden alphabetisch geordnet
fertig
Spezielle LigandKenntzeichungen:
verbrückend: μ
mehrfach: η
Benutze den
vollen Elementnamen des ZA
ohne Endung
Benutze den
Elementstamm
des ZA und die
Endung -id
Benutze den
Elementstamm
des ZA und die
Endung -at
fertig
EN: Elektronegativität
(siehe Periodensystem)
MP: Multiplikationspräfix
bi-, tri-, tetra-, … bei
Zweideutigkeit auch
bis-, tris-, tetrakis, …
ZA: Zentralatom oder -ion
Ausgewählte
Stammnamen:
H: HydrB: BorC: Carbid / Carbonat
N: NitrO: Oxid(o) / Oxigenat
F: FluorAl: AluminSi: SilicP: PhosphS: SulfCl: ChlorFe: FerrCu: CuprZn: ZincMo: MolybdAg: ArgentSn: StannSb: StibIr: IridAu: AurHg: MercurPb: PlumbAusgewählte
Trivialnamen
für Liganden:
H2O: aqua
OH¯: hydroxido
CN ¯: cyanido
NH3: ammin
CO: carbonyl
NO: nitrosyl
SCN¯: thiocyanato
SCN¯: isothiocyanato
Wegleitung zur alternativen Nomenklatur für Metallkomplexe (IUPAC)
Zusammengesetzte Verbindungen wie Salze sind nach einzelnen Komponenten (Kation / Anion) zu behandeln.
ohne Anspruch auf Vollständigkeit,
dafür konsultiere man das „Red Book“ der IUPAC:
Connelly, Neil G.; Damhus Ture; Nomenclature of Inorganic Chemistry,
RSC Publishing IUPAC, Cambridge
Ligandnamenstamm()
2. LIGANDENNAMEN:
1. STAMM:
3. KLAMMER:
Variante a mit
Ladungen oder Variante b
mit OZ?*
Das Atom (ausser
Wasserstoff) mit
der kleinsten EN
ist das ZA
ja
Behandle jeden
Ligand-Typ
einzeln
ja
Gibt es mehrere
verschiedene
Liganden?
ja
a
*b
Setze eine
Klammer und gib
die OZ in
römischen
Zahlen an
Setze eine
Klammer und gib
die Ladung in
arabischen
Zahlen an
fertig
fertig
Gibt es Liganden?
nein
nein
Finde den
Ligandnamen
(analog zum ZA
oder als
Trivialnamen)
ja
Ist der Ligand
anioisch?
*Variante b mit OZ ist nicht mehr
von der IUPAC empfohlen.
Mehr als ein ZA
erhält einen
MP
ja
Hänge ein -o
an den
Ligandnamen
Ist die
Verbindung negativ
geladen?
nein
nein
nein
Mehr als ein Ligand gleicher Art
erhält einen MP
Alle Ligandnamen ohne MP
werden alphabetisch geordnet
fertig
Spezielle LigandKenntzeichungen:
verbrückend: μ
mehrfach: η
Ist die
Verbindung negativ
geladen?
ja
Benutze den
Elementstamm
des ZA und die
Endung -at
Benutze den
vollen Elementnamen des ZA
ohne Endung
Benutze den
Elementstamm
des ZA und die
Endung -id
EN: Elektronegativität
(siehe Periodensystem)
MP: Multiplikationspräfix
bi-, tri-, tetra-, … bei
Zweideutigkeit auch
bis-, tris-, tetrakis, …
ZA: Zentralatom oder –ion
OZ: Oxidationsstufe
Ausgewählte
Stammnamen:
H: HydrB: BorC: Carbid / Carbonat
N: NitrO: Oxid(o) / Oxigenat
F: FluorAl: AluminSi: SilicP: PhosphS: SulfCl: ChlorFe: FerrCu: CuprZn: ZincMo: MolybdAg: ArgentSn: StannSb: StibIr: IridAu: AurHg: MercurPb: PlumbAusgewählte
Trivialnamen
für Liganden:
H2O: aqua
OH¯: hydroxido
CN ¯: cyanido
NH3: ammin
CO: carbonyl
NO: nitrosyl
SCN¯: thiocyanato
SCN¯: isothiocyanato
Alphabetische Ordnung für anorganische Nomenklatur
In Formeln
Atomsymbole werden generell alphabetisch geordnet, kürzere vor längeren (N3- vor NO)
kleine Zahlen vor grossen (NO2- vor NO3-) und kleinere Ladungen vor grösseren.
Innerhalb der Gruppen der Kationen (zurerst), der Anionen (nachfolgend) wird eine
alphabetische Ordndung eingehalten:
(Doppelsalz mit Cl- und O2-)
(mit dem mehratomigen anion OCl-,
Oxidochlorat(1–))
BiClO
NaOCl
KNa4Cl(SO4)2
CaTiO3
Ausnahmen können sind nur zulässig, falls sich falsche strukturelle Information daraus
ableiten liesse. So schreibt man das Persovskit-artige Mineral vom Typ ABO3
SrFeO3
Komplexe werden als eine Einheit betrachtet und folgen strikt der alphabetischen
Ordnung:
[CrCl2(NH3)2(OH2)2]
(Cl, N, O – beachte, dass das komplexierende Atom
an der Position am nächsten zum Zentralion steht.)
In Namen
Innerhalb der Gruppen der formal elektropositiven (zuerst) und formal elektronegativen
Elementen (nachfolgend) wird eine alphabetische Ordndung eingehalten, die nicht
immer mit jener Formel übereinstimmt:
Kaliummagnesiumfluorid
Bismutchloridoxid
Zinkhydroxidiodid
Eisenstrontiumoxid
KMgF3
BiClO
ZnI(OH)
SrFeO3 (siehe oben)
Multiplikatoren von Liganden werden bei der alphabetischen Ordnung nicht
berücksichtigt. Sollte der Mulitplikand aber Teil des Ligandnamen sein, dann wird er
wohl berücksichtigt:
K[AuS(S2)]
[CrCl2(NH3)4]+
Kalium(disulfido)sulfidoaurat(1-)
Tetraammindichloridochrom(1+)
Beispiele zur anorganischen Nomenklatur nach IUPAC
Verbindung
H
O
IUPAC Name
{Variante für Metallkomplexe}
Varianten a und b
Oxidan
Vairante
(Veraltet)
Dioxidan
Diwasserstoffperoxid
Bis(hydridosauerstoff)(O-O)
(Wasserstoffperoxid)
(Wasserstoffsuperoxid)
Hydridodisauerstoff(•)
Dioxid(•1-)
Dioxidokohlenstoff
Dihydroxidooxidokohlenstoff
Dioxidanyl
Superoxid
Kohlendioxid
(Kohlensäure)
Hydroxidodioxidocarbonat(1-)
Hydrogencarbonat
(Bicarbonat)
Trioxidocarbonat(2-)
Carbonat
Oxidostickstoff(•)
H
H
O
O
H
HOO•
O2•–
O
C
O
OH
Diwasserstoffoxid
(Wasser)
C
HO
O
O
-
C
HO
O
-
O
O
C
-
O
N
O
Dioxidostickstoff(•)
N
OH
Hydroxidooxidostickstoff
Stickstoffmonoxid
(nitric oxide)
Stickstoffdioxid
(nitrous oxide)
(Salpetrige Säure)
N
O
Dioxidonitrat(1-)
Nitrit
(Hydridodioxido)oxidostickstoff
(Persalpetrige Säure)
Dioxidooxidonitrat(1-)
Peroxynitrit
Hydroxidodioxidostickstoff
(Salpetersäure)
N
O
O
O
-
O
OH
N
O
O
O
N
-
O
O
Trioxidonitrat(1-)
N2O
NO3•
(2 Isomere, trigonal und linear)
NH2-N=NH-NH-NH2
O
HO
S
-
Oxidodistickstoff
Trigonal: Trioxidostickstoff(•)
Linear: (Dioxido)oxidostickstoff(•)
Dihydroxidodioxidoschwefel
Pentaaz-2-en
Schwefelsäure
Tetraoxidosulfat(2-)
Sulfat
O
OH
O
O
Nitrat
S
O
-
O
O
O
-
µ-Dioxido-1κO,2κO’-bis
O (trioxidosulfate)(2-)
O
-
O
S
S
O
O
O
O
O
S
Bis(dioxidosulfat)(S-S)(2-)
(Dithionit)
Chloridobrom
Difluoridosauerstoff
Bromchlorid
Sauerstoffdifluorid
S
-
O
O
Cl Br
O
F
µ-Peroxido-1κO,2κO’-bis
(trioxidosulfate)(2-)
Peroxodisulfat
F
K4[Fe(CN)6]
K4[Ni(CN)4]
[Co(NH3)6]Cl(SO4)
[Co(NH3)6][Co(CN)6]
[CoCl(NH3)5]2+
[Fe(CO)4]2[Co(NH3)5NO2]2+
[Co(NH3)5(ONO)]2+
Tetrakaliumhexacyanidoferrat
a:{Kaliumhexacyanidoferrat(4-)}
b:{Kaliumhexacyanidoferrat(II)}
Tetrakaliumtetracyanidonickelat
a:{Kaliumtetracyanidonickelat(4-)}
b:{Kaliumtetracyanidonickelat(0)}
a:Hexaammincobalt(3+)chloridsulfat
b:Hexaammincobalt(III)chloridsulfat
a: Hexammincobalt(3+)hexacyanidocobaltat(3-)
b: Hexammincobalt(III)hexacyanidocobaltat(III)
a: Chloridopentaammincobalt(2+)
b: Chloridopentaammincobalt(III)
a: Tetra(oxidokohlenstoff)ferrat(2-)
b: Tetra(oxidokohlenstoff)ferrat(-II))
a: Pentaamminnitrito-κN-cobalt(2+)
b: Pentaamminnitrito-κN-cobalt(III)
a: Pentaamminnitrito-κO-cobalt(2+)
b: Pentaamminnitrito-κO-cobalt(III)
Tetracarbonylferrat(II)
AsO43SeO32S42-
O
-
-
O
O
Si - Si
O
O
O O
NaTl(NO3)2
AlK(SO4)•12H2O
2 H
SiH3OH
Tetraoxidoarsenat(3-)
Trioxidoselenat(2-)
Tetrasulfid(2-)
µ-Oxidobis(trioxido)silikat(6-)
Natriumnitrattellurid
Aluminiumkaliumsulfat-Wasser(1/12)
[2H]Hydrid
Silanol
Deuterid