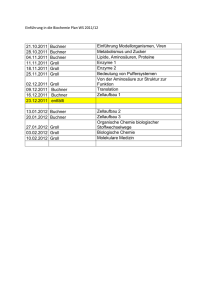
Carfilzomib
Werbung

Pharmazeutische Chemie - Carfilzomib Carfilzomib (Kyprolis®) Carfilzomib ist ein weiterer Proteasom-Inhibitor, der zur Behandlung des Multiplen Myeloms zugelassen ist (Strukturformel s. Abbildung 1). Der Arzneistoff ist als Pulver zur Herstellung einer Indusionslösung unter dem Namen Kyprolis® im Handel. Indiziert ist Carfilzomib in Kombination mit Lenalidomid und Dexamethason bei erwachsenen Patienten, die mindestens eine vorangehende Therapie erhalten haben. Ein Behandlungszyklus mit den drei Arzneistoffen entspricht 28 Tagen (4 Wochen), wobei Carfilzomib jeweils an den ersten zwei Tagen einer Behandlungswoche als zehnminütige Infusion appliziert wird. In der vierten Woche des Behandlungszyklus wird eine Pause eingelegt, so dass Carfilzomib an den Tagen 1, 2, 8, 9, 15 und 16 verabreicht wird und in den Tagen 17 - 28 keine Applikation erfolgt. Ab dem 13. Behandlungszyklus entfallen die CarfilzomibInfusionen an den Tagen 8 und 9. Die Anfangsdosis beträgt 20 mg/m2 (maximal 44 mg Carfilzomib pro Infusion). Wird diese Dosis toleriert, so wird ab Tag 8 des 1. Behandlungszyklus auf 27 mg/m2 erhöht (maximal 60 mg Carfilzomib pro Infusion). Die Behandlung kann bis zur Progression oder bis zum Auftreten nicht tolerierbarer Toxizitäten fortgesetzt werden, wobei die Datenlage für eine über 18 Behandlungszyklen hinausgehende Behandlung begrenzt ist und nur unter individueller Nutzen-Risiko-Abwägung für den Patienten erfolgen sollte (Jakubowiak 2014, Fachinformation Kyprolis® 2015). Abbildung 1 Carfilzomib ist nach Bortezomib, das bereits im Jahr 2004 zur Behandlung des Multiplen Myeloms zugelassen wurde, der zweite in Deutschland verfügbare Proteasom-Inhibitor. Beide Inhibitoren sind Peptide, sie unterscheiden sich aber dennoch stark in ihrer Struktur (und somit natürlich in ihrem Wirkmechanismus) (s. Tabelle 1). Arzneistoff (Fertigarzneimittel) Markteinführung Struktur Wirkmechanismus Bortezomib (Velcade®) 2004 Dipeptid Borsäure-Derivat Reversibler, nichtselektiver Proteasom-Inhibitor Carfilzomib (Kyprolis®) 2016 Tetrapeptid Epoxyketon irreversibler, selektiver Proteasom-Inhibitor Tabelle 1: In Deutschland verfügbare Proteasom-Inhibitoren 1 CA 6.2.2016 Pharmazeutische Chemie - Carfilzomib Bortezomib ist ein synthetisches Dipeptidyl-Borsäure-Derivat (s. Abbildung 2), das die Chymotrypsin- sowie die Caspase-ähnliche Aktivität (CT-L und C-L) des 20SProteasoms hemmt. Die Trypsin-ähnliche Aktivität (T-L) des 20S-Proteasoms wird erst bei höheren Bortezomib-Konzentrationen gehemmt (Kubiczkova et al. 2014, Accardi et al. 2015). Eine Kristallstruktur des Bortezomibs mit dem Hefe-20SProteasom ist verfügbar (Groll et al. 2006) und zeigt, dass Bortezomib mittels seiner Borsäure-Partialstruktur kovalent über die Hydroxyl-Gruppe des Threonins an Position 1 im aktiven Zentrum an das Proteasom bindet. Das tetraedrische BorsäureAddukt wird zusätzlich durch mehrere Wasserstoff-Brücken (u.a. mit Glycin 47) stabilisiert. Das Bortezomib-Proteasom-Addukt ist dadurch sehr stabil aber nicht irreversibel. Vielmehr handelt es sich bei der Bildung des Addukts um eine reversible Reaktion, die gekennzeichnet ist durch eine geringe Dissoziationsrate. Dadurch bleibt das Addukt für mehrere Stunden stabil (Groll et al. 2006, Miller et al. 2013, Kubiczkova et al. 2014). Abbildung 2: Strukturformel des Bortezomibs sowie des „langsam“ reversiblen BortezomibProteasom-Adduktes nach Groll et al. 2006. Im Gegensatz zum Bortezomib ist Carfilzomib ein lineares Tetrapeptid. Die BorsäureStruktur fehlt, stattdessen liegt eine α,β-Epoxyketon-Funktion vor. Als Ausgangspunkt für die Entwicklung des Carfilzomibs diente das natürlich vorkommende Epoxomicin, das zur Gruppe der Epoxyketonpeptide gehört und erhebliche Antitumoreigenschaften aufweist (s. Abbildung 3) (Hanada et al. 1992). Abbildung 3: Strukturvergleich des Carfilzomibs mit tetrapeptidischer Epoxyketon-Struktur sowie des natürlich vorkommenden Epoxomicins als Ausgangspunkt für dessen Entwicklung 2 CA 6.2.2016 Pharmazeutische Chemie - Carfilzomib Allerdings war das Interesse am Epoxomicin als potenzielle Leitstruktur für die Entwicklung eines Zytostatikums anfangs eher gering, wahrscheinlich wegen seiner Peptidstruktur sowie der labilen Epoxyketon-Funktion. Zudem war der Wirkmechanismus zur damaligen Zeit nicht bekannt. Das änderte sich allerdings, nachdem das Proteasom als Target ausgemacht werden konnte und zusätzlich noch eine sehr hohe Selektivität für das Proteasom gegenüber anderen Serin-Proteasen entdeckt wurde. Andere damals bekannte Proteasom-Inhibitoren - wie z.B. Bortezomib - zeigten diese Selektivität nicht (Sin et al. 1999). Wie ist diese Proteasom-Selektivität des Epoxomicins und damit die des Carfilzomibs zu erklären? Auch hier lieferte eine Kristallstruktur im Komplex mit dem 20SProteasom die Erklärung (s. Abbildung 4) (Groll et al. 2000). Abbildung 4: irreversible Bildung des Carfilzomib-Proteasom-Adduktes durch doppelten nukleophilen Angriff des N-terminalen Threonins des Proteasoms (nach Kim und Crews 2013) 3 CA 6.2.2016 Pharmazeutische Chemie - Carfilzomib Genauso wie Bortezomib binden die Epoxyketone an das N-terminale Threonin des 20S-Proteasoms. Die Aminosäure agiert dabei aber als „doppeltes“ Nukleophil, indem sowohl die Hydroxyl-Gruppe der Seitenkette als auch die freie Amino-Gruppe das elektrophile α,β-Epoxyketon angreifen. Das Resultat dieser irreversiblen Reaktion ist die Bildung eines sechsgliedrigen Morpholin-Ringes. Die Selektivität kommt daher, dass eben nur N-terminal nukleophile Proteasen wie das Proteasom mit seinem N-terminalen Threonin diese Reaktion mit den Epoxyketonen eingehen können, andere Proteasen reagieren nicht (Kim und Crews 2013). Carfilzomib bindet irreversibel an die Chymotrypsin-ähnliche Aktivität des Proteasoms, hohe Konzentrationen hemmen auch die Trypsin- und Caspaseähnliche Aktivität (Demo et al. 2007, Kubiczkova et al. 2014). Zahlreiche weitere Proteasom-Inhibitoren befinden sich derzeit in der klinischen Prüfung. Ein Nachteil der beiden Proteasom-Hemmer Bortezomib sowie Carfilzomib ist deren schlechte orale Bioverfügbarkeit, weshalb beide parenteral (i.v.) appliziert werden müssen. Abbildung 5: Zwei neue, peroral bioverfügbare Proteasom-Inhibitoren, die derzeit in der klinischen Prüfung sind Ixazomibcitrat befindet sich derzeit in der klinischen Prüfung und ist für eine perorale Applikation vorgesehen. Es ist ein Prodrug, das im Plasma schnell zu seiner aktiven Wirkform, dem freien Borsäure-Analogon und reversibel wirksamen ProteasomInhibitor Ixazomib, hydrolisiert wird (s. Abbildung 5). Eine Weiterentwicklung des Carfilzomib ist das Epoxyketon Oprozomib, das auch peroral bioverfügbar ist und wie Carfilzomib irreversibel an CT-L-Untereinheit des Porteasoms bindet (s. Abbildung 5) (Miller et al. 2013, Kubiczkova et al. 2014, Accardi et al. 2015). Literatur: Accardi, F. et al. Biomed Res Int 2015, 2015:172458 4 CA 6.2.2016 Pharmazeutische Chemie - Carfilzomib Demo, S.D. et al. Cancer Res 2007, 67, 6383 Fachinformation Kyprolis® 2015, Amgen Europe B.V. Groll, M. et al. J Am Chem Soc 2000, 122, 1237 Groll, M. et al. Structure 2006, 14, 451 Hanada, M. et al. J Antibiot (Tokyo) 1992, 45, 1746 Jakubowiak, A.J. Cancer Treat Rev 2014, 40, 781 Kim, K.B. und Crews, C.M. Nat Prod Rep 2013, 30, 600 Kubiczkova L. et al. J Cell Mol Med 2014, 18, 947 Miller, Z. et al. Curr Pharm Des 2013, 19, 4140 Sin, N. et al. Bioorg Med Chem Lett 1999, 9, 2283 5 CA 6.2.2016