Thieme: Taschenlehrbuch Biochemie
Werbung
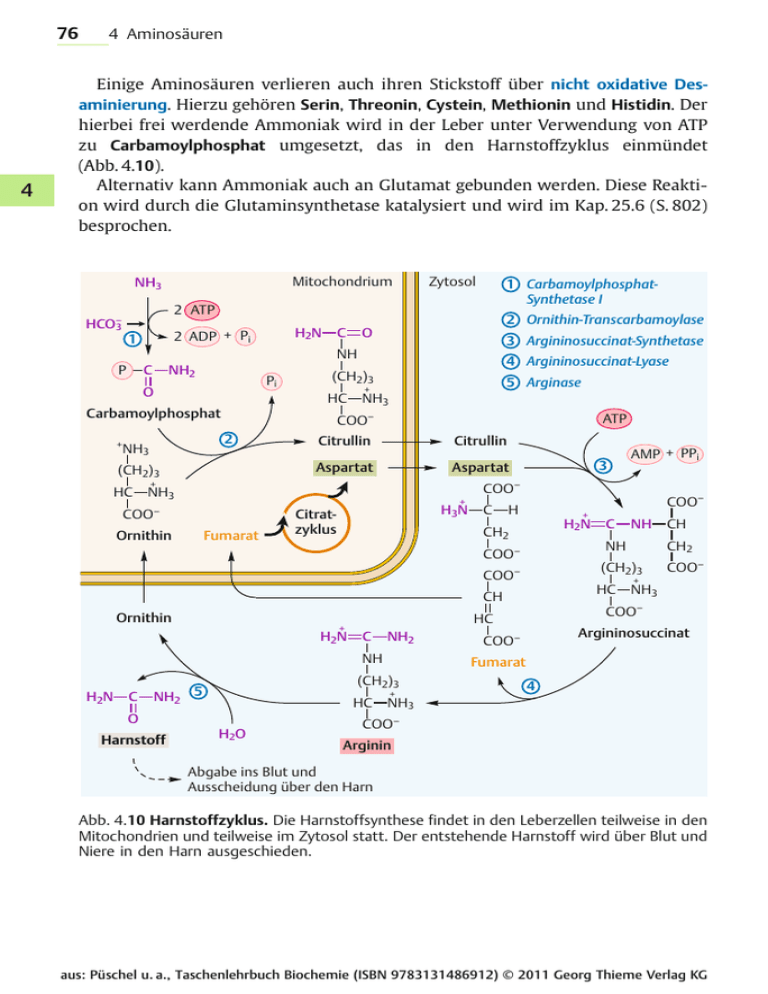
76 4 4 Aminosäuren Einige Aminosäuren verlieren auch ihren Stickstoff über nicht oxidative Desaminierung. Hierzu gehören Serin, Threonin, Cystein, Methionin und Histidin. Der hierbei frei werdende Ammoniak wird in der Leber unter Verwendung von ATP zu Carbamoylphosphat umgesetzt, das in den Harnstoffzyklus einmündet (Abb. 4.10). Alternativ kann Ammoniak auch an Glutamat gebunden werden. Diese Reaktion wird durch die Glutaminsynthetase katalysiert und wird im Kap. 25.6 (S. 802) besprochen. NH3 Mitochondrium Zytosol 1 CarbamoylphosphatSynthetase I 2 ATP HCO–3 H2N 2 ADP + Pi 1 C 2 Ornithin-Transcarbamoylase O 3 Argininosuccinat-Synthetase NH C P NH2 Pi O HC Carbamoylphosphat + (CH2)3 HC 5 Arginase + NH3 COO– 2 NH3 4 Argininosuccinat-Lyase (CH2)3 ATP Citrullin Citrullin Aspartat Aspartat + – Ornithin Fumarat + H3N Citratzyklus C COO– H + H2N CH2 COO + H2N HC NH2 NH C O Harnstoff HC H2O CH2 COO– + NH3 Argininosuccinat COO– Fumarat (CH2)3 NH2 5 CH COO– HC C NH (CH2)3 – CH Ornithin C NH COO– H2N AMP + PPi COO– NH3 COO 3 + 4 NH3 COO– Arginin Abgabe ins Blut und Ausscheidung über den Harn Abb. 4.10 Harnstoffzyklus. Die Harnstoffsynthese findet in den Leberzellen teilweise in den Mitochondrien und teilweise im Zytosol statt. Der entstehende Harnstoff wird über Blut und Niere in den Harn ausgeschieden. aus: Püschel u. a., Taschenlehrbuch Biochemie (ISBN 9783131486912) © 2011 Georg Thieme Verlag KG 4.2 Stoffwechsel der Aminosäuren 77 Harnstoffzyklus Der Hauptanteil der Stickstoffausscheidung beim Menschen erfolgt über Harnstoff (ca. 30 g pro Tag). Die Stickstofffixierung und -ausscheidung in Form von Harnstoff dient der Entgiftung, da Ammoniak ein starkes Zellgift ist und auf diese Art und Weise entsorgt wird. Der Harnstoffzyklus (Ornithinzyklus) läuft vorrangig in Leberzellen ab, in geringem Maße auch in der Niere. In der Zelle sind die Enzyme des Harnstoffzyklus teils in den Mitochondrien, teils im Zytosol lokalisiert. Den Transport der Intermediate durch die Membranen besorgen spezielle Transportproteine. Zuerst wird der Ammoniak in der Mitochondrienmatrix aus Glutamat freigesetzt. Er reagiert dort mit 2 ATP und Bicarbonat zu Carbamoylphosphat, die Reaktion wird durch die Carbamoylphosphat-Synthetase katalysiert. Es existiert noch eine zytosolische Carbamoylphosphat-Synthetase II, die unter Verwendung von Glutamin Carbamoylphosphat für die Pyrimidinbasensynthese bereitstellt. Dieses Enzym enthält eine zusätzliche Glutaminase-Domäne (s. Kap. 12.1.5, S. 339). Nun beginnt der eigentliche Zyklus (Abb. 4.10): ● Das Carbamoylphosphat reagiert mit der nicht proteinogenen Aminosäure Ornithin (das der Aminosäure Lysin ähnelt, jedoch eine CH2-Gruppe weniger enthält) zu Citrullin (Enzym: Ornithin-Carbamoyltransferase). ● Mithilfe des Antiporters ORNT 1 wird Citrullin aus dem Mitochondrium ins Zytosol und Ornithin aus dem Zytosol in das Mitochondrium transportiert. ● Citrullin reagiert im Zytosol mit der Aminogruppe von Aspartat unter ATPVerbrauch zu Argininosuccinat, wodurch der zweite Aminostickstoff für den Harnstoff eingeführt wird (Enzym: Argininosuccinat-Synthetase). ● Unter Fumarat-Abspaltung entsteht aus Argininosuccinat Arginin (Enzym: Argininosuccinat-Lyase; Aspartatzyklus). ● Mithilfe des Enzyms Arginase werden daraus Harnstoff und Ornithin gebildet. ● Ornithin wird nun wieder in das Mitochondrium transportiert, womit sich der Kreislauf schließt. Harnstoff selbst ist sehr gut wasserlöslich, wird über den Blutkreislauf in die Niere transportiert und dort in den Harn ausgeschieden. Die Werte der Harnstoffkonzentration im Blutplasma liegen in der Regel im Bereich von 100 – 500 mg/l. Die Synthese von Harnstoff ist energieaufwendig, es wird das Äquivalent von 4 Mol ATP pro Mol Harnstoff verbraucht. Dieser Energieverbrauch wird jedoch durch den Energiegewinn der mit dem Harnstoffzyklus assoziierten Reaktionen weitgehend kompensiert. So wird im Harnstoffzyklus aus Aspartat Fumarat gebildet, das im Citratzyklus über Malat zu Oxalacetat führt, aus dem durch Transaminierung wieder Aspartat entsteht. Dabei wird in der Malat-Dehydrogenase- aus: Püschel u. a., Taschenlehrbuch Biochemie (ISBN 9783131486912) © 2011 Georg Thieme Verlag KG 4