Die SSS-Regel - kienzlers
Werbung

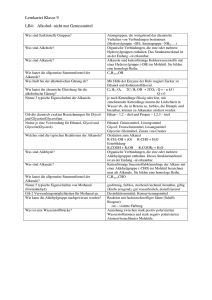
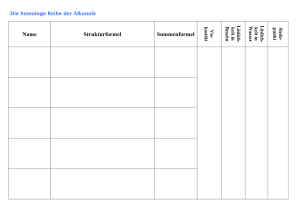
„Organische Chemie mit funktionellen Gruppen“ Name: Klasse: Datum: Wir haben die Bedeutung von „funktionellen Gruppen“ besprochen. Bei den Alkoholen („Alkanole“) ist dies die „Hydroxylgruppe“ ( - OH ). Welche Eigenschaften diese Hydroxylgruppe bewirkt, lässt sich insbesondere auch bei den Eigenschaften (hier im Beispiel: Löslichkeit) erkennen: Die SSS-Regel (von lat. „similia similibus solvuntur“ = „Gleiches löst sich in gleichem“) Löslichkeit von Alkoholen Alkohol – ein so genanntes _____________ Teilchen – kann sich sowohl in Wasser als auch in einem Kohlenwasserstoff (hier im Beispiel: Hexan) lösen! Der Grund liegt darin, dass sich im Alkoholteilchen (in der Abbildung unten) sowohl eine ____________ Gruppe (die Hydroxylgruppe), als auch ein unpolarer Anteil (der __________-Rest) vereinigen! Somit finden wir innerhalb des Alkoholteilchens eine „wasserfreundliche“ (= ______________) Gruppe, als auch einen Teil, der eine große Verwandtschaft zu den Kohlenwasserstoffen (in der Abbildung links oben) aufweist. Dieser Teil ist wasserabweisend (Wasser und Kohlenwasserstoffe lassen sich nicht ineinander lösen!) – man sagt er ist __________________. Bei höheren Alkoholen* lässt die Löslichkeit in Wasser dann mehr und mehr nach! Erkläre warum: _____________________________________________________________________ _________________________________________________________________________________ _________________________________________________________________________________ Fremdworterläuterungen: Lippos = „das Fett“, Hydros = „das Wasser“, phil = griech.: „Freund“, phobie = griech.: „Abneigung gegen“ * Unter „höhere Alkanole“ versteht man Alkohole mit längeren Kohlenwasserstoffketten! RS Rottweil Chemie Kienzler