Chemie für Biologen-VL12
Werbung

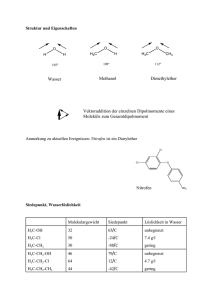
Chemie für Biologen WS 2005/6 Arne Lützen Institut für Organische Chemie der Universität Duisburg-Essen (Teil 12: Organische Chemie – funktionelle Gruppen) Die funktionelle Gruppe von Alkoholen und Phenolen H3C H2 C C H2 H2 C C H2 H2 C OH OH Alkanol R = Alkylrest 1-Hexanol OH = Hydroxygruppe H H C C H3C C R OH OH C OH C C H H p-Kresol Ar OH Phenol Ar = Arylrest Alkohole und Phenole sind funktionalisierte Alkane bzw. Arene. Sie sind Derivate des Wassers, H2O, bei dem ein H-Atom durch einen Alkyl- bzw. Arylrest ersetzt wurde. Wasserlöslichkeit von 1-Alkanolen R−OH R CH3 C2H5 C3H7 C4H9 Name Methanol Ethanol Propanol Butanol Gew. % ∞ ∞ ∞ 7.9 R C5H11 C6H13 C7H15 C8H17 Name Pentanol Hexanol Heptanol Octanol Gew. % 2.3 0.6 0.2 0.05 blau: hydrophiler Molekülteil rot: hydrophober Molekülteil Mit der Größe von R nimmt der hydrophobe Anteil zu und damit sinkt die Wasserlöslichkeit. Nomenklatur der Alkohole Systematischer Name: Alkanol H3C OH Methanol Methylalkohol H3C CH2 OH Ethanol Ethylalkohol H3C CH2 CH2 OH 1-Propanol n-Propylalkohol H3C CH CH3 2-Propanol Isopropylalkohol 2-Methyl-1-propanol Isobutylalkohol Phenylmethanol Benzylalkohol OH H3C CH CH2 OH CH3 CH 2 OH Glykole und Glycerine, Diole und Triole Glykole (2 OH-Gruppen) CH 2 CH 2 OH H3 C CH CH 2 OH OH OH Ethylenglykol 1,2-Ethandiol Propylenglykol 1,2-Propandiol H H CH 2 CH 2 CH 2 OH OH OH OH Trimethylenglykol cis-1,2-Cyclopentandiol 1,3-Propandiol Glycerine (3 OH-Gruppen) CH2 CH CH2 OH OH OH Glycerin 1,2,3-Propantriol Glycerin ist der Alkohol-Bestandteile der Fette. Fette sind Glycerin-Ester der Fettsäuren = „Triglyceride“. Glykole und Glycerine sind sehr gut wasserlöslich. Phenole OH OH OH α β OH α1 β 2 3 4 1-Naphthol (α-Naphthol) Phenol 2-Naphthol (β-Naphthol) NO2 p-Nitrophenol Zweiwertige Phenole OH OH OH Hydrochinon OH Brenzkatechin OH Resorcin OH Phenole sind stärkere Säuren als Alkohole. Sie lassen sich in wässriger Lösung (z. B. mit Natronlauge) deprotonieren. Herstellung von Ethanol Rohrzucker CH 3 CH 2OH Melasse Zucker Getreide C6H 12O6 Glucose Stärke Vergärung mit Hefe Fuselöle 2 C2H 5OH + 2 CO2 (anaerob; alkoholische Gärung) Fuselöle: CH 3 CH 2 CH 2OH Propanol CH 3 CH CH 2OH CH 3 CH 3 CH 2 CH CH 2OH 2-Methyl-1-butanol CH 3 2-Methyl-1-propanol CH 3 CH CH 2 CH 2OH 3-Methyl-1-butanol CH 3 Alle Alkohole sind giftig! Ethanol ist (u.a.) ein Hypnotikum. Reines Ethanol ist für Organismen aller Art ein starkes Gift; bei Mikroorganismen wird das Protoplasma-Protein denaturiert. Daher werden Bakterien in 70%igem Ethanol abgetötet oder in ihrer Entwicklung gehemmt. Ethanol dient deshalb auch als Konservierungsmittel im Haushalt und für anatomische Präparate. Industrielle Herstellung von Alkoholen 1. 2. 3. CO + 2 H2 H2C CH2 + H2O H2C CH2 + H2O Katalysator 250°C, 50 bar H3PO4 Δ O Oxacyclopropan (Ethylenoxid) 4. C6H5Cl + H2O Ca3(PO4)2 CH3OH CH3CH2OH Hefe - CO2 HOCH2CH2OH C6H5OH + HCl Glucose Chemische Reaktionen von Alkoholen und Phenolen Alkohole und Phenole sind Brönstedt-Säuren und Basen (Ampholyte). +H O R H Base O R H + H2O Säure R O H H Oxonium-Ion R O + H3O+ Alkoholat-Ion PhOH >> MeOH > prim. > sek. > tert. Alkohol pKa Acidität NO 2 O2N OH NO 2 2,4,6-Trinitrophenol Pikrinsäure Starke Säure; pK S = 0.25 Oxidation von Alkoholen Primärer Alkohol R CH 2 OH [O] R C -2H O H [O] R C O OH Carbonsäure Aldehyd meist nicht stabil, wird weiter oxidiert [O] º Oxidationsmittel z. B. CrO 3; K 2Cr2O7 (Vgl. Folie 106) Sekundärer Alkohol R1 R2 [O] CH OH R1 R2 C O Keton R1 = R2 = CH3: Aceton, einfachstes Keton Tertiärer Alkohol R1 R2 C OH R3 Primäre, sekundäre und tertiäre Alkohole lassen sich an Hand ihres Oxidationsverhaltens unterscheiden. Nucleophile Substitution R−X + :B(-) → R−Y + :X(-) :B(-) Nucleophil = Kern-liebend Beispiele für Nucleophile: OH(-), R−O(-), Hal(-); auch Neutral-Moleküle wie H2O, R−OH, NH3, ... Beispiel: R−X + OH(-) → R−OH + X(-) Halogenalkan Alkohol Nach der Kinetik lassen sich zwei verschiedene Mechanismen unterscheiden: SN2 bimolekulare Reaktion RG = -d[R−X]/dt = k[R−X][B(-)] Regelfall SN1 monomolekulare Reaktion RG = -d[R−X]/dt = k [R−X] Nur bei tertiären Gruppen R. Nucleophile Substitution SN1 R−X + :B(-) → R−B + :X(-) SN1 monomolekulare Reaktion RG = -d[R−X]/dt = k [R−X] Die Reaktion ist zweistufig und nicht stereoselektiv. Im 1. Schritt erfolgt die heterolytische Spaltung der R−X-Bindung, und es entsteht ein (tertiäres) Carbenium-Ion. R1 B sp3 sp2 R1 C C X R2 R3 - X(-) (a) R1 sp3 C R2 Produkt I R3 (+) + B(-) R2 R3 planares Carbenium-Ion R1 (b) sp3 C B Produkt II R2 R3 Die Produkte I und II entstehen im Verhältnis 1 : 1 (als Racemat). Nucleophile Substitution SN2 R−X + :B(-) → R−B + :X(-) SN2 bimolekulare Reaktion RG = k[R−X][B(-)] EA = Aktivierungsenergie Die Reaktion ist einstufig und stereospezifisch unter Konfigurations-Inversion. Im Übergangszustand ist das Reaktionszentrum sp2-hybridisiert. sp2 sp3 sp3 Beispiele für die nucleophile Substitution Nu + geladenes Nucleophil R X R Nu Halogenalkan (X = Cl, Br, I) HO R OH Alkohol R O R O R Ether R S R S R Thioether R I Iodalkan I X - Halogenid H Nu + neutrales Nucleophil H R X + X R X - Halogenalkan R Nu H X -H X O R OH O R O R H H3 N R NH2 prim. RNH2 R NHR sek. R2 N R NR2 tert. R Nu H R H Amine Eliminierungsreaktion Als Konkurrenz zur nucleophilen Substitution wird die 1,2- oder β-Eliminierung beobachtet (Jedes Nucleophil ist eine Base!). Auch diese kann monomolekular (E1) oder bimolekular (E2) auftreten. Dabei werden C,C-Mehrfachbindungen gebildet. Es handelt sich um die Umkehrung der elektrophilen Addition. H H H3C C CH2 H3C CH X Base - HX H3C H CH3 + H3C H 2-Methyl-2-buten Saytzeff-Produkt H3C H3C H H H 3-Methyl-1-buten Hofmann-Produkt Das Verhältnis von Saytzeff und Hofmann-Produkt hängt vom jeweiligen Reaktionssystem und von den Reaktionsbedingungen ab. Normalerweise überwiegt das thermodynamisch stabilere Saytzeff-Produkt. Carbonylverbindungen: Aldehyde O R = H, Alkyl, Aryl Name: alcoholus dehydrogenatus: der Aldehyd R C H Carbonyl-Gruppe Polare CO-Doppelbindung: δ+ δC O sp2 (planar) O O O HC H3C C H Formaldehyd Methanal H H3C CH2 C Acetaldehyd Ethanal Propionaldehyd Propanal O C H Benzaldehyd H Bindungsenergie [kJ/mol] C−O 351 C=O 707 C−C 348 C=C 595 O H3C CH2 CH2 C Butyraldehyd Butanal O C Salicylaldehyd H (o-Hydroxybenzaldehyd) OH H Carbonylverbindungen: Ketone R1 R2 O H 3 C C CH 3 Aceton Propanon C O R1, R2 = Alkyl, Aryl ≠ H H3C CH2 O C O C CH3 Ethylmethylketon Butanon CH 3 Methylphenylketon Acetophenon O O O Cyclohexanon Campher (Kampfer) O Progesteron Steroid-Hormon Reaktivität der Carbonylgruppe O δ- Elektrophile E C δ+ C acides H H Nucleophile Nu Addition von Nucleophilen an die C=O-Gruppe Eine der wichtigsten Reaktionen der organischen Chemie und der Biochemie δ+ δC O H H C OH C O H Nu H Nu Beispiele: R1 R2 C O Nu + H 2O R1 (H+) R2 + ROH R1 (H+) R2 Aldehyd: Keton: H O Hydroxyaldehyd: OH C Hydrat (meist nur in wässriger Lösung stabil) OH OH C OR + ROH R1 (H+) R2 Halbacetal Halbketal H C O (H+) OR + H 2O C OR Acetal Ketal O OH Cyclisches Halbacetal bei Zuckern: Furanosen und Pyranosen Addition von primären Aminen an Ketone R1 R2 C O + NH 2 R O C NH 2 R R2 R1 Nucleophil Halbaminal O R2 C N R Imin - H 2O Cyclohexanonoxim (Ausgangsprodukt für Nylon6) Cyclohexanon Hydroxylamin O R NH O R - H2O O + H2N Retinal R1 N OH + NH 2 OH H R1 OH - H 2O C NH R R2 N H blau: Polypeptidkette Aminosäure Lysin des Proteins Opsin NH Rhodopsin Sehpurpur Aldol-Kondensation 2 H3C C O OH OH (kat.) H3C CH CH 2 C H O - H 2O H3C CH CH C H 2-Butenal Crotonaldehyd 2-Hydroxybutanal Acetaldol Ethanal Acetaldehyd H C C O OH(-) - (-) C H(+) H O O C C C H O H (-) Enolat-Ion = C-Nucleophil H α-Deprotonierung C nucleophile Addition O C C H O - H2O C C O H H α,β-ungesättigte Aldol-Kondensation Carbonyl-Verbindung O H2O + H(+) C C O H O Aldol-Addition Eine sehr wichtige Reaktion zum Aufbau von Kohlenstoff-Gerüsten. Carbonylverbindungen: Carbonsäuren O R H O C C O H Bildung von Dimeren über Wasserstoffbrückenbindungen ⇒ hohe Siedepunkte ⇒ relativ gute Wasserlöslichkeit (bis Buttersäure) R O Siedepunkt R C O OH O H C OH O H3C C OH O H3C CH2 C OH O H3C CH2 CH2 C OH Ameisensäure (Methansäure) 101°C Essigsäure (Ethansäure) 118°C Propionsäure (Propansäure) 141°C Buttersäure (Butansäure) 164°C Dissoziation von Carbonsäuren O R C O H O + H2O R C R C O O + H3O mesomeres Carboxylat-Anion (Ladung ist delokalisiert) Beispiele: O O H C pKS O OH Ameisensäure 3.8 H3C C OH Essigsäure 4.8 Vergleich mit Alkoholen: R O H + H2O pKS ≈ 15 - 16 O H3C CH 2 C OH Propionsäure 4.9 R O + H3O Alkoholat-Anion (Ladung ist lokalisiert) Carbonsäuren sind wesentlich stärkere Säuren als Alkohole. Carbonsäuren mit zusätzlichen funktionellen Gruppen α O H3C CH C OH OH α-Hydroxycarbonsäure Milchsäure chiral O α O β H3C C CH2 C OH β-Ketosäure Acetessigsäure α α O R CH C OH NH 2 H 3C C C OH O α-Aminocarbonsäure: Aminosäure R ≠ H: chiral R = H: achiral: Glycin O C H α-Ketosäure Brenztraubensäure Pyruvat O O C O O OH C C CH 2 CH CH 2 C O OH H3C β Cα OH HO OH H Citronensäure Enolform 3-Carboxy-3-hydroxypentandisäure, eine Hydroxytricarbonsäure Reaktivität der Carboxylgruppe O C R elektrophil δδ+ O nucleophil, basisch H O δH δ+ C O C R' H acides H B H Nucleophile Substitution an der Carbonyl-Gruppe δ+ R C δO + O R C X Nu sp 3 Nu X sp2 R C O + X Nu sp2 • Es handelt sich um einen Additions-Eliminierungs-Mechanismus. • Die Reaktion kann durch Säuren katalysiert werden: Protonen-Katalyse Darstellung von Carbonsäurechloriden Es entstehen nur gasförmige Nebenprodukte. R C O OH + SOCl2 Thionylchlorid R C O Cl + SO 2 + HCl Reaktionen von Säurechloriden + H2 O R C O + HCl OH R´ OH R C O Cl H2 N R´ R C O + HCl O R´ Ester R C O + HCl NH R´ Amid R C O O Na O O R C O C R + Na Cl Anhydrid Säurechloride sind reaktive Acylierungs-Reagenzien. Carbonsäureanhydride H3C C O O O C O H3C C O Essigsäureanhydrid Acetanhydrid C OH OH C Phthalsäure C ΔT - H2O ΔT - H2O O O Phthalsäureanhydrid O O H3C C OH OH Salicylsäure + H3C C O O O Maleinsäureanhydrid O Synthese von Aspirin O C Maleinsäure O O O OH OH O C OH O + H3C C O C CH 3 Ester O Acetylsalicylsäure ASS OH Carbonsäureester Veresterung von Carbonsäuren O + R´ OH R C O H + H OH R C OH O R´ Gleichgewichtsreaktion: Das Gleichgewicht lässt sich durch Abdestillieren von H2O zur Ester-Seite verschieben. Die Reaktion wird durch starke Säuren katalysiert. Eigenschaften von Carbonsäureestern Einfache Ester sind in der Regel flüssig und haben relativ niedrige Siedepunkte. Z.B. CH3-CO2-C2H5 (“Essigester”): Sdp. 77° C, Schmp. –84° C. Sie sind in Wasser nicht löslich. Verwendung als Lösungsmittel (Lacke). Ester besitzen einen angenehm fruchtartigen Geruch. Sie sind Aroma- und Duftstoffe. Sie kommen verbreitet in Pflanzen, Blüten und Früchten vor. Ester Aroma Ester Ameisensäureethylester Rum Aroma Buttersäuremethylester Apfel Essigsäure-n-butylester Orange Buttersäureethylester Ananas Essigsäureisobutylester Banane Buttersäureisoamylester Birne Verseifung von Estern Ester-Hydrolyse (Verseifung) O + Na OH R C O R´ O O Na + OH O R C OR´ OH + HO R´ R C Neutralisation O R C + OH Säure + O R´ Base Mechanismus: Nucleophile Substitution Seife: Alkali-Salz einer Fettsäure Fette und Seifen Na + -OOC R CH 2 OH CH 2 O C R O CH O C R´ + 3 NaOH O CH 2 O C R´´ O Fett (Triglycerid) CH OH ++ Na OOC R´ Na + -OOC R´´ CH 2 OH Glycerin Seife COO(-) Na (+) hydrophil Lipophil bzw. hydrophob O 2 R C O 2 Na O wasserlöslich + Ca 2+ R C O Ca 2+ + 2 Na+ 2 wasserunlöslich In "hartem" Wasser sind Seifen unwirksam. Waschmittel und Detergenzien enthalten lineare, unverzweigte Alkansulfonate, die biologisch abbaubar sind. Die Salze reagieren neutral ⇒ Neutralseife SO3 K+ Ca2+- und Mg2+- Salze sind wasserlöslich. Fettsäuren Gesättigte Fettsäure Stearinsäure Octadecansäure 1 COOH 18 Ungesättigte Fettsäuren H 9 H 10 8 11 6 7 12 13 4 5 14 H 9 2 1 3 COOH 15 16 17 1 COOH H 12 18 18 H H Ölsäure (Z)-9-Octadecensäure Linolsäure (Z,Z)-9,12-Octadecadiensäure 1 H 9 COOH 18 H 12 H 15 H H H Linolensäure (Z,Z,Z)-9,12,15-Octadecatriensäure Wirkung von Tensiden Mizelle Fett unlöslich in H2O Seife löslich in H2O Fett löslich gemacht mit Seife in H2O Carbonsäureamide Synthesen O R C OH O + NH 3 R C HNH3 ΔT O R C - H 2O O Ammoniumcarboxylat Carbonsäure NH 2 P2O5 - H 2O Carbonsäurenitril R C N O R C Cl O + NHR'2 + HCl R C NR'2 Carbonsäurechlorid Nomenklatur O H C NH 2 Formamid H3C C O O H C NH 2 N CH 3 CH 3 N,N-Dimethylformamid Acetamid Cyclische Amide: Lactame α β RNH NH O β-Lactam (gespannter Vierring, hydrolyseempfindlich) O Penicilline .. O R C : NR2 S CH 3 N CH 3 COOH O N γ H γ-Lactam α β γ O NH δ ε ε-Lactam ε-Caprolactam (-) : O: R C NR2 (+) β α H Mesomerie: Die Amidbindung besitzt partiellen Doppelbindungscharakter. Kohlensäure-Derivate O + 2 HCl H2N NH 2 Harnstoff (Diamid der Kohlensäure) Cl + 2 NH3 Cl Phosgen (Säurechlorid) HO OH H 2CO3 Kohlensäure NH H2N O O CO 2H NH NH 2 Arginin α-Aminosäure O + H 2O H2N NH 2 + H2N Harnstoff CO 2H NH 2 Ornithin α-Aminosäure Harnstoff ist das Endprodukt des Eiweißabbaus bei Menschen und Säugetieren. Ein erwachsener Mensch produziert ca. 20 g/Tag. Die Hydrolyse von Arginin ist der letzte Schritt im Harnstoff-Zyklus.