Hartmut Köpf
Werbung

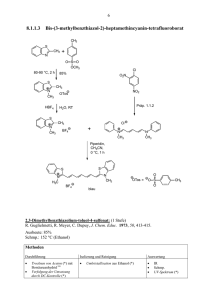
[l]Metallocenophane: 1H-NMR-Untersuchungen [l]Metallocenophanes: 1 H NMR Investigations Hartmut Köpf* Institut für Anorganische und Analytische Chemie der Technischen Universität Berlin, D-1000 Berlin 12, Deutschland und Nikolaos Klouras Institut für Anorganische Chemie, Universität Patras, Korinthoustraße 231, Patras, Griechenland Z. Naturforsch. 38b, 321-325 (1983); eingegangen am 15. Juni/24. November 1982 Bridged Metallocenes, [l]Hafnocenophanes, [l]Titanocenophanes, [lJZirconocenophanes The synthesis of a series of [ljmetallocenophanes has been achieved. The structure and conformation of these compounds are discussed in the light of their X H N M R spectra. Einleitung [lJMetallocenophan-halogenide lassen sich am besten nach folgendem Reaktionsschema darstellen [1-4]: LiC^H,- phanen, wie z.B. (CH3)2Si(C5H4)2TiCl2, wird durch die Verklammerung der beiden Fünfringe deren freie Rotation aufgehoben und es werden für die acht paarweise magnetisch gleichwertigen Ring- oder H x NaC5H5 R2ECI2 R2E Hierbei bedeuten: a l i c 4 h 9 R M'X E M Pentan Petrolether H MCI R2E' Pentan+THF z^1 Cl = = = = organischer Rest AgF, LiBr, K I C, Si, Ge Ti, Zr, H f M'X (I) Aceton Durch Abwandlung sowohl der Brücke als auch des Metallocen-Kerns, also durch systematisches Durchvariieren der verbrückenden Elemente E und der an ihnen haftenden Substituenten R einerseits sowie der Übergangsmetalle M und der an ihnen koordinierten Liganden X andererseits, haben wir eine größere Zahl von [l]Metallocenophanen synthetisiert und iH-NMR-spektroskopisch untersucht. Einfache Metallocene, wie z.B. (CsHs^TiCl^ zeigen in ihrem 1H-NMR-Spektrum wegen der freien Rotation der Cyclopentadienylringe für alle zehn Protonen ein scharfes Singulett [5]. Bei [l]Metalloceno* Sonderdruckanforderungen an Prof. Dr. A. Golloch. 0340-5087/83/0300-0326/S 01.00/0 protonen zwei triplettartige Multipletts vom AA'XX'-Kopplungstyp beobachtet [1], Abb. 1 zeigt dies an der analogen Zirkonium-Verbindung. Da die Verschiebungsdifferenz AT zwischen den AA'- und XX'-Teilspektren u.a. vom Grad der Winkelung der Cyclopentadienyl-Liganden abhängt [1,6], kann diese aus den Spektren experimentell zu ermittelnde Größe direkt Aufschlüsse über die Strukturverhältnisse der Komplexe geben. In der vorliegenden Arbeit wird anhand der 1 H-NMR-Spektren der Einfluß des verbrückenden Elements E, des Zentralatoms M oder des Liganden X auf die Verschiebungsdifferenz der Ringprotonen von [l]Metallocenophanen verfolgt und diskutiert. Dieses Werk wurde im Jahr 2013 vom Verlag Zeitschrift für Naturforschung in Zusammenarbeit mit der Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. digitalisiert und unter folgender Lizenz veröffentlicht: Creative Commons Namensnennung-Keine Bearbeitung 3.0 Deutschland Lizenz. This work has been digitalized and published in 2013 by Verlag Zeitschrift für Naturforschung in cooperation with the Max Planck Society for the Advancement of Science under a Creative Commons Attribution-NoDerivs 3.0 Germany License. Zum 01.01.2015 ist eine Anpassung der Lizenzbedingungen (Entfall der Creative Commons Lizenzbedingung „Keine Bearbeitung“) beabsichtigt, um eine Nachnutzung auch im Rahmen zukünftiger wissenschaftlicher Nutzungsformen zu ermöglichen. On 01.01.2015 it is planned to change the License Conditions (the removal of the Creative Commons License condition “no derivative works”). This is to allow reuse in the area of future scientific usage. 322 H . K ö p f - N . Klouras • Metallocenophane CHC1. JJUL AA Abb. 1. i H - N M R - S p e k t r u m von (CH3)2Si(C5H4)2ZrCl2 und Strukturmodell der Verbindung. XX' Experimenteller Teil Diskussion der 1 H-NMR-Spektren 1. Allgemeines 1. Einfluß des verbrückenden Elements E auf die V erSchiebung sdiff er enz Sämtliche Operationen unter Beteiligung metallorganischer Reagenzien wurden unter Argonatmosphäre mit absolut trockenen, luftfreien Lösungsmitteln durchgeführt. Die Isolierung und Reinigung der luftstabilen Metallocenophan-dihalogenide erfolgte unter Luftzutritt. Schmelzpunkte wurden mit einem Kofler-Heiztischmikroskop (Reichert Thermovar) bestimmt. Elementaranalysen wurden von Prof. Dipl.-Ing. Dr. H. Malissa und G. Reuter, Analytische Laboratorien, 5270 Gummersbach 1, Elbach, durchgeführt. Zur massenspektroskopischen Bestimmung (Varian MAT 311 A) von Molmassen wurde der intensivste Peak des Isotopenmusters des jeweiligen Molekülions ausgewertet. 1H-NMR-Spektren wurden bei 60 MHz an gesättigten Lösungen in CDCI3 gegen CHCI3 als inneren Standard gemessen (Varian A 60); angegebene Werte sind auf den Standard Si(CH3)4 umgerechnet. 2. Bis(cyclopentadienyle) Alle Bis(cyclopentadienyle) wurden direkt oder analog nach Literaturangaben hergestellt und durch Vakuumdestillation gereinigt [7-9]. Da diese Verbindungen bei längerem Stehen zerfallen, wurden sie gleich weiter umgesetzt oder bis zum Verbrauch bei tiefer Temperatur aufbewahrt. 3. [1[Metallocenophane Gemäß Reaktionsschema (I) waren die [l]Metallocenophandichloride aus den entsprechenden Bis(cyclopentadienylen) durch Dimetallierung mit nButyllithium in Petrolether oder Benzol und nachfolgende Umsetzung mit Metall-tetrachlorid unter Zugabe von THF zugänglich. Ausgehend von den Chloriden konnten weiter die restlichen [l]-Metallocenophan-dihalogenide (Tab.I) durch Austauschreaktionen synthetisiert werden. Die Versuchsergebnisse sind in der Tab. I zusammengestellt. Die Verschiebungsdifferenz A r zwischen AA'- und XX'-Ringprotonen sollte, wie verschiedentlich festgestellt wurde [1, 6], u.a. vom Schnittwinkel der Fünfringebenen abhängen. Bei abnehmender Brükkengröße (CH2)3 > Ge(CH3)2 > Si(CH3)2 > CH2 nehmen, wie Tab. II zeigt, die Ar-Werte und damit die Schrägstellung der Ringliganden zu (beim gleichen Zentralatom nimmt cp ab, Abb. 1). Es wäre denkbar, daß ein induktiver Effekt wegen Elektronegativitätsdifferenzen zwischen den Brükkenatomen - besonders zwischen C und Si - das AA'-Signalmuster in die gleiche Richtung wie der sterische Faktor verschieben könnte. Da aber bei (I) und (IV) trotz fast gleicher Elektronegativität eine sprunghafte Zlr-Änderung beobachtet wird, kann man den elektronischen Faktor vernachlässigen und das Variieren der Brückengröße für dieses Phänomen verantwortlich machen. 2. Einfluß des Zentralatoms E auf die Verschiebungsdifferenz Die A r-Werte kann man auch durch Zentralatomwechsel beeinflussen. Mit steigendem Radius der Zentralatome (Ti->Hf) nehmen hier die A r-Werte ab (Tab. III). 3. Einfluß der Liganden X auf die Verschiebungsdifferenz Ein Halogenaustausch bei (CÖH 5 ) 2 MX 2 in der Reihe X = F, CL, Br, I verschiebt das Signal der Ringprotonen zu tieferem Feld, obwohl nach Elektronegativitätskriterien die abnehmende Entschirmungswirkung in dieser Reihe zu größeren r-Werten 323 H . K ö p f - N . Klouras • Metallocenophane Tab. I. Darstellung und Charakterisierung v o n [l]Metallocenophanen. Verbindung Umkrist. aus Farbe A u s b . Schmp. [% [°C] d.Th.] Summenformel Molmasse gef. (ber.) Elementaranalyse gef. (ber.) [ % ] C H Hai. H 2 C(C 5 H 4 ) 2 TiCl 2 [11] CHC1 3 dunkelrot 23 CuHioCl2Ti 260(261,0) CH 3 CH(C 5 H 4 ) 2 TiCl 2 CHC1 3 dunkelbraun ab 220 C i 2 H i 2 a 2 T i 274(275,0) CH 3 SiH(C 5 H 4 ) 2 TiCl 2 Benzol rotbraun (CH 3 ) 2 Si(C 5 H 4 ) 2 TiCl 2 [l] CHC1 3 (CH 3 ) 2 Si(C 5 H 4 ) 2 ZrCl 2 50,42 3,55 27,08 (50,62)(3,86)(27,17) 52,81 4,75 25,45 (52,41) (4,40) (25,78) 45,02 4,38 24,14 (45,38) (4,15) (24,36) 46,98 5,01 22,99 (47,24) (4,63) (23,24) 41,72 3,79 20,60 (41,36) (4,05) (20,35) 33,48 3,16 16,21 (33,08) (3,24) (16,27) 50,43 5,30 21,19 (50,47)(5,45)(21,28) 41,07 4,45 20,02 (41,31) (4,05) (20,28) 36,28 3,40 17,86 (36,67) (3,59) (18,06) 52,48 5,32 13,60 (52,94)(5,18)(13,96) 36,39 3,56 40,35 (36,58) (3,58) (40,56) 32,59 3,11 16,41 (32,96) (3,23) (16,21) 29,85 2,97 51,88 (29,53) (2,89) (52,00) 27,50 2,68 47,71 (27,13)(2,66)(47,76) Z. 305 6 Z. 5 Z . 180-190 C n H i 2 C l 2 S i T i 290(291,1) 7 Z . 250-270 Ci 2 Hi 4 Cl 2 SiTi 304(305,1) Toluol hellgelb 10 Z. 3 1 4 - 3 1 5 Ci 2 Hi 4 Cl 2 SiZr 346(348,4) (CH 3 ) 2 Si(C 5 H 4 ) 2 HfCl 2 Toluol gelblichweiß 10 Z. 301-303 Ci 2 Hi 4 Cl 2 SiHf 438(435,0) (C 2 H 5 ) 2 Si(C 5 H 4 ) 2 TiCl 2 Toluol purpurrot 10 (CH 3 ) 2 Ge(C 5 H 4 ) 2 TiCl 2 [l] Toluol hellbraun 2 dunkelbraun 190 Ci 4 Hi 8 Cl 2 SiTi 332(333,1) 56 Z. 185-186 Ci 2 Hi 4 Cl 2 GeTi nicht gemessen Z. 162-170 Ci 2 Hi 4 Cl 2 GeZr nicht gemessen Z. 1 9 1 - 1 9 6 C i 2 H i 4 F 2 S i T i 272(272,2) 31 Z. 2 (CH 3 ) 2 Ge(C 5 H 4 ) 2 ZrCl 2 Toluol hellgelb (CH 3 ) 2 Si(C 5 H 4 ) 2 TiF 2 Toluol (CH 3 ) 2 Si(C 5 H 4 ) 2 TiBr 2 Toluol braunschw. (CH 3 ) 2 Si(C 5 H 4 ) 2 ZrBr 2 Toluol grünlich 5 (CH 3 ) 2 Si(C 5 H 4 ) 2 TiI 2 Toluol schwarz 47 Z. 318-319 Ci 2 Hi 4 Br 2 SiZr nicht gemessen Z. ab 250 Ci 2 Hi 4 I 2 SiTi 488(488,0) (CH 3 ) 2 Si(C 5 H 4 ) 2 ZrI 2 Toluol 43 Z. orange olivgrün führen sollte [10]. Dies wurde durch die Bildung einer p.T->djr-Rückbindung zwischen Halogen und Zentralatom interpretiert [5], die beim F am stärksten T a b . I I . A b h ä n g i g k e i t der Verschiebungsdifferenz AT zwischen A A ' - u n d X X ' - R i n g p r o t o n e n v o n der B r ü k kengröße in Titanocenophanen. T AA' (I) (II) (III) (IV) (C6H4) (H 2 C) 3 (C 5 H 4 ) 2 TiCl 2 [6] 3,51(4)m (CH 3 ) 2 Ge(C 5 H 4 ) 2 TiCl 2 [l]2,79(4)t (CH 3 ) 2 Si(C 5 H 4 ) 2 TiCl 2 [l] 2,75(4)t H 2 C(C 5 H 4 ) 2 TiCl 2 [11] 3,02(4)t XX' AT 3,55(4)m 4,00(4)t 4,00(4)t 4,37(4)t 0,04 1,21 1,25 1,35 T a b . I I I . A b h ä n g i g k e i t der Verschiebungsdifferenz Ar zwischen A A ' - und X X ' - R i n g p r o t o n e n v o n der Zentralatomgröße in [l]Metallocenophanen. ab 260 C i 2 H i 4 B r 2 S i T i 392(396,0) ab 305 Ci 2 Hi 4 I 2 SiZr 530(531,3) sein soll. Mit anderen Worten: von den zwei in Konkurrenz stehenden Phänomenen, dem induktiven und dem Mesomerieeffekt, herrscht hier der Mesomerieeffekt vor. Ferner taucht das CsHs-Signal von (C5H5)2TiF2 im iH-NMR-Spektrum wegen 19 F- 1 H-Kopplung als Triplett auf. Die Kopplungskonstante von 1,7 Hz ist jedenfalls so klein, daß bei Zunahme der Bindungslängen M-F in den entsprechenden Zr- und Hf-Verbindungen keine derartige Kopplung mehr erkennbar ist [10]. Ähnliche Phänomene beobachtet man, wie Tab. IV zeigt, auch bei den neuen Verbindungen (V)-(VIII). T a b . I V . A b h ä n g i g k e i t der Verschiebungsdifferenz Ar zwischen A A ' - und X X ' - R i n g p r o t o n e n v o m Liganden X in [l]Titanocenophanen. T T AA' (CH 3 ) 2 Si(C 5 H 4 ) 2 TiCl 2 [1] (CH 3 ) 2 Si(C 5 H 4 ) 2 ZrCl 2 (CH 3 ) 2 Si(C 5 H 4 ) 2 HfCl 2 (C5H4) 2,75(4)t 3,02(4) t 3,10(4) t XX' AT 4,00(4)t 4,00(4) t 4,07(4) t 1,25 0,98 0,97 AA' (V) (VI) (VII) (VIII) (CH 3 ) 2 Si(C 5 H 4 ) 2 TiI 2 (CH 3 ) 2 Si(C 5 H 4 ) 2 TiBr 2 (CH 3 ) 2 Si(C 5 H 4 ) 2 TiCl 2 [l] (CH 3 ) 2 Si(C 5 H 4 ) 2 TiF 2 (C5H5) l,88(4)t 2,47(4)t 2,75(4)t 3,25(4)t XX' AT 4,13(4)t 4,02(4)t 4,00(4)t 3,98(4)t 2,25 1,55 1,25 0,73 H . K ö p f - N . Klouras • Metallocenophane 324 CHC1. (V) J* A b b . 2. (a) A A ' - u n d X X ' - S i g n a l e der R i n g p r o t o n e n der 1 H - N M R - S p e k t r e n v o n ( V ) - ( V I I I ) . (b) D e n k b a r e sterisehe W i r k u n g des H a l o g e n s a u f die S c h r ä g s t e l l u n g der C y c l o p e n t a d i e n y l - R i n g e in den [1]T i t a n o c e n o p h a n e n (V) - ( V I I I ) . ' (VI) i Me^ ^ Me (a) ( (VII) X ^ / ' N Me/' Me \ Si (?) (VIII) (b) Hier verschiebt sich das AA'-Teilspektrum in der gleichen Weise wie das CsHa-Signal der oben erwähnten nichtverbrückten Komplexe (Abb. 2a), während das XX'-Signalmuster ungefähr den gleichen r-Wert beibehält. Dies erinnert an die vorher beschriebene Abhängigkeit der Ar-Werte vom Schnittwinkel der Fünfringebenen bei unterschiedlichen Brückengrößen. Zur Deutung könnte man eine analoge sterisehe Wirkung des Halogens, wie Abb. 2b zeigt, heranziehen. Gegen diese Interpretation spricht jedoch die Tatsache, daß wie bei den entsprechenden Metallocenen wahrscheinlich gemacht wurde [5], die Bildungsmöglichkeit einer pn-+dji-Bindung zwischen Halogen und Zentralatom berücksichtigt werden muß. Außerdem erwartet man bei Berücksichtigung von räumlichen Einflüssen ein Anwachsen von Ar mit steigender Größe des Zentralatoms M, was den Befunden widerspricht (Tab. III). Die Effekte lassen sich jedoch verstehen, wenn man annimmt, daß bei [l]Metallocenophanen der in verschiedenen Röntgenstrukturanalvsen für (C5Hö)2MX2-Derivate ge- fundene Wert [12-14] des Winkels <p von 120-150° am Zentralatom M dadurch aufrechterhalten wird, daß der Winkel co am Fünfringzentrum zu kleineren Werten als 90° deformiert wird (vgl. Abb. 1 und 3). Als Folge davon sind die Abstände vom Metallatom zum substituierten C-Atom und den a-ständigen C-Atomen der Fünfringliganden kürzer als die zu den ^-ständigen, wie es durch eine Röntgenstrukturanalyse an (CH3)2Si(C5H4)2TiCl2 gezeigt wurde [15]. Zur Erklärung der Verschiebung des iH-NMR- R 2E A b b . 3. V e r f e i n e r t e s S t r u k t u r m o d e l l f ü r cenophandihalogenide. [l]Metallo- 325 H. K ö p f - N . Klouras • Metallocenophane AA' (ppm) A b b . 4. Abhängigkeit der Verschiebungsdifferenz Ar und der TAA'-Werte von der Elektronegativität (AllredRochow-Skala) des Halogens in ( V ) - ( V I I I ) . Signals der AA'-Protonen an den a-C-Atomen könnte man somit einen auf diese Protonen stärkeren Einfluß des Mesomerieeffekts der Halogenliganden als auf die /^-ständigen heranziehen. Ein ähnlich „einseitiger" Verschiebungseffekt auf das XX'-Teilspektrum wurde bei der Verbindung (CHa^S^CsH^TiSs diskutiert [1]. Zum besseren Verständnis dieses Phänomens geht man von der Iod-Verbindung aus, wobei die Tendenz zur Rückbindung nicht groß ist und der induktive Effekt dominiert; die AA'-Protonen werden entschirmt und das AA'-Signal verschiebt sich zum tieferen Feld. Bei der Brom- bzw. Chlor-Verbindung nimmt der Einfluß des induktiven Effekts wegen des stärkeren, entgegengerichteten mesomeren Effekts ab; das AA'-Signal wandert zu höherem Feld. Den größten r-Wert erreichen die AA'-Protonen bei der Fluor-Verbindung, wobei der Elektronenfluß durch die Rückbindung vom Halogen- über das Metallatom in das .^-System der Cyclopentadienylringe hinein diese Protonen stark abschirmt. Eine schwache 19 F- 1 H-Kopplung führt hier zu multiplettartigen AA'- und XX'-Signalen. Abb. 4 zeigt, wie sich die Verschiebungsdifferenz Ar und der r AA/ -Wert bei diesen Verbindungen mit der Elektronegativität des Halogens ändern. [1] H . K ö p f und W . K a h l , J . Organomet. Chem. 64, C 37 (1974). [2] H . K ö p f und N . Klouras, Chemiedozenten-Tagung Regensburg, Referateband, B 60 (1976). [3] N . Klouras und H . K ö p f , Monatsh. Chem. 112, 887 (1981). [4] P . Köpf-Maier, W . K a h l , N . Klouras, G. H e r m a n n und H . K ö p f , Eur. J . Med. Chem. 16, 275 (1981). [5] H . C. Beachell und S. A . Butter, Inorg. Chem. 4, 1133 (1965). [6] M. Hillmann und A . Weiss, J . Organomet. Chem. 42, 123 (1972). [7] R . Riemschneider und R . Nehring, Monatsh. Chem. 90, 568 (1959). [8] H . Schaltegger, M. Neuenschwander und D . Meuche, Helv. Chim. A c t a 48, 955 (1965). [9] E . W . Abel, M. O. Dunster und A . Waters, J . Organomet. Chem. 49, 287 (1973). [10] P . Druce, B . Kingston, M. Läppert, T . Spalding und R . Srivastava, J. Chem. Soc. A 1969, 2106. [11] T. K a t z , X . A c t o n und G. Martin, J . A m . Chem. Soc. 95, 2934 (1973). [12] G. N a t t a , P . Corradini und I. W . Bassi, J . A m . Chem. Soc. 80, 775 (1958). [13] N . V . Alekseev und I. A . R o n o v a , Zh. Strukt. K h i m . 7, 101 (1966). [14] J. L . Petersen und L . F . Dahl, J. A m . Chem. Soc. 97, 6422 (1975). [15] H . K ö p f und J. Pickardt, Z. Naturforsch. 36b, 1208 (1981). 4. Einfluß der Substituenten R auf die Verschiebungsdifferenz Wie man aus der Tab. V entnehmen kann, werden die A r-Werte durch den Austausch der Substituenten R kaum beeinflußt. T a b . V . Abhängigkeit der Verschiebungsdifferenz Ar zwischen A A ' - und X X ' - R i n g p r o t o n e n v o m Substituenten R in [l]Titanocenophanen. AA' CH 3 SiH(C 5 H4)2TiCl2 (CH3)2Si(C5H4)2TiCl2 [1] (C 2 H5)2Si(C5H4) 2 TiCl 2 T(C6H4) 2,88(4)t 2,75(4)t 2,73(4)t XX' Ar 4,06(4)q 4,00(4)t 3,95(4)t 1,18 1,25 1,22 Für die finanzielle Unterstützung dieser Arbeit danken wir dem Fonds der Chemischen Industrie.