5.1.2 - IOC
Werbung

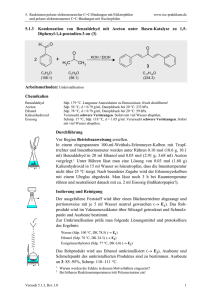
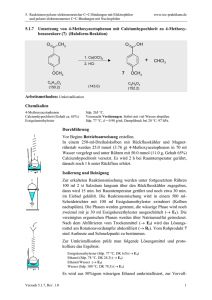
5. Reaktionen polarer elektronenreicher C=C-Bindungen mit Elektrophilen und polarer elektronenarmer C=C-Bindungen mit Nucleophilen www.ioc-praktikum.de 5.1.2 Kondensation von Benzaldehyd mit Aceton unter Basen-Katalyse zu E-4-Phenyl3-buten-2-on (2) H O O O + KOH / EtOH H3C CH3 CH3 2 C7H6O (106.1) C3H6O (58.1) C10H10O (146.2) Arbeitsmethoden: Feststoffdestillation Chemikalien Benzaldehyd Aceton Ethanol tert-Butylmethylether Kaliumhydroxid Eisessig n-Pentan Sdp. 179 °C. Langsame Autoxidation zu Benzoesäure, frisch destillieren! Sdp. 56 °C, d = 0.79 g/ml, Dampfdruck bei 20 °C: 233 hPa. Sdp. 78 °C, d = 0.79 g/ml, Dampfdruck bei 20 °C: 59 hPa. Sdp. 55 °C, d = 0.74 g/ml, Dampfdruck bei 20 °C: 268 hPa. Verursacht schwere Verätzungen. Sofort mit viel Wasser abspülen. Schmp. 17 °C, Sdp. 118 °C, d = 1.05 g/ml. Verursacht schwere Verätzungen. Sofort mit viel Wasser abspülen. Sdp. 36 °C, d = 0.63 g/ml, Dampfdruck bei 20 °C: 573 hPa. Durchführung Vor Beginn Betriebsanweisung erstellen. In einem 100-ml-Dreihalskolben mit Tropftrichter und Innenthermometer werden unter Rühren 0.10 mol (10.6 g) Benzaldehyd in 20 ml Ethanol und 0.30 mol (17.4 g, 22.0 ml) Aceton vorgelegt.1 Unter Rühren lässt man eine Lösung von 5.0 mmol (0.28 g) Kaliumhydroxid in 5 ml Wasser so hinzutropfen, dass die Innentemperatur nicht über 25 °C steigt. Nach beendeter Zugabe wird noch 3 h bei Raumtemperatur gerührt und mit 0.5 ml Eisessig neutralisiert (Indikatorpapier). Isolierung und Reinigung Wasser Versuch 5.1.2, Rev. 1.0 Das Reaktionsgemisch wird in einen Scheidetrichter überführt, mit 80 ml Wasser versetzt und die organische Phase abgetrennt. Die wässrige Phase wird dreimal mit je 30 ml tert-Butylmethylether ausgeschüttelt (→ E1). Die organische und die etherischen Phasen werden vereinigt und über Natriumsulfat getrocknet. Nach dem Abfiltrieren des Trockenmittels (→ E2) wird das Lösungsmittel am Rotationsverdampfer unter vermindertem Druck abdestilliert (→ R1) und der verbleibende Rückstand in einer Feststoffdestillationsapparatur bei vermindertem Druck destilliert. Der Siedepunkt des Produktes ist im Bereich von 138– 140 °C/ 21 hPa zu erwarten (→ E3). Das Rohprodukt wird in der zum Lösen bei etwa 25 °C notwendigen Menge n-Pentan aufgenommen und in einem Eis/ Kochsalz-Bad zur Kristallisation gebracht. Nach dem Absaugen (→ E4) wird das Produkt im Vakuumexsikkator getrocknet und Ausbeute und Schmelzpunkt bestimmt. Ausbeute an 2: 35–45%, Schmp. 37 °C. 1 5. Reaktionen polarer elektronenreicher C=C-Bindungen mit Elektrophilen und polarer elektronenarmer C=C-Bindungen mit Nucleophilen www.ioc-praktikum.de 1 Warum werden die Edukte in diesem Molverhältnis eingesetzt? 2 Bei höheren Reaktionstemperaturen tritt Polymerisation ein! Hinweise zur Entsorgung (E), Recycling (R) der Lösungsmittel E1: E2: E3: E4: R 1: Wässrige Lösung mit Spuren von organischen Verbindungen → Entsorgung (H2O mit RH). Kontaminiertes Natriumsulfat → Entsorgung (Anorg. Feststoffe). Destillationsrückstand in wenig Aceton lösen → Entsorgung (RH). Mutterlauge mit organischen Verunreinigungen → Entsorgung (RH). Abdestilliertes Lösungsmittel → Recycling (tert-Butylmethylether). Auswertung des Versuchs H-NMR-Spektrum von 2 (300 MHz, CDCl3): δ = 2.35 (3 H), 6.69 (1 H), 7.33–7.41 (3 H), 7.45–7.56 (3 H). 2017.1 Hz 2000.7 Hz 2256.4 Hz 2240.0 Hz 1 7.5 8.0 7.0 6.0 7.0 5.0 6.5 4.0 3.0 2.0 [ppm] 0.0 C-NMR Spektrum von 2 (75.5 MHz, CDCl3): δ = 27.54 (CH3), 127.16 (CH), 128.28 (CH), 128.99 (CH), 130.54 (CH), 134.42 (C), 143.45 (CH), 198.40 (C). 13 LM 200 180 160 Versuch 5.1.2, Rev. 1.0 140 120 100 80 60 40 20 [ppm] 0 2 5. Reaktionen polarer elektronenreicher C=C-Bindungen mit Elektrophilen und polarer elektronenarmer C=C-Bindungen mit Nucleophilen www.ioc-praktikum.de IR-Spektrum von 2 (Film): 100 T [%] 2920 3000 3060 50 3025 1670 0 4000 3000 1575 1610 1690 2000 1500 1000 -1 ~ ν [cm ] * Formulieren Sie den zu 2 führenden Reaktionsmechanismus. * Vergleichen Sie das Ergebnis dieses Versuchs mit dem von Versuch 5.1.3. Weitere denkbare Reaktionsprodukte: HO O O O H C OH 3 CH3 H3C CH3 B A O C CH3 D * Mit welchen spektroskopischen Daten lassen sich A–D ausschließen? * Diskutieren Sie die denkbaren Reaktionsmechanismen. In welchem Zusammenhang stehen 2/A und B/D? Literatur, allgemeine Anwendbarkeit der Methode Literatur, auf der dieser Versuch beruht: [1]. Aldolreaktionen zwischen Aldehyden und Ketonen führen nur dann zu einheitlichen Produkten, wenn der Aldehyd kein α-H besitzt und somit nur als Elektrophil reagieren kann (Benzaldehyd, Pivalaldehyd (Me3CCHO), Formaldehyd), das Keton muss das Nucleophil bilden können. Unter diesen Voraussetzungen besitzt die als Claisen-Schmidt-Reaktion bezeichnete "gekreuzte Aldolreaktion" eine große Anwendungsbreite. Die Produkte mit aromatischen Aldehyden unterliegen direkt der Wasserabspaltung (Aldolkondensation) zu α,β-ungesättigten Carbonylverbindungen, mit aliphatischen Aldehyden bleibt die Umsetzung auf der Aldoladditionsstufe stehen: H Ph H O C CH2 + OH - H2O C R OH O C CH R' H3C - OH R O PhHC CH C R R H + H C OH O O R' Ph C CH2 OH O C R' = Alkyl R [1] N.L. Drake, P. Allen in Organic Syntheses Coll. Vol. 1 (Hrsg. H. Gilman, A.H. Blatt), J. Wiley & Sons, New York, 1941, S. 77–78. Versuch 5.1.2, Rev. 1.0 3
![6.3.1 1-Oxa-spiro[2.5]octan - Institut für Organische Chemie](http://s1.studylibde.com/store/data/001356875_1-96e669e5c88ad586db9f9f199d424d05-300x300.png)